名校
解题方法
1 . 向一定量铁的氧化物 (铁只有+2、+3价)中,加入100ml2mol/L稀盐酸,恰好使固体完全溶解,再向所得溶液中通入标准状况下448mL氯气,恰好能使溶液中的FeCl2完全转化为FeCl3,则x:y为
(铁只有+2、+3价)中,加入100ml2mol/L稀盐酸,恰好使固体完全溶解,再向所得溶液中通入标准状况下448mL氯气,恰好能使溶液中的FeCl2完全转化为FeCl3,则x:y为
 (铁只有+2、+3价)中,加入100ml2mol/L稀盐酸,恰好使固体完全溶解,再向所得溶液中通入标准状况下448mL氯气,恰好能使溶液中的FeCl2完全转化为FeCl3,则x:y为
(铁只有+2、+3价)中,加入100ml2mol/L稀盐酸,恰好使固体完全溶解,再向所得溶液中通入标准状况下448mL氯气,恰好能使溶液中的FeCl2完全转化为FeCl3,则x:y为| A.1:1 | B.2:3 | C.3:4 | D.4:5 |
您最近一年使用:0次
2024-08-25更新
|
238次组卷
|
3卷引用:第三章 铁 金属材料【单元测试B卷】
解题方法
2 . 装置如图所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。请回答:___________ 极,C极的电极反应式为___________ ,一段时间后丁中X极附近的颜色逐渐___________ (填“变深”或“变浅”)。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成,对应单质的物质的量之比为___________ 。
(3)现用丙装置给铜件镀银,则H应该是___________ (填“铜”或“银”),电镀液是___________ 溶液。常温下,当乙中溶液的c(OH-)=0.1mol·L-1时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为___________ g,甲中溶液的酸性___________ (填“变大”“变小”或“不变”)。

(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成,对应单质的物质的量之比为
(3)现用丙装置给铜件镀银,则H应该是
您最近一年使用:0次
3 . 某研究小组对铁生锈进行研究。
(1)甲同学设计了A、B、C一组实验(如图),探究铁生锈的条件。
①通过上述实验现象分析,可得出铁生锈的外部条件是___________ 。
②由于与金属接触的介质不同,金属腐蚀分成不同类型,本实验中铁生锈属于___________ ,正极电极反应式为___________ 。
③实验B所用的水要经过___________ 处理;植物油的作用是___________ 。
④实验C中碱石灰的作用是___________ 。
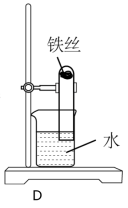
(2)乙同学为了达到同样目的,设计了实验D(如图),发现一段时间后,试管中的液面升高,其原因是___________ ,该实验___________ (填“能”或“不能”)说明水对铁钉生锈产生影响。
(1)甲同学设计了A、B、C一组实验(如图),探究铁生锈的条件。

①通过上述实验现象分析,可得出铁生锈的外部条件是
②由于与金属接触的介质不同,金属腐蚀分成不同类型,本实验中铁生锈属于
③实验B所用的水要经过
④实验C中碱石灰的作用是
(2)乙同学为了达到同样目的,设计了实验D(如图),发现一段时间后,试管中的液面升高,其原因是
您最近一年使用:0次
4 . 电化学在现代生活、生产和科学技术的发展中发挥着越来越重要的作用。
(1)图1是利用燃料电池工作原理处理某酸性废水的示意图。b电极的电极反应式为___________ 。 和
和 是主要大气污染物,图2是同时吸收
是主要大气污染物,图2是同时吸收 和
和 的示意图。
的示意图。___________ 极(填“正”或“负”。)
②阳极的电极反应式为___________ 。
③当 均为NO时,吸收池中发生反应的氧化剂与还原剂的物质的之比为
均为NO时,吸收池中发生反应的氧化剂与还原剂的物质的之比为___________ 。
(3)图3是甲醇( )燃料电池的工作原理示意图。
)燃料电池的工作原理示意图。___________ 。
②若用该电池电解精炼铜,氧气放电电极应接___________ (填“纯铜”或“粗铜”。)
(4)如图是高铁酸钾电池的模拟实验装置(已知:放电时,石墨电极附近有红褐色浑浊)。___________ 。
②盐桥中盛有饱和 溶液,此盐桥中
溶液,此盐桥中 向
向___________ (填“左”或“右”移动)。
(1)图1是利用燃料电池工作原理处理某酸性废水的示意图。b电极的电极反应式为

 和
和 是主要大气污染物,图2是同时吸收
是主要大气污染物,图2是同时吸收 和
和 的示意图。
的示意图。
②阳极的电极反应式为
③当
 均为NO时,吸收池中发生反应的氧化剂与还原剂的物质的之比为
均为NO时,吸收池中发生反应的氧化剂与还原剂的物质的之比为(3)图3是甲醇(
 )燃料电池的工作原理示意图。
)燃料电池的工作原理示意图。
②若用该电池电解精炼铜,氧气放电电极应接
(4)如图是高铁酸钾电池的模拟实验装置(已知:放电时,石墨电极附近有红褐色浑浊)。

②盐桥中盛有饱和
 溶液,此盐桥中
溶液,此盐桥中 向
向
您最近一年使用:0次
解题方法
5 . 电解的应用比较广泛,回答下列问题:
(1)由下列物质冶炼相应金属时采用电解法的是___________ (填字母,下同)。
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是___________ 。
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
e.若阳极质量减少64 g,则转移电子数为2NA个
f.SO 的物质的量浓度不变(不考虑溶液体积变化)
的物质的量浓度不变(不考虑溶液体积变化)
(3)如图为电解精炼银的示意图,___________ (填“a”或“b”)极为含有杂质的粗银,若b极有少量红棕色气体生成,则生成该气体的电极反应式为___________ 。___________ (填化学式)溶液,阳极电极反应式为___________ ,电解过程中Li+向___________ (填“A”或“B”)电极迁移。___________ 极,已知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴极电极反应式为___________ 。若改用AlCl3水溶液作电解液,则阴极产物为___________ 。
(1)由下列物质冶炼相应金属时采用电解法的是
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
e.若阳极质量减少64 g,则转移电子数为2NA个
f.SO
 的物质的量浓度不变(不考虑溶液体积变化)
的物质的量浓度不变(不考虑溶液体积变化)(3)如图为电解精炼银的示意图,


您最近一年使用:0次
解题方法
6 . 相同条件下,ag的A气体与bg的B气体占有相同体积,下列叙述错误的是
| A.a:b等于A与B的相对分子质量之比 |
| B.a:b等于等质量的A与B的分子数之比 |
| C.a:b等于同温同压下A与B的密度之比 |
| D.a:b等于同温同体积等质量的A与B的压强比 |
您最近一年使用:0次
7 . 下列说法正确的是
①标准状况下,6.02×1023个分子所占的体积约是22.4 L
②0.5 mol H2所占体积为11.2 L
③标准状况下,1 mol H2O的体积为22.4 L
④常温常压下,28 g CO与N2的混合气体所含的原子数为2NA
⑤各种气体的气体摩尔体积都约为22.4 L·mol−1
⑥标准状况下,体积相同的气体的分子数相同
①标准状况下,6.02×1023个分子所占的体积约是22.4 L
②0.5 mol H2所占体积为11.2 L
③标准状况下,1 mol H2O的体积为22.4 L
④常温常压下,28 g CO与N2的混合气体所含的原子数为2NA
⑤各种气体的气体摩尔体积都约为22.4 L·mol−1
⑥标准状况下,体积相同的气体的分子数相同
| A.①③⑤ | B.④⑥ | C.③④⑥ | D.①④⑥ |
您最近一年使用:0次
解题方法
8 . 将一小块钠放入下列溶液中,既能产生气体又能生成白色沉淀的是
| A.硝酸铜溶液 | B.稀硫酸 | C.氯化钠溶液 | D.氯化镁溶液 |
您最近一年使用:0次
名校
解题方法
9 . 下列关于物质性质的比较,正确的是
A.原子半径大小: | B.氢化物稳定性: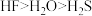 |
C.酸性强弱: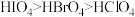 | D.碱性强弱: |
您最近一年使用:0次
2024-08-12更新
|
189次组卷
|
3卷引用:第四章 物质结构 元素周期律【单元测试B卷】
解题方法
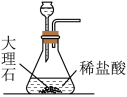
10 . 实验室模拟侯氏制碱法制备Na2CO3,下列装置与原理均正确的是
|
|
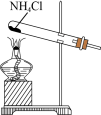
| A.制取CO2 | B.制取NH3 |
|
|
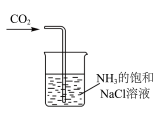
| C.制取NaHCO3 | D.制取Na2CO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次