1 . 乙烯的产量可以用来衡量一个国家的石油化工发展水平,A和B是生活中两种常见的有机物,C是一种具有香味的物质,且碳原子数是A的两倍。现以乙烯为主要原料合成C,其合成路线如图所示,请回答下列问题:
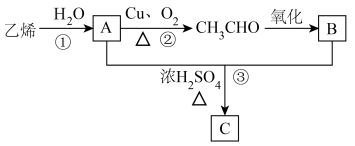
(1)乙烯的结构简式:______ 。
(2)A分子中含有的官能团名称为______ 。
(3)②的反应类型为______ ,③的反应类型为______ 。
(4)写出反应①的化学方程式_______ 。

(1)乙烯的结构简式:
(2)A分子中含有的官能团名称为
(3)②的反应类型为
(4)写出反应①的化学方程式
您最近一年使用:0次
2 . 我国科学家首次在实验室实现从CO2到淀粉的全合成。其部分合成路线如图所示:
CO2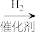 CH3OH
CH3OH HCHO
HCHO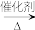 …→(C6H10O5)n
…→(C6H10O5)n
(1)CH3OH分子中与氧原子形成共价键的原子为_______ 。
(2)CH3CHO与HCHO互为同系物,具有相同的官能团是_______ (写名称)。
(3)CO2催化加H2制CH3OH,该反应一般由以下两步反应实现:
Ⅰ. CO2+H2⇌CO+H2O Ⅱ. ……
写出一定条件下反应Ⅱ的化学方程式:_______ 。
CO2
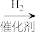 CH3OH
CH3OH HCHO
HCHO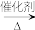 …→(C6H10O5)n
…→(C6H10O5)n(1)CH3OH分子中与氧原子形成共价键的原子为
(2)CH3CHO与HCHO互为同系物,具有相同的官能团是
(3)CO2催化加H2制CH3OH,该反应一般由以下两步反应实现:
Ⅰ. CO2+H2⇌CO+H2O Ⅱ. ……
写出一定条件下反应Ⅱ的化学方程式:
您最近一年使用:0次
3 . 氮、硫的化合物与人类生活和生产有着密切的联系。
Ⅰ.氨既是一种重要的化工产品,又是一种重要的化工原料。图1为合成氨以及氨氧化制硝酸的流程示意图。

(1)合成塔中发生反应的化学方程式为_____ 氧化炉中发生反应的化学方程式为_____ 。
(2)A为_____ ;向吸收塔中通入A的作用_____ 。
(3)工业生产中为了盛装大量浓硝酸,可选择_____ (填字母)作为罐体材料。
a.铜 b.铂 c.铝 d.镁
Ⅱ.浓硫酸与木炭在加热条件下可发生化学反应,为检验反应的产物,某同学设计了如图2所示的实验。请据此回答下列问题:
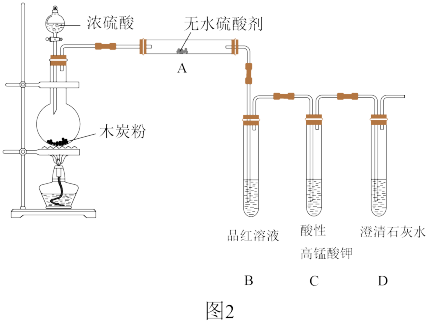
(4)浓硫酸与木炭反应的化学方程式:_____ 。
(5)装置B中的现象_____ ;证明产物中有_____ 。
(6)装置C的作用是_____ 。
Ⅰ.氨既是一种重要的化工产品,又是一种重要的化工原料。图1为合成氨以及氨氧化制硝酸的流程示意图。

(1)合成塔中发生反应的化学方程式为
(2)A为
(3)工业生产中为了盛装大量浓硝酸,可选择
a.铜 b.铂 c.铝 d.镁
Ⅱ.浓硫酸与木炭在加热条件下可发生化学反应,为检验反应的产物,某同学设计了如图2所示的实验。请据此回答下列问题:

(4)浓硫酸与木炭反应的化学方程式:
(5)装置B中的现象
(6)装置C的作用是
您最近一年使用:0次
4 . 化学与人类的“衣、食、住、行、医”关系密切,回答下列问题:
(1)衣:市场上的衣物琳琅满目,它们的主要成分有合成纤维,有天然的棉、麻、毛、丝,区分羊毛线和棉纱线的方法是_____ 。
(2)食:粮食可以酿成美酒,俗话说:“酒是陈的香”,写出生成香味物质的化学方程式:______ 。
(3)住:居民小区楼房的铝合金门窗主要原料为金属铝,写出铝与稀硫酸反应的离子方程式_____ 。
(4)行:汽车的出现极大方便了我们的出行,汽油是石油通过炼制得到,区分直馏汽油和裂化汽油的方法是______ 。
(5)医:苯是合成医药的重要原料,苯与液溴反应的化学方程式为______ 。
(1)衣:市场上的衣物琳琅满目,它们的主要成分有合成纤维,有天然的棉、麻、毛、丝,区分羊毛线和棉纱线的方法是
(2)食:粮食可以酿成美酒,俗话说:“酒是陈的香”,写出生成香味物质的化学方程式:
(3)住:居民小区楼房的铝合金门窗主要原料为金属铝,写出铝与稀硫酸反应的离子方程式
(4)行:汽车的出现极大方便了我们的出行,汽油是石油通过炼制得到,区分直馏汽油和裂化汽油的方法是
(5)医:苯是合成医药的重要原料,苯与液溴反应的化学方程式为
您最近一年使用:0次
5 . 申泮文院士(1916-2017),广东籍化学家、教育家,长期致力于无机化学教学研究为我国无机化学教学和教材建设做出了卓越贡献。他在化学教育研究领域创下多项第一;编写出新中国第一部大学化学教材、第一个引入美国科技出版物、第一个在化学教学应用计算机技术、主持完成我国第一部多媒体教科书等。他常在课堂教学中,号召学生牢记历史,报效祖国。2005年,申先生入选“中国10位最令人感动的教师”,也是我国执教时间最长的化学教师。2011年,95岁高龄的申先生还坚持骑着行车去给本科生讲课。
申先生是我国在离子型金属氢化物、储氢合金材料和镍/金属氢化物可逆电池等研究领域的先驱者。1959年10月,他和龚毅生等在《化学通报》发表“氢化铝锂的合成”,这是我国在氢化物研究领域发表的第一篇论文。
(1)完成以氢化锂(LiH)和氯化铝为原料合成氢化铝锂(LiAlH4)的反应方程式:
4LiH+______ =LiAlH4+3______
(2)根据以上材料谈一谈你的认识和启示______ 、______ 、______ (写三点)。
申先生是我国在离子型金属氢化物、储氢合金材料和镍/金属氢化物可逆电池等研究领域的先驱者。1959年10月,他和龚毅生等在《化学通报》发表“氢化铝锂的合成”,这是我国在氢化物研究领域发表的第一篇论文。
(1)完成以氢化锂(LiH)和氯化铝为原料合成氢化铝锂(LiAlH4)的反应方程式:
4LiH+
(2)根据以上材料谈一谈你的认识和启示
您最近一年使用:0次
名校
6 . 碘及其化合物主要用于医药、照相及染料等。碘是合成碘化物的基本原料。空气吹出法从卤水中提碘的流程如下:
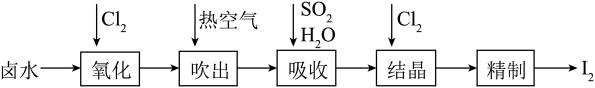
回答下列问题:
(1)“氧化”时,Cl2过量会将I2氧化为HIO3,写出生成HIO3的化学方程式_________ ;
(2)“吹出”在吹出塔中进行,含碘卤水从_________ (填“塔顶”或“塔底”,下同)进入,热空气从_________ 进入,理由为_________ ;
(3)吸收塔应选择耐酸材料,原因是_________ ;
(4)结晶时,发生反应的离子方程式为_________ ;
(5)从“氧化”所得含碘卤水中提取碘还可以采用加CCl4的方法,该分离方法为_________ ;为进一步分离I2和CCl4,向其中加入NaOH溶液与I2反应,生成的I-、 进入水溶液;分液后再酸化,即得粗碘.加入NaOH后溶液中I-、
进入水溶液;分液后再酸化,即得粗碘.加入NaOH后溶液中I-、 的物质的量之比为
的物质的量之比为_________ ;
(6)H2O2也能发生与Cl2类似的反应,若先用H2O2将卤水中的I-氧化为 ,再将其与卤水按一定比例混合、酸化制取粗碘,处理含I-为254mg/L的卤水1m3,理论上需20%的H2O2
,再将其与卤水按一定比例混合、酸化制取粗碘,处理含I-为254mg/L的卤水1m3,理论上需20%的H2O2_________ g。

回答下列问题:
(1)“氧化”时,Cl2过量会将I2氧化为HIO3,写出生成HIO3的化学方程式
(2)“吹出”在吹出塔中进行,含碘卤水从
(3)吸收塔应选择耐酸材料,原因是
(4)结晶时,发生反应的离子方程式为
(5)从“氧化”所得含碘卤水中提取碘还可以采用加CCl4的方法,该分离方法为
 进入水溶液;分液后再酸化,即得粗碘.加入NaOH后溶液中I-、
进入水溶液;分液后再酸化,即得粗碘.加入NaOH后溶液中I-、 的物质的量之比为
的物质的量之比为(6)H2O2也能发生与Cl2类似的反应,若先用H2O2将卤水中的I-氧化为
 ,再将其与卤水按一定比例混合、酸化制取粗碘,处理含I-为254mg/L的卤水1m3,理论上需20%的H2O2
,再将其与卤水按一定比例混合、酸化制取粗碘,处理含I-为254mg/L的卤水1m3,理论上需20%的H2O2
您最近一年使用:0次
2016-12-09更新
|
367次组卷
|
3卷引用:2018届高三一轮复习化学:考点27-溴、碘及其化合物性质



