解题方法
1 . 某实验小组以含铁污泥(主要成分为Fe2O3、FeO、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾(FeSO4•7H2O)和柠檬酸铁铵。
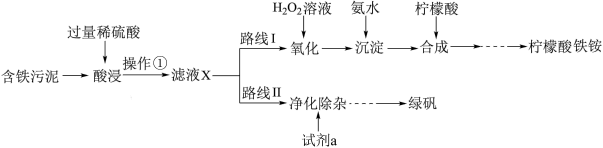
根据所学知识,回答下列问题:
(1)操作①的名称是_______ ,路线I中,加入H2O2溶液的目的是_______ 。
(2)写出“酸浸”时,Fe2O3与硫酸反应的化学方程式:_______ ;检验含有Fe3+的试剂是_______ 。
(3)实验室中配制FeSO4溶液时通常需加入少量的试剂a,目的是_______ 。
(4)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:_______ 。
(5)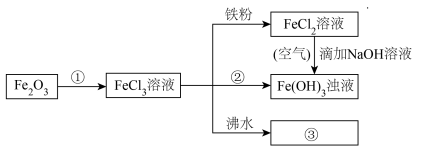
FeCl2溶液→Fe(OH)3浊液的过程中,观察到的实验现象是_______ 。

根据所学知识,回答下列问题:
(1)操作①的名称是
(2)写出“酸浸”时,Fe2O3与硫酸反应的化学方程式:
(3)实验室中配制FeSO4溶液时通常需加入少量的试剂a,目的是
(4)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
(5)

FeCl2溶液→Fe(OH)3浊液的过程中,观察到的实验现象是
您最近一年使用:0次
名校
解题方法
2 . 铁及其化合物在日常生活、生产中应用广泛。
(1)高铁酸钠 是水处理过程中的一种新型净水剂,工业上利用
是水处理过程中的一种新型净水剂,工业上利用 和
和 的混合溶液将
的混合溶液将 氧化性制备高铁酸钠,反应的化学方程式为
氧化性制备高铁酸钠,反应的化学方程式为______ ;高铁酸钠能用作新型净水剂的原理是______ 。
(2)某实验小组模拟工业制法,以含铁污泥(主要成分为 、
、 、
、 及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾
及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾 和柠檬酸铁铵。
和柠檬酸铁铵。
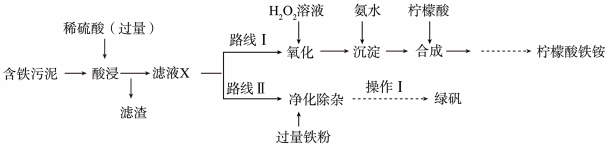
根据所学知识,回答下列问题:
①“滤液X”中一定含有的阳离子为______ 。
②路线I中,加入 溶液的离子方程式
溶液的离子方程式______ 。
③“操作I”为过滤、______ 、______ 、过滤、洗涤、低温烘干。
④实验室用绿矾配置硫酸亚铁溶液时,往往会加入适量的稀硫酸,请你解释其中原因______ (结合必要的方程式)。
(1)高铁酸钠
 是水处理过程中的一种新型净水剂,工业上利用
是水处理过程中的一种新型净水剂,工业上利用 和
和 的混合溶液将
的混合溶液将 氧化性制备高铁酸钠,反应的化学方程式为
氧化性制备高铁酸钠,反应的化学方程式为(2)某实验小组模拟工业制法,以含铁污泥(主要成分为
 、
、 、
、 及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾
及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾 和柠檬酸铁铵。
和柠檬酸铁铵。
根据所学知识,回答下列问题:
①“滤液X”中一定含有的阳离子为
②路线I中,加入
 溶液的离子方程式
溶液的离子方程式③“操作I”为过滤、
④实验室用绿矾配置硫酸亚铁溶液时,往往会加入适量的稀硫酸,请你解释其中原因
您最近一年使用:0次
3 . 化合物M是一种新型发光材料中间体。实验室由烃A制备M的一种合成路线如下:
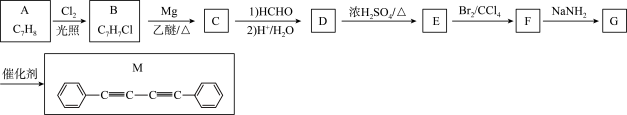
已知:①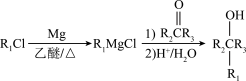
②2RC≡CH RC≡C-C≡CR(R、R1、R2、R3表示氢原子或烃基)
RC≡C-C≡CR(R、R1、R2、R3表示氢原子或烃基)
回答下列问题:
(1)由A生成B的反应类型为___________ 。
(2)C的结构简式为___________ 。D中官能团的电子式为___________
(3)E的化学名称为___________ ;由E制得高聚物的平均相对分子质量为10400,则所得高聚物的平均聚合度为___________ 。
(4)由G生成M的化学方程式为___________ 。
(5)参照上述合成路线和信息,以1,2-二氯乙烷为原料(其他无机试剂任选),设计制备丁烷的合成路线___________ 。

已知:①

②2RC≡CH
 RC≡C-C≡CR(R、R1、R2、R3表示氢原子或烃基)
RC≡C-C≡CR(R、R1、R2、R3表示氢原子或烃基)回答下列问题:
(1)由A生成B的反应类型为
(2)C的结构简式为
(3)E的化学名称为
(4)由G生成M的化学方程式为
(5)参照上述合成路线和信息,以1,2-二氯乙烷为原料(其他无机试剂任选),设计制备丁烷的合成路线
您最近一年使用:0次
解题方法
4 . 某实验小组以含铁污泥(主要成分为 、FeO、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾(
、FeO、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾( )和柠檬酸铁铵。
)和柠檬酸铁铵。
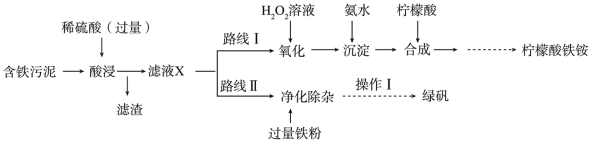
根据所学知识,回答下列问题:
(1)写出“酸浸”时, 与硫酸反应的离子方程式:
与硫酸反应的离子方程式:_______ 。
(2)“滤液X”中一定含有的阳离子为_______ 。
(3)路线Ⅰ中,加入 溶液的目的是
溶液的目的是_______ 。
(4)写出加入过量铁粉时发生反应的离子方程式:_______ 。
(5)“操作Ⅰ”为过滤、_______ 、_______ 、过滤、洗涤、低温烘干。
(6)“酸浸”时加入400mL1.5 硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为_______ g。
 、FeO、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾(
、FeO、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾( )和柠檬酸铁铵。
)和柠檬酸铁铵。
根据所学知识,回答下列问题:
(1)写出“酸浸”时,
 与硫酸反应的离子方程式:
与硫酸反应的离子方程式:(2)“滤液X”中一定含有的阳离子为
(3)路线Ⅰ中,加入
 溶液的目的是
溶液的目的是(4)写出加入过量铁粉时发生反应的离子方程式:
(5)“操作Ⅰ”为过滤、
(6)“酸浸”时加入400mL1.5
 硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
硫酸(硫酸过量),若仅按照路线Ⅱ发生反应,则理论上制得的绿矾的质量为
您最近一年使用:0次
名校
5 . 化合物I是合成米非司酮的一种中间体,其合成路线如下:

已知:①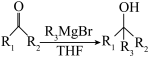 (R1、R2为烃基或H,R3为烃基)
(R1、R2为烃基或H,R3为烃基)
②C、D、F均为含有-CN(氰基)的腈类化合物,如CH2CN可称为乙腈。
回答下列问题:
(1)A的化学名称为_________ 。
(2)由A生成C的反应类型是______ 。
(3)由D和E生成F的化学方程式为_______ 。
(4)H的结构简式为________ 。
(5)I中所含官能团的名称为_______ 。
(6)G的芳香同分异构体中,含有酯基且能发生银镜反应,核磁共振氢谱有4组峰,且峰面积之比为9:2:2:1的有_______ 种。
(7)设计以CH2=CHCH2Cl和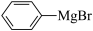 为原料制备
为原料制备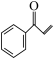 的合成路线
的合成路线________ (无机试剂及有机溶剂任用)。

已知:①
 (R1、R2为烃基或H,R3为烃基)
(R1、R2为烃基或H,R3为烃基)②C、D、F均为含有-CN(氰基)的腈类化合物,如CH2CN可称为乙腈。
回答下列问题:
(1)A的化学名称为
(2)由A生成C的反应类型是
(3)由D和E生成F的化学方程式为
(4)H的结构简式为
(5)I中所含官能团的名称为
(6)G的芳香同分异构体中,含有酯基且能发生银镜反应,核磁共振氢谱有4组峰,且峰面积之比为9:2:2:1的有
(7)设计以CH2=CHCH2Cl和
 为原料制备
为原料制备 的合成路线
的合成路线
您最近一年使用:0次
2020-09-09更新
|
182次组卷
|
2卷引用:湖南省百校联考2021届高三8月联考化学试题
名校
6 .  、
、 和含氮化合物的资源化利用,既能解决环保问题,又能提供化工原料,缓解能源紧张,具有重要的现实意义和广阔的应用前景。
和含氮化合物的资源化利用,既能解决环保问题,又能提供化工原料,缓解能源紧张,具有重要的现实意义和广阔的应用前景。
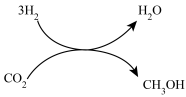
(1)利用 可合成多种化工产品。
可合成多种化工产品。
2021年9月24日我国科学家首次报告了 到淀粉的人工合成路线,其中第一步转化如图所示,该反应的化学方程式为
到淀粉的人工合成路线,其中第一步转化如图所示,该反应的化学方程式为___________ 。
(2)氨氮废水是造成河流及湖泊富营养化的主要因素。
①某氮肥厂产生的氨氮废水中的氮元素多以 和
和 的形式存在,我们可以通过一些化学方法把
的形式存在,我们可以通过一些化学方法把 和
和 转化为
转化为 。
。 在催化剂的作用会和氧气发生反应,该反应的化学方程式为
在催化剂的作用会和氧气发生反应,该反应的化学方程式为___________ 。
②某团队设计处理氨氮废水的流程如下:

过程Ⅰ为硝化过程,在微生物的作用下实现 的转化,在碱性条件下,
的转化,在碱性条件下, 被氧气氧化成
被氧气氧化成 的总反应离子方程式为
的总反应离子方程式为___________ 。过程Ⅲ为反硝化过程,向一定条件下的废水中加入甲醇( )实现
)实现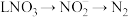 的转化,将
的转化,将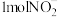 完全转化为
完全转化为 转移电子的物质的量为
转移电子的物质的量为___________ 。
(3)硫酸生产及煤燃烧过程中产生的废气 等会对大气造成污染,可用氨水吸收
等会对大气造成污染,可用氨水吸收 或采用钙基固硫法。
或采用钙基固硫法。 属于
属于___________ (填“电解质”或“非电解质”),氨水吸收少量 ,反应的离子方程式为
,反应的离子方程式为___________ 。
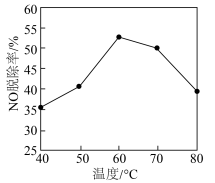
(4)氮的氧化物(NO、 等)是主要的大气污染物,必须脱除才能排放。研究不同温度下经酸化处理的
等)是主要的大气污染物,必须脱除才能排放。研究不同温度下经酸化处理的 溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是
溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是___________ 。
 、
、 和含氮化合物的资源化利用,既能解决环保问题,又能提供化工原料,缓解能源紧张,具有重要的现实意义和广阔的应用前景。
和含氮化合物的资源化利用,既能解决环保问题,又能提供化工原料,缓解能源紧张,具有重要的现实意义和广阔的应用前景。
(1)利用
 可合成多种化工产品。
可合成多种化工产品。2021年9月24日我国科学家首次报告了
 到淀粉的人工合成路线,其中第一步转化如图所示,该反应的化学方程式为
到淀粉的人工合成路线,其中第一步转化如图所示,该反应的化学方程式为(2)氨氮废水是造成河流及湖泊富营养化的主要因素。
①某氮肥厂产生的氨氮废水中的氮元素多以
 和
和 的形式存在,我们可以通过一些化学方法把
的形式存在,我们可以通过一些化学方法把 和
和 转化为
转化为 。
。 在催化剂的作用会和氧气发生反应,该反应的化学方程式为
在催化剂的作用会和氧气发生反应,该反应的化学方程式为②某团队设计处理氨氮废水的流程如下:

过程Ⅰ为硝化过程,在微生物的作用下实现
 的转化,在碱性条件下,
的转化,在碱性条件下, 被氧气氧化成
被氧气氧化成 的总反应离子方程式为
的总反应离子方程式为 )实现
)实现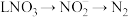 的转化,将
的转化,将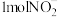 完全转化为
完全转化为 转移电子的物质的量为
转移电子的物质的量为(3)硫酸生产及煤燃烧过程中产生的废气
 等会对大气造成污染,可用氨水吸收
等会对大气造成污染,可用氨水吸收 或采用钙基固硫法。
或采用钙基固硫法。 属于
属于 ,反应的离子方程式为
,反应的离子方程式为(4)氮的氧化物(NO、
 等)是主要的大气污染物,必须脱除才能排放。研究不同温度下经酸化处理的
等)是主要的大气污染物,必须脱除才能排放。研究不同温度下经酸化处理的 溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是
溶液对NO脱除率的影响,结果如图所示。在60~80℃时,NO脱除率下降的原因是
您最近一年使用:0次
解题方法
7 . 一水硫酸四氨合铜(Ⅱ)的化学式为 是一种重要的染料及农药中间体。某学习小组以废铜料(含少量铁及难溶性杂质)为主要原料合成该物质,合成路线如下:
是一种重要的染料及农药中间体。某学习小组以废铜料(含少量铁及难溶性杂质)为主要原料合成该物质,合成路线如下:不正确 的是
 是一种重要的染料及农药中间体。某学习小组以废铜料(含少量铁及难溶性杂质)为主要原料合成该物质,合成路线如下:
是一种重要的染料及农药中间体。某学习小组以废铜料(含少量铁及难溶性杂质)为主要原料合成该物质,合成路线如下:
A.操作I中发生的主要反应为: |
| B.操作II中趁热过滤除去的是难溶性杂质和氢氧化铁 |
| C.操作III中洗涤可用乙醇和水的混合液,干燥可采用减压干燥方式 |
| D.设计操作IV的目的是为了提高乙醇的利用率 |
您最近一年使用:0次
名校
解题方法
8 . 硒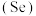 是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光
是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光 效应以来,
效应以来, 在发光材料、生物医学等领域引起广泛关注。一种含
在发光材料、生物医学等领域引起广泛关注。一种含 的新型
的新型 分子IV的合成路线如下:
分子IV的合成路线如下: 与S同族,
与S同族, 在元素周期表中的位置为
在元素周期表中的位置为_______ 。
(2) 是一种有恶臭的气体,常作半导体用料。与
是一种有恶臭的气体,常作半导体用料。与 相比,沸点
相比,沸点
_______  (填“>”或“<”,下同),原因是
(填“>”或“<”,下同),原因是_______ ;热稳定性:
_______  。
。
(3)研究发现,给小鼠喂食适量硒酸钠 可减轻重金属铊引起的中毒。
可减轻重金属铊引起的中毒。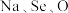 形成的简单离子的半径由大到小的顺序为
形成的简单离子的半径由大到小的顺序为_______ 。
(4)反应物III的部分结构与肼 十分相似,
十分相似, 的电子式为
的电子式为_______ 。以 为原料合成的液体火箭燃料偏二甲肼
为原料合成的液体火箭燃料偏二甲肼 与液态氧化剂
与液态氧化剂 接触时立刻反应,产生大量无害气体,放出巨大能量,把火箭送上天空,偏二甲肼与
接触时立刻反应,产生大量无害气体,放出巨大能量,把火箭送上天空,偏二甲肼与 反应的化学方程式为
反应的化学方程式为_______ 。
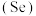 是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光
是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光 效应以来,
效应以来, 在发光材料、生物医学等领域引起广泛关注。一种含
在发光材料、生物医学等领域引起广泛关注。一种含 的新型
的新型 分子IV的合成路线如下:
分子IV的合成路线如下: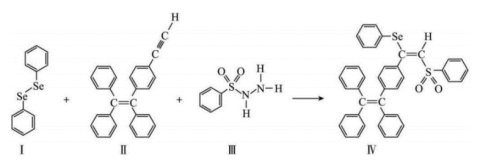
 与S同族,
与S同族, 在元素周期表中的位置为
在元素周期表中的位置为(2)
 是一种有恶臭的气体,常作半导体用料。与
是一种有恶臭的气体,常作半导体用料。与 相比,沸点
相比,沸点
 (填“>”或“<”,下同),原因是
(填“>”或“<”,下同),原因是
 。
。(3)研究发现,给小鼠喂食适量硒酸钠
 可减轻重金属铊引起的中毒。
可减轻重金属铊引起的中毒。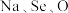 形成的简单离子的半径由大到小的顺序为
形成的简单离子的半径由大到小的顺序为(4)反应物III的部分结构与肼
 十分相似,
十分相似, 的电子式为
的电子式为 为原料合成的液体火箭燃料偏二甲肼
为原料合成的液体火箭燃料偏二甲肼 与液态氧化剂
与液态氧化剂 接触时立刻反应,产生大量无害气体,放出巨大能量,把火箭送上天空,偏二甲肼与
接触时立刻反应,产生大量无害气体,放出巨大能量,把火箭送上天空,偏二甲肼与 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
2023-03-24更新
|
267次组卷
|
2卷引用:湖北省名校3月联考2022-2023学年高一下学期化学试题
名校
解题方法
9 . 将CO或 转化为高附加值化学品是颇具前景的合成路线。
转化为高附加值化学品是颇具前景的合成路线。
(1)相比于煤和石油,天然气作为燃料的主要优点有_______ 。
(2)煤的气化可将煤转化为可燃性气体,写出生成水煤气的化学方程式_______ 。
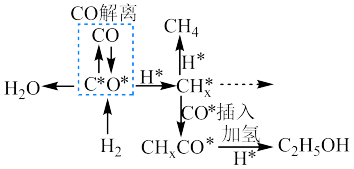
(3)钴系催化剂催化下CO加氢反应的一种路径如下图所示(*表示微粒吸附在催化剂表面的形态): 和
和 反应生成
反应生成 反应的重要中间体有
反应的重要中间体有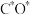 、
、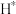 、
、_______ 、 和
和_______ 。
(4) 与二甲醚可发生反应:
与二甲醚可发生反应:
 。反应中二甲醚的平衡转化率与温度和压强的关系见下图:
。反应中二甲醚的平衡转化率与温度和压强的关系见下图:
_______ 0(填“大于”“小于”或“等于”)0,a、b、c的大小关系为_______ 。
②TK下,向恒压密闭容器中充入CO和 ,反应前
,反应前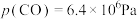 ,
,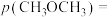
 ;充分反应达到平衡后CO的转化率为25%,则TK下该反应的平衡常数
;充分反应达到平衡后CO的转化率为25%,则TK下该反应的平衡常数
_______ 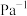 。
。
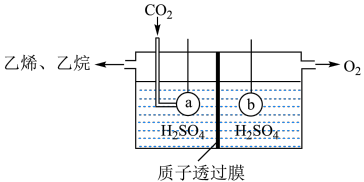
(5)以 为原料,电解法制取乙烯、乙烷的装置如图,生成乙烷的电极反应式为:
为原料,电解法制取乙烯、乙烷的装置如图,生成乙烷的电极反应式为:_______ ,当左侧有8.96L(标准状况) 反应时,a极区产品中乙烯的体积分数为50%,此时左右两侧溶液质量变化差
反应时,a极区产品中乙烯的体积分数为50%,此时左右两侧溶液质量变化差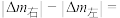
_______ g。
 转化为高附加值化学品是颇具前景的合成路线。
转化为高附加值化学品是颇具前景的合成路线。(1)相比于煤和石油,天然气作为燃料的主要优点有
(2)煤的气化可将煤转化为可燃性气体,写出生成水煤气的化学方程式
(3)钴系催化剂催化下CO加氢反应的一种路径如下图所示(*表示微粒吸附在催化剂表面的形态):
 和
和 反应生成
反应生成 反应的重要中间体有
反应的重要中间体有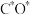 、
、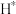 、
、 和
和(4)
 与二甲醚可发生反应:
与二甲醚可发生反应:
 。反应中二甲醚的平衡转化率与温度和压强的关系见下图:
。反应中二甲醚的平衡转化率与温度和压强的关系见下图:

②TK下,向恒压密闭容器中充入CO和
 ,反应前
,反应前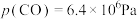 ,
,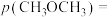
 ;充分反应达到平衡后CO的转化率为25%,则TK下该反应的平衡常数
;充分反应达到平衡后CO的转化率为25%,则TK下该反应的平衡常数
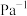 。
。(5)以
 为原料,电解法制取乙烯、乙烷的装置如图,生成乙烷的电极反应式为:
为原料,电解法制取乙烯、乙烷的装置如图,生成乙烷的电极反应式为: 反应时,a极区产品中乙烯的体积分数为50%,此时左右两侧溶液质量变化差
反应时,a极区产品中乙烯的体积分数为50%,此时左右两侧溶液质量变化差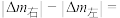
您最近一年使用:0次
解题方法
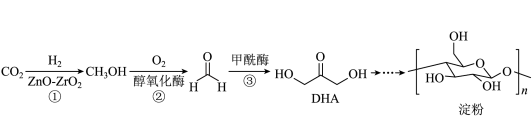
10 . 中国科学院天津工业生物技术研究所科研团队在实验室里首次实现了以 为原料人工合成淀粉,其合成路线如图所示。设
为原料人工合成淀粉,其合成路线如图所示。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为原料人工合成淀粉,其合成路线如图所示。设
为原料人工合成淀粉,其合成路线如图所示。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
| A.DHA可以被氧化成含醛基的物质 |
B.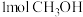 分子中含 分子中含 的数目为 的数目为 |
| C.30g HCHO和30g DHA中含有的H原子数目不同 |
| D.淀粉与纤维素互为同分异构体 |
您最近一年使用:0次



