1 . 氢化铝钠 是有机合成中的重要还原剂,其合成路线如图所示。
是有机合成中的重要还原剂,其合成路线如图所示。

某实验小组利用如图所示的装置制备无水 。
。

(1)装置F的作用是_____________________________ 。
(2) 与NaH反应时,需将
与NaH反应时,需将 溶于有机溶剂,再将得到的溶液滴加到NaH粉末上,此反应中NaH的转化率较低的原因可能是
溶于有机溶剂,再将得到的溶液滴加到NaH粉末上,此反应中NaH的转化率较低的原因可能是 _____________________________
(3)利用氢化铝钠遇水反应生成的氢气的体积测定氢化铝钠样品的纯度。
①其反应的化学方程式为_____________________________
②设计如图四种装置测定氢化铝钠样品的纯度(假设杂质不参与反应)。

从简约性、准确性角度考虑,最适宜的装置是___________ 。
 是有机合成中的重要还原剂,其合成路线如图所示。
是有机合成中的重要还原剂,其合成路线如图所示。
某实验小组利用如图所示的装置制备无水
 。
。
(1)装置F的作用是
(2)
 与NaH反应时,需将
与NaH反应时,需将 溶于有机溶剂,再将得到的溶液滴加到NaH粉末上,此反应中NaH的转化率较低的原因可能是
溶于有机溶剂,再将得到的溶液滴加到NaH粉末上,此反应中NaH的转化率较低的原因可能是 (3)利用氢化铝钠遇水反应生成的氢气的体积测定氢化铝钠样品的纯度。
①其反应的化学方程式为
②设计如图四种装置测定氢化铝钠样品的纯度(假设杂质不参与反应)。

从简约性、准确性角度考虑,最适宜的装置是
您最近一年使用:0次
2 . 聚四氟乙烯的耐热性和化学稳定性都超过了其他塑料,号称“塑料王”,在工业上有广泛的用途。其合成路线如下所示:
A[氯仿(CHCl3)] B(二氟一氯甲烷)
B(二氟一氯甲烷) C(四氟乙烯)
C(四氟乙烯) D(聚四氟乙烯)
D(聚四氟乙烯)
(1)写出B、C的结构式:B___________ 、C___________ 。
(2)A→B的化学方程式为___________ ,反应类型为___________ 。
(3)C→D的化学方程式为___________ 。
A[氯仿(CHCl3)]
 B(二氟一氯甲烷)
B(二氟一氯甲烷) C(四氟乙烯)
C(四氟乙烯) D(聚四氟乙烯)
D(聚四氟乙烯)(1)写出B、C的结构式:B
(2)A→B的化学方程式为
(3)C→D的化学方程式为
您最近一年使用:0次
3 . 近年来,乳酸成为研究热点之一、乳酸可以用化学方法合成,也可以由淀粉通过发酵法制备。以乳酸(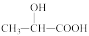 )为原料制成的高分子材料具有生物相容性,而且在哺乳动物体内或自然环境中都可以最终降解为二氧化碳和水。乳酸还有许多其他用途,如它能与铁粉反应制备一种药物,反应的化学方程式为:2
)为原料制成的高分子材料具有生物相容性,而且在哺乳动物体内或自然环境中都可以最终降解为二氧化碳和水。乳酸还有许多其他用途,如它能与铁粉反应制备一种药物,反应的化学方程式为:2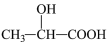 +Fe
+Fe
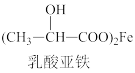 +X。
+X。
(1)乳酸降解为二氧化碳的反应的化学方程式为_______ 。
(2)乳酸与铁的反应中,X的化学式为_______ ,该反应中乳酸表现出酸性和_______ 性。
(3)试从自然界物质循环的角度解释利用乳酸合成高分子材料对环境的重要意义_______ 。
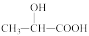 )为原料制成的高分子材料具有生物相容性,而且在哺乳动物体内或自然环境中都可以最终降解为二氧化碳和水。乳酸还有许多其他用途,如它能与铁粉反应制备一种药物,反应的化学方程式为:2
)为原料制成的高分子材料具有生物相容性,而且在哺乳动物体内或自然环境中都可以最终降解为二氧化碳和水。乳酸还有许多其他用途,如它能与铁粉反应制备一种药物,反应的化学方程式为:2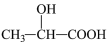 +Fe
+Fe
 +X。
+X。(1)乳酸降解为二氧化碳的反应的化学方程式为
(2)乳酸与铁的反应中,X的化学式为
(3)试从自然界物质循环的角度解释利用乳酸合成高分子材料对环境的重要意义
您最近一年使用:0次
2022-11-26更新
|
152次组卷
|
2卷引用:2019版鲁科化学必修第二册第3章本章自我评价课后习题
解题方法
4 . 人类可以主动参与氮循环,合成氨工业就是参与的手段之一。以天然气为原料合成氨是新的生产氮肥的方法,它具有污染小、成本低等诸多优点,其过程大体如图所示:
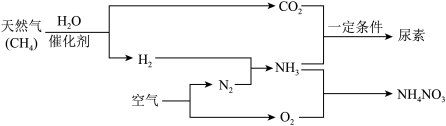
(1)写出用天然气制备氢气的化学方程式:____ 。
(2)写出合成尿素反应的化学方程式:_____ 。
(3)写出O2与NH3反应生成NH4NO3和H2O的化学方程式:____ 。
(4)每生产1molNH4NO3最少需要NH3_____ mol,而要生产这些NH3又最少需要CH4____ mol。

(1)写出用天然气制备氢气的化学方程式:
(2)写出合成尿素反应的化学方程式:
(3)写出O2与NH3反应生成NH4NO3和H2O的化学方程式:
(4)每生产1molNH4NO3最少需要NH3
您最近一年使用:0次
2022-11-24更新
|
261次组卷
|
3卷引用:苏教2020版化学必修第二册专题7第一单元 氮的固定课后习题
苏教2020版化学必修第二册专题7第一单元 氮的固定课后习题7.1.3人工固氮(课后)-2019苏教版必修2课前课中课后(已下线)第07讲 氮的固定-【寒假自学课】2022年高一化学寒假精品课(苏教版必修第二册)
名校
5 . 氯气是一种重要的化工原料,氯气及其化合物在自来水的消毒,农药的生产、药物的合成等领域都有着重要的应用。
Ⅰ.(1)NaClO中Cl的化合价为____ ,NaClO具有较强的_____ (填“氧化”或“还原”)性,是常用的消毒剂和漂白剂的有效成分。
(2)黄色气体 可用于污水杀菌和饮用水净化。
可用于污水杀菌和饮用水净化。
① 与
与 在强酸性溶液中反应可制得
在强酸性溶液中反应可制得 、
、 被氧化为
被氧化为 ,该反应的离子方程式为
,该反应的离子方程式为________________ 。
② 可将废水中的
可将废水中的 氧化为
氧化为 而除去,本身被还原为
而除去,本身被还原为 ,该反应过程中氧化剂与还原剂的物质的量之比为
,该反应过程中氧化剂与还原剂的物质的量之比为_______ 。
Ⅱ.某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(该反应为放热反应),回答下列问题:

(1)在A装置中用固体二氧化锰与浓盐酸在加热条件下反应制取氯气,写出该反应的化学方程式______________ 。
(2)C装置的作用是______________ 。
(3)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成 ,为避免此副反应的发生,可采取的措施是
,为避免此副反应的发生,可采取的措施是______________ 。
②另一个副反应 ,为避免此副反应的发生,装置的改进措施为
,为避免此副反应的发生,装置的改进措施为________________ 。
Ⅰ.(1)NaClO中Cl的化合价为
(2)黄色气体
 可用于污水杀菌和饮用水净化。
可用于污水杀菌和饮用水净化。①
 与
与 在强酸性溶液中反应可制得
在强酸性溶液中反应可制得 、
、 被氧化为
被氧化为 ,该反应的离子方程式为
,该反应的离子方程式为②
 可将废水中的
可将废水中的 氧化为
氧化为 而除去,本身被还原为
而除去,本身被还原为 ,该反应过程中氧化剂与还原剂的物质的量之比为
,该反应过程中氧化剂与还原剂的物质的量之比为Ⅱ.某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(该反应为放热反应),回答下列问题:

(1)在A装置中用固体二氧化锰与浓盐酸在加热条件下反应制取氯气,写出该反应的化学方程式
(2)C装置的作用是
(3)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成
 ,为避免此副反应的发生,可采取的措施是
,为避免此副反应的发生,可采取的措施是②另一个副反应
 ,为避免此副反应的发生,装置的改进措施为
,为避免此副反应的发生,装置的改进措施为
您最近一年使用:0次
2020-10-07更新
|
425次组卷
|
3卷引用:人教版(2019)高一必修第一册第二章 海水中的重要元素 素养拓展区



