21-22高一下·全国·单元测试
解题方法
1 . 氨气( )
)
(1)分子结构:由极性键形成的_______ 形的极性分子,N原子有一孤对电子;N为_______ 价,为N元素的最低价态;
(2)物理性质:_______ 气味的气体,密度比空气_______ ,_______ 溶于水,常温常压下1体积水能溶解_______ 体积的氨气,易_______ ;
(3)化学性质:
①与 反应:
反应:_______ ,溶液呈弱碱性,氨水的成分为:_______ ;氨水易_______ ;
②与酸反应:硫酸_______ ,盐酸_______ (有白烟生成);
③还原性(催化氧化):_______ (N为 价,最低价态,具有还原性);
价,最低价态,具有还原性);
(4)实验室制法_______ ;工业上采取 与
与 在高温高压催化剂条件下合成氨气;
在高温高压催化剂条件下合成氨气;
(5)用途:化工原料,制硝酸、氮肥等,做_______ 剂。
 )
)(1)分子结构:由极性键形成的
(2)物理性质:
(3)化学性质:
①与
 反应:
反应:②与酸反应:硫酸
③还原性(催化氧化):
 价,最低价态,具有还原性);
价,最低价态,具有还原性);(4)实验室制法
 与
与 在高温高压催化剂条件下合成氨气;
在高温高压催化剂条件下合成氨气;(5)用途:化工原料,制硝酸、氮肥等,做
您最近一年使用:0次
21-22高一下·全国·单元测试
解题方法
2 . 硝酸( )
)
(1)物理性质:无色、_______ 气味、_______ 挥发液体,能与水以任意比例互溶,常用浓硝酸的质量分数大约为69%。
(2)化学性质
硝酸为_______ 酸,具有以下性质:
①具有酸的通性;
②不稳定性:_______ ;
③强氧化性:无论浓、稀硝酸均具有强氧化性,与金属反应时不放出_______ 。
A.与金属反应:
铜与浓硝酸:_______ ;
铜与稀硝酸:_______ ;
银与浓硝酸:_______ ;
常温下浓硝酸与铁、铝发生_______ 。
B.与非金属反应:
碳与浓硝酸:_______ 。
C.与其他还原剂反应,如H2S、SO2、Fe2+等。
D.与有机物反应:硝化反应、酯化反应、与蛋白质发生颜色反应等。
(3)制法
①实验室制法:硝酸盐与浓硫酸微热,_______ (不能用强热和稀硫酸);
②工业制法:
氨的催化氧化法:_______ ;_______ ;_______ ;
尾气处理:_______ (用NaOH溶液吸收尾气)。
(4)用途:_______ 等。
 )
)(1)物理性质:无色、
(2)化学性质
硝酸为
①具有酸的通性;
②不稳定性:
③强氧化性:无论浓、稀硝酸均具有强氧化性,与金属反应时不放出
A.与金属反应:
铜与浓硝酸:
铜与稀硝酸:
银与浓硝酸:
常温下浓硝酸与铁、铝发生
B.与非金属反应:
碳与浓硝酸:
C.与其他还原剂反应,如H2S、SO2、Fe2+等。
D.与有机物反应:硝化反应、酯化反应、与蛋白质发生颜色反应等。
(3)制法
①实验室制法:硝酸盐与浓硫酸微热,
②工业制法:
氨的催化氧化法:
尾气处理:
(4)用途:
您最近一年使用:0次
21-22高一下·全国·单元测试
解题方法
3 . 1.氮的氧化物
(1)氮的氧化物
简介:氮元素有_______ 五种正价态,对应有六种氧化物
(2)NO和 的重要性质和制法(横线部分书写化学方程式)
的重要性质和制法(横线部分书写化学方程式)
①性质:_______ (易被氧气氧化,无色气体转化为红棕色);
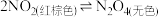 (平衡体系);
(平衡体系);
_______ (工业制硝酸);
_______ (尾气吸收);
 有较强的氧化性,能使湿润的KI淀粉试纸
有较强的氧化性,能使湿润的KI淀粉试纸_______ 。
②制法:
NO: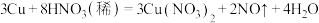 (必须
(必须_______ 法收集NO);
 :
: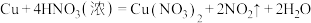 (必须
(必须_______ 法收集 )
)
(3)氮的氧化物溶于水的计算
① 或
或 与
与 (非
(非 )的混合气体溶于水可依据
)的混合气体溶于水可依据 利用气体体积变化差值进行计算。
利用气体体积变化差值进行计算。
② 和O2的混合气体溶于水时,由
和O2的混合气体溶于水时,由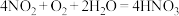 进行计算,当体积比
进行计算,当体积比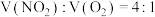 时,恰好反应;
时,恰好反应; 时,
时, 过量,剩余NO;
过量,剩余NO; 时,
时, 过量,剩余
过量,剩余 。
。
③NO和 同时通入水中时,由
同时通入水中时,由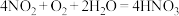 进行计算,原理同②。
进行计算,原理同②。
④NO、 、
、 的混合气体通入水中,先按①求出NO的体积,再加上混合气体中NO的体积再按③方法进行计算。
的混合气体通入水中,先按①求出NO的体积,再加上混合气体中NO的体积再按③方法进行计算。
(1)氮的氧化物
简介:氮元素有
| 种类 | 色态 | 化学性质 |
 | 无色气体 | 较不活泼 |
| NO | 活泼,不溶于水 | |
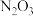 (亚硝酸酐) (亚硝酸酐) | 蓝色液体(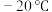 ) ) | 常温极易分解为NO, |
 | 较活泼,与水反应 | |
 | 无色气体 | 较活泼,受热易分解 |
 (硝酸酸酐) (硝酸酸酐) | 无色固体 | 气态时不稳定,易分解 |
 的重要性质和制法(横线部分书写化学方程式)
的重要性质和制法(横线部分书写化学方程式)①性质:
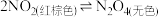 (平衡体系);
(平衡体系); 有较强的氧化性,能使湿润的KI淀粉试纸
有较强的氧化性,能使湿润的KI淀粉试纸②制法:
NO:
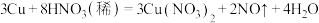 (必须
(必须 :
: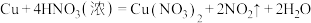 (必须
(必须 )
)(3)氮的氧化物溶于水的计算
①
 或
或 与
与 (非
(非 )的混合气体溶于水可依据
)的混合气体溶于水可依据 利用气体体积变化差值进行计算。
利用气体体积变化差值进行计算。②
 和O2的混合气体溶于水时,由
和O2的混合气体溶于水时,由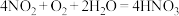 进行计算,当体积比
进行计算,当体积比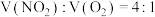 时,恰好反应;
时,恰好反应; 时,
时, 过量,剩余NO;
过量,剩余NO; 时,
时, 过量,剩余
过量,剩余 。
。③NO和
 同时通入水中时,由
同时通入水中时,由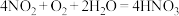 进行计算,原理同②。
进行计算,原理同②。④NO、
 、
、 的混合气体通入水中,先按①求出NO的体积,再加上混合气体中NO的体积再按③方法进行计算。
的混合气体通入水中,先按①求出NO的体积,再加上混合气体中NO的体积再按③方法进行计算。
您最近一年使用:0次
21-22高一下·全国·单元测试
解题方法
4 . 氮气(N2)
(1)分子结构:电子式为_______ ,结构式为_______ ,氮氮叁键键能大,分子结构_______ ,化学性质_______ 。
(2)物理性质:纯净的氮气是无色无味的_______ ,难溶于水,空气中约占总体积的_______ 。
(3)化学性质:常温下性质稳定,可作_______ ;但在高温、放电、点燃等条件下能与H2、O2、IIA族的Mg、Ca等发生化学反应,即发生氮的固定(将空气中的氮气转变为含氮化合物的过程,有_______ 和_______ 两种形式)。N2中N元素0价,为N的中间价态,既有氧化性又有还原性。
①与H2反应_______ 。
②与O2反应:_______ 。
③与活泼金属Mg反应:_______ 。
(4)氮气的用途:化工原料;_______ 是火箭燃烧的推进剂;还可用作医疗、保护气等。
(1)分子结构:电子式为
(2)物理性质:纯净的氮气是无色无味的
(3)化学性质:常温下性质稳定,可作
①与H2反应
②与O2反应:
③与活泼金属Mg反应:
(4)氮气的用途:化工原料;
您最近一年使用:0次
21-22高一下·全国·单元测试
解题方法
5 . 铵盐
(1)物理性质:_______ 色晶体,_______ 溶于水;
(2)化学性质:
①受热分解:
_______ ( 以上可分解),
以上可分解),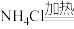
_______ ;
②与碱反应:在稀溶液中不加热反应离子方程式_______ ,铵盐与碱溶液加热条件下反应的离子方程式:_______ (该性质可用于氨气的制取和铵根离子的检验)。
(1)物理性质:
(2)化学性质:
①受热分解:

 以上可分解),
以上可分解),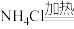
②与碱反应:在稀溶液中不加热反应离子方程式
您最近一年使用:0次
21-22高一下·全国·单元测试
解题方法
6 . 【卷号】15000
【题号】3491666971516928
6 .
(1)硫
物理性质
硫为_______ 黄色晶体,俗称_______ 。密度比水_______ ,不溶于_______ ,微溶于_______ ,易溶于_______ 。
(2)(2)化学性质
硫元素位于第3周期VIA族,原子最外层有6个电子,在反应中易得到2个电子而呈-2价;硫元素的最高正价为+6价;单质硫中硫元素的化合价为0,处于中间价态,故单质硫既有_______ 又有_______ ,在反应中既可作_______ 又可作_______ 。如:
①氧化性:
i.与金属反应
Na+S Na2S(剧烈反应,轻微爆炸)
Na2S(剧烈反应,轻微爆炸)
2Al+3S Al2S3
Al2S3
Fe+S
_______ (黑色)
2Cu+S
_______ (黑色)
ii.与非金属反应:H2+S
_______
②还原性
S+O2 SO2(在空气中燃烧产生淡蓝色火焰,在纯氧中燃烧产生明亮的蓝紫色火焰,均产生刺激性气味。)
SO2(在空气中燃烧产生淡蓝色火焰,在纯氧中燃烧产生明亮的蓝紫色火焰,均产生刺激性气味。)
S+2H2SO4(浓) 3SO2↑+2H2O
3SO2↑+2H2O
【注意】硫与氧气反应只能生成SO2,不能生成SO3
③既有氧化性又有还原性:3S+6NaOH 2Na2S+Na2SO3+3H2O
2Na2S+Na2SO3+3H2O
【拓展】3S+6KOH——K2SO3+2K2S+3H2O(可用热碱液除去试管中残留的硫)
特性:Hg、Ag在常温下不跟O2反应,但易跟S反应。Hg+S——HgS(可用于消除室内洒落的Hg)
(3)存在与用途:游离态的硫主要存在于_______ 。化合态主要以化合物的形式存在。硫黄主要用于制造_______ 等,还用于制造黑火药、烟花爆竹等。
【题号】3491666971516928
6 .
(1)硫
物理性质
硫为
(2)(2)化学性质
硫元素位于第3周期VIA族,原子最外层有6个电子,在反应中易得到2个电子而呈-2价;硫元素的最高正价为+6价;单质硫中硫元素的化合价为0,处于中间价态,故单质硫既有
①氧化性:
i.与金属反应
Na+S
 Na2S(剧烈反应,轻微爆炸)
Na2S(剧烈反应,轻微爆炸)2Al+3S
 Al2S3
Al2S3Fe+S

2Cu+S

ii.与非金属反应:H2+S

②还原性
S+O2
 SO2(在空气中燃烧产生淡蓝色火焰,在纯氧中燃烧产生明亮的蓝紫色火焰,均产生刺激性气味。)
SO2(在空气中燃烧产生淡蓝色火焰,在纯氧中燃烧产生明亮的蓝紫色火焰,均产生刺激性气味。)S+2H2SO4(浓)
 3SO2↑+2H2O
3SO2↑+2H2O【注意】硫与氧气反应只能生成SO2,不能生成SO3
③既有氧化性又有还原性:3S+6NaOH
 2Na2S+Na2SO3+3H2O
2Na2S+Na2SO3+3H2O【拓展】3S+6KOH——K2SO3+2K2S+3H2O(可用热碱液除去试管中残留的硫)
特性:Hg、Ag在常温下不跟O2反应,但易跟S反应。Hg+S——HgS(可用于消除室内洒落的Hg)
(3)存在与用途:游离态的硫主要存在于
您最近一年使用:0次
21-22高一下·全国·单元测试
解题方法
7 . 新型无机非金属材料
(1)硅单质
①Si位于元素周期表第_______ 周期,第_______ 族,处于金属与非金属过渡位置,为半导体材料。硅在地壳中含量仅次于氧,居第2位。
②硅在自然界的存在形态:没有游离态,只有化合态_______ 、硅酸盐。
③用途:主要用来做集成电路、晶体管、硅整流器等_______ 材料,还可以制成太阳能电池、硅的合金可用来制造变压器铁芯等。
(2)二氧化硅(硅石)
①SiO2是自然界中沙子、石英的主要成分。天然二氧化硅叫_______ ;结晶的二氧化硅叫_______ 。二氧化硅可以用来制造_______ ,具有优良的性能。
②光导纤维主要特性:①抗干扰性能好,不发生辐射;②通讯质量好;③质量轻、耐腐蚀。
(1)硅单质
①Si位于元素周期表第
②硅在自然界的存在形态:没有游离态,只有化合态
③用途:主要用来做集成电路、晶体管、硅整流器等
(2)二氧化硅(硅石)
①SiO2是自然界中沙子、石英的主要成分。天然二氧化硅叫
②光导纤维主要特性:①抗干扰性能好,不发生辐射;②通讯质量好;③质量轻、耐腐蚀。
您最近一年使用:0次
8 . 检验
检验硫酸根离子的正确操作方法:_______ 。先加稀盐酸的目的是_______ 。检验硫酸根离子一定要先加入稀盐酸,再加入氯化钡溶液,若有白色沉淀生成,则说明存在硫酸根离子。

检验硫酸根离子的正确操作方法:
您最近一年使用:0次
21-22高一下·全国·单元测试
解题方法
9 . 稀硫酸的性质:硫酸是强酸,具有酸的通性。
(1)使指示剂变色(如石蕊试液),溶液变_______ 。
(2)与活泼金属反应(如Fe、Zn),生成_______ 。
(3)与碱性氧化物反应(如CuO),生成_______ 。
(4)与碱发生中和反应(如Ba(OH)2),生成_______ 。
(5)与弱酸盐反应(如Na2CO3),生成_______ 。
(1)使指示剂变色(如石蕊试液),溶液变
(2)与活泼金属反应(如Fe、Zn),生成
(3)与碱性氧化物反应(如CuO),生成
(4)与碱发生中和反应(如Ba(OH)2),生成
(5)与弱酸盐反应(如Na2CO3),生成
您最近一年使用:0次
21-22高一下·全国·单元测试
解题方法
10 . 浓硫酸的特性:浓硫酸主要以分子形式存在,所以具有和稀硫酸不同的化学性质。
(1)吸水性(吸收游离的水)
浓硫酸能够吸收气体、液体中的水分子及固体中的结晶水,故常用作_______ 。吸水性属于_______ 变化。
【思考】不能用浓硫酸干燥的气体有哪些?
浓硫酸常用来干燥_______ 气体和_______ 气体,如_______ 等。不能用浓硫酸干燥的气体有碱性气体如_______ 、还原性气体如_______ 。
(2)脱水性(有机物中的H、O元素按2:1的比例脱去)
浓硫酸能够将蔗糖、纸张、棉布和木材等有机物中的_______ 元素和_______ 元素按水的组成比脱去。(注意:物质本身不含水)
(3)强氧化性
①与金属反应:常温时Fe、Al等少数金属遇浓硫酸发生_______ 。加热时,浓硫酸可以与除金、铂之外的_______ 反应。
②与非金属反应(与C的反应)化学方程式:_______ 。
③与还原性化合物(H2S、HBr)反应:_______ 、_______ 。
(1)吸水性(吸收游离的水)
浓硫酸能够吸收气体、液体中的水分子及固体中的结晶水,故常用作
【思考】不能用浓硫酸干燥的气体有哪些?
浓硫酸常用来干燥
(2)脱水性(有机物中的H、O元素按2:1的比例脱去)
浓硫酸能够将蔗糖、纸张、棉布和木材等有机物中的
(3)强氧化性
①与金属反应:常温时Fe、Al等少数金属遇浓硫酸发生
②与非金属反应(与C的反应)化学方程式:
③与还原性化合物(H2S、HBr)反应:
您最近一年使用:0次



