解题方法
1 . 有关胶体性质的说法正确的是
| A.过滤可以分离Fe(OH)3胶体和FeCl3溶液 |
| B.Fe(OH)3.胶体与FeCl3溶液的本质区别是可以发生丁达尔效应 |
| C.雾是气溶胶,在阳光下可观察到丁达尔效应 |
| D.Fe(OH)3胶体的制备是在饱和氯化铁溶液中逐滴加入NaOH溶液,再煮沸 |
您最近一年使用:0次
名校
解题方法
2 . 最近,华为Mate60 Pro上市,其搭载的新型麒麟9000s芯片,突破了美国的芯片封锁,实现了智能手机5G芯片国产化。下列有关说法正确的是
| A.晶体硅和无定形硅是硅元素的同素异形体,二者化学性质完全不同 |
B.工业粗硅的冶炼方法为 ,在该反应中 ,在该反应中 作还原剂 作还原剂 |
| C.硅是芯片的主要成分之一,晶体硅是一种性能优良的半导体材料,它属于非电解质 |
| D.光刻胶是制造芯片的关键材料,金属氧化物纳米颗粒光刻胶由金属氧化物纳米簇和溶剂等组成,是一种胶体 |
您最近一年使用:0次
名校
3 . 化学与生活、社会发展息息相关。下列叙述不正确的是
| A.胶体区别于其他分散系的本质特征是分散质粒子直径的大小 |
B.“纳米汽车”用 作车轮, 作车轮, 、金刚石和石墨互为同素异形体 、金刚石和石墨互为同素异形体 |
| C.“熬胆矾铁釜,久之亦化为铜”,该过程涉及置换反应、离子反应 |
| D.我国十大科技成果之一的“纳米氮化镓(GaN)”是一种胶体 |
您最近一年使用:0次
名校
解题方法
4 . 下列关于胶体的说法,不正确的是
| A.胶体与其他分散系的本质区别是粒子直径的大小 |
| B.CuSO4溶液和Fe(OH)3胶体都能产生丁达尔效应 |
| C.明矾净水是利用胶体的吸附性 |
| D.雾、豆浆、淀粉溶液属于胶体 |
您最近一年使用:0次
5 . 2023年化学诺贝尔奖授予了三位研究量子点的科学家。量子点是一种纳米级的半导体材料,其尺寸通常在1-20nm之间,常见的量子点有CdS、ZnS等,在医疗,科技等多个领域有广泛的应用。下列叙述错误的是
| A.CdS、ZnS量子点属于金属材料 | B.量子点可用于制作太阳能电池 |
| C.量子点与水形成的分散系能产生丁达尔效应 | D.X射线衍射实验可测定量子点晶体结构 |
您最近一年使用:0次
2024-03-30更新
|
520次组卷
|
3卷引用:广东省高州市第四中学2023-2024学年高二下学期月考化学试题
名校
6 . “点水成冰”实验中,用蘸有 粉末的小棒触碰液体球后(成分为饱和
粉末的小棒触碰液体球后(成分为饱和 溶液),它开始“结冰”。下列说法错误的是
溶液),它开始“结冰”。下列说法错误的是
 粉末的小棒触碰液体球后(成分为饱和
粉末的小棒触碰液体球后(成分为饱和 溶液),它开始“结冰”。下列说法错误的是
溶液),它开始“结冰”。下列说法错误的是A.液体球中分散质粒子直径小于 m m |
B. 属于离子化合物,只含离子键 属于离子化合物,只含离子键 |
C.向 溶液中加入NaOH固体,溶液导电性逐渐增强 溶液中加入NaOH固体,溶液导电性逐渐增强 |
D. 中四种元素的原子半径:Na>C>O>H 中四种元素的原子半径:Na>C>O>H |
您最近一年使用:0次
2024-03-26更新
|
66次组卷
|
3卷引用:山西省大同市2023-2024学年高一下学期3月月考化学试题
名校
解题方法
7 . 当光束通过下列分散系时,能产生丁达尔效应的是
| A.稀HNO3 | B.CuSO4溶液 |
C. 胶体 胶体 | D.NaNO3溶液 |
您最近一年使用:0次
解题方法
8 . 用特殊的方法把固体加工成纳米级(直径为1-100nm)的超细粉末粒子,可制得纳米材料。下列分散系中,分散质粒子的直径和这种超细粉末粒子的直径具有相同数量级的是
| A.溶液 | B.胶体 | C.悬浊液 | D.乳浊液 |
您最近一年使用:0次
2024-03-06更新
|
101次组卷
|
3卷引用:福建省厦门英才学校2023-2024学年高一下学期3月月考化学试卷(学考)
9 . 高铁酸钾(K2FeO4)是一种新型高效的水处理剂,在碱性溶液中较稳定。工业上有干法与湿法两种制备高铁酸钾的方法。(已知:Fe3++3H2O⇌Fe(OH)3+3H+)
(1)高铁酸钾可用于杀菌消毒,是因为它具有强___________ 性。
(2)高铁酸钾被用于消毒后,产物与水形成一种分散系,其中的分散质能使得水中的悬浮杂质聚沉,方便除去,这是因为________ 。这种分散系区分于其他分散系的最本质区别是_________ 。
(3)在使用高铁酸钾时,常通过测定其纯度来判断是否变质。K2FeO4在硫酸溶液中发生如下反应:______ +______H+=_____O2↑+______Fe3++_______。
+______H+=_____O2↑+______Fe3++_______。
①完成上述离子方程式:___________ 。
②现取10.00g样品,加入稀硫酸完全反应后,共收集到0.8064L气体(已换算成标准状况)。则样品中高铁酸钾的质量分数约为___________ 。(计算结果保留到0.1%)
湿法制备高铁酸钾的流程如下图。
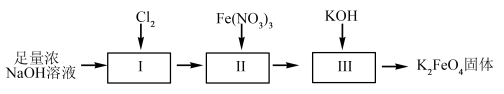
(4)过程II为碱性条件下制备高铁酸钠。写出过程II中反应的离子方程式,并标出电子转移方向和数目。___________ ,反应每生成1molCl-转移的电子数目为___________ 。
(5)湿法制备时,不同的温度下,不同质量浓度的Fe3+对K2FeO4生成率有不同影响,由下图可知工业生产中最佳条件(温度和Fe3+的质量浓度)为___________。

(1)高铁酸钾可用于杀菌消毒,是因为它具有强
(2)高铁酸钾被用于消毒后,产物与水形成一种分散系,其中的分散质能使得水中的悬浮杂质聚沉,方便除去,这是因为
(3)在使用高铁酸钾时,常通过测定其纯度来判断是否变质。K2FeO4在硫酸溶液中发生如下反应:______
 +______H+=_____O2↑+______Fe3++_______。
+______H+=_____O2↑+______Fe3++_______。①完成上述离子方程式:
②现取10.00g样品,加入稀硫酸完全反应后,共收集到0.8064L气体(已换算成标准状况)。则样品中高铁酸钾的质量分数约为
湿法制备高铁酸钾的流程如下图。

(4)过程II为碱性条件下制备高铁酸钠。写出过程II中反应的离子方程式,并标出电子转移方向和数目。
(5)湿法制备时,不同的温度下,不同质量浓度的Fe3+对K2FeO4生成率有不同影响,由下图可知工业生产中最佳条件(温度和Fe3+的质量浓度)为___________。

| A.24℃,75g∙L-1 | B.26℃,75g∙L-1 | C.28℃,75g∙L-1 | D.22℃,80g∙L-1 |
您最近一年使用:0次
名校
解题方法
10 . 下图是侯氏制碱法在实验室进行模拟实验的生产流程示意图,则下列叙述正确的是
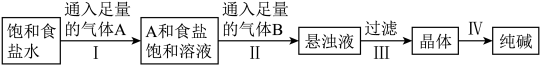

| A.通入A气体是为了使溶液呈酸性 |
| B.第Ⅱ步得到的悬浊液不属于分散系 |
| C.第Ⅲ步操作中析出晶体,是因为该晶体的溶解度相对较小 |
| D.第Ⅳ步操作得到的物质用来治疗胃酸过多 |
您最近一年使用:0次



