解题方法
1 . 下列关于钠、氯、铁及其化合物说法正确的是
A. 可与水反应生成NaOH,说明 可与水反应生成NaOH,说明 是碱性氧化物 是碱性氧化物 |
B.新制氯水光照下容易分解产生 ,实验室需用棕色瓶密封保存 ,实验室需用棕色瓶密封保存 |
C.侯德榜制碱法利用了 在溶液中溶解度较小的性质 在溶液中溶解度较小的性质 |
D.向NaOH溶液中滴加5~6滴饱和 溶液可制得 溶液可制得 胶体 胶体 |
您最近一年使用:0次
名校
解题方法
2 . 制取Fe(OH)3胶体的两个方案如下:

(1)实验1,生成Fe(OH)3胶体的方程式为___________ 。
(2)用最简单的方法判断溶液中是否成功制备胶体,写出相关的操作、现象和结论_________________ ,能产生该现象的原因是胶体粒子对光波的___________ 所致。
(3)实验2与实验1对比,优点是___________ 。
(4)将稀盐酸逐滴加入制得的Fe(OH)3胶体中,实验现象为___________ , 反应方程式为___________ 。
(5)制得的Fe(OH)3胶体中往往混有H+和Cl-,可以利用___________ 的方法来提纯Fe(OH)3胶体。

| 实验 | 实验操作 |
| 1 | 向40mL沸腾的蒸馏水中滴入5滴饱和FeCl3溶液(质量分数约为30%) |
| 2 | 向40mL蒸馏水中滴入5滴质量分数为10%的FeCl3溶液,然后滴入1滴质量分数为10%的NaOH溶液,边滴边搅拌 |
(1)实验1,生成Fe(OH)3胶体的方程式为
(2)用最简单的方法判断溶液中是否成功制备胶体,写出相关的操作、现象和结论
(3)实验2与实验1对比,优点是
(4)将稀盐酸逐滴加入制得的Fe(OH)3胶体中,实验现象为
(5)制得的Fe(OH)3胶体中往往混有H+和Cl-,可以利用
您最近一年使用:0次
名校
3 . FeCl3是实验室常见的药品,将少量FeCl3饱和溶液分别滴加到下列物质中,可得到三种分散系。

回答下列问题:
(1)可判断丙中成功制备胶体的是_________
(2)关于分散系的下列说法中,正确的是_________
(3)用括号中注明的方法分离下列各组混合物,其中正确的是_________
(4)丙中溶液液体呈透明的红褐色,发生反应的化学方程式为___________ 。
(5)现有另一胶体丁,向丁中插入电极通电,胶体粒子移向电源正极相连的一极,说明该胶体粒子带___________ 电荷;将丁与丙混合,可观察到___________ 现象。
(6)用如图所示的装置来提纯丙中制得的胶体,实验过程中需不断更换烧杯中的蒸馏水。证明胶体中杂质离子已经完全除去的方法是___________ 。

(7)四氯化碳也是一种重要的含氯化合物,其沸点约为76℃。碘单质沸点为184℃。若要从含碘的四氯化碳中提取碘和回收四氯化碳,还需要经过蒸馏,装置如图(加热和夹持装置已略去)。冷凝水应从___________ (填a或b)口通入,该装置使用水浴加热的优点是___________ ,最后晶态碘在___________ 里聚集(填仪器名称)。


回答下列问题:
(1)可判断丙中成功制备胶体的是_________
| A.布朗运动 | B.丁达尔现象 |
| C.形成分散系 | D.形成澄清透明的液体 |
(2)关于分散系的下列说法中,正确的是_________
| A.分散系一定是混合物 | B.分散剂一定是液体 |
| C.一种分散系里只能有一种分散质 | D.胆矾、空气、有色玻璃都是分散系 |
(3)用括号中注明的方法分离下列各组混合物,其中正确的是_________
| A.溴的四氯化碳溶液(分液) |
| B.淀粉和水(过滤) |
| C.KCl和MnO2(溶解过滤,再蒸发结晶) |
| D.碘和蒸馏水(萃取) |
(4)丙中溶液液体呈透明的红褐色,发生反应的化学方程式为
(5)现有另一胶体丁,向丁中插入电极通电,胶体粒子移向电源正极相连的一极,说明该胶体粒子带
(6)用如图所示的装置来提纯丙中制得的胶体,实验过程中需不断更换烧杯中的蒸馏水。证明胶体中杂质离子已经完全除去的方法是

(7)四氯化碳也是一种重要的含氯化合物,其沸点约为76℃。碘单质沸点为184℃。若要从含碘的四氯化碳中提取碘和回收四氯化碳,还需要经过蒸馏,装置如图(加热和夹持装置已略去)。冷凝水应从

您最近一年使用:0次
解题方法
4 . 如图是实验室制备Fe(OH)3胶体并验证丁达尔效应的示意图,下列说法错误的是
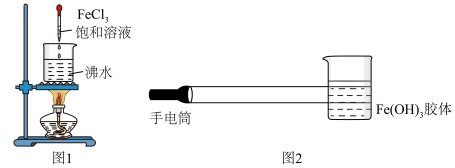

A.制备氢氧化铁胶体的化学反应方程式为FeCl3+3H2O Fe(OH)3(胶体)+3HCl Fe(OH)3(胶体)+3HCl |
| B.光束通过胶体时有一条光亮的“通路”,是胶体粒子对光线散射形成的 |
C.此实验需要加热,故应在实验设计时注明 以作提醒 以作提醒 |
| D.氢氧化铁胶体不属于分散系 |
您最近一年使用:0次
5 . 下列实验过程不能达到目的的是
| 编号 | 实验目的 | 实验过程 |
| A | 比较 和 和 的Ksp大小 的Ksp大小 | 向饱和 溶液滴加碳酸钠溶液,产生白色沉淀 溶液滴加碳酸钠溶液,产生白色沉淀 |
| B | 制备 胶体 胶体 | 将5~6滴饱和 溶液滴入40mL沸水中,继续加热并搅拌一段时间,可观察到生成红褐色液体 溶液滴入40mL沸水中,继续加热并搅拌一段时间,可观察到生成红褐色液体 |
| C | 验证气体分子的扩散会自发的向混乱度增大方向进行 | 两个广口瓶中分别盛有氯气和氢气,倒扣在一起,开始时中间用玻璃片隔开,抽掉玻璃片后,可观察到最后两瓶气体均显浅黄绿色,且颜色相同 |
| D | 验证温度对化学平衡的影响 | 把 和 和 的混合气体通入两只连通的烧瓶,中间的乳胶管用弹簧夹夹住,分别将两只烧瓶浸泡在热水和冷水中,可观察到两只烧瓶中气体的颜色深浅不同 的混合气体通入两只连通的烧瓶,中间的乳胶管用弹簧夹夹住,分别将两只烧瓶浸泡在热水和冷水中,可观察到两只烧瓶中气体的颜色深浅不同 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 下列说法合理的是:
| A.氯化铁溶液在空气中加热、蒸干、灼烧得到的固体不是氯化铁 |
| B.向热的稀氢氧化钠溶液中滴加饱和氯化铁溶液,制备氢氧化铁胶体 |
| C.明矾净水的主要作用就杀菌消毒 |
| D.氯化铝溶液可以导电,氯化铝是离子化合物 |
您最近一年使用:0次
7 . 定性和定量是中学化学研究物质性质、组成的常用方法。胶体是一种重要的分散系(三种分散系分散质粒子大小如图示)。
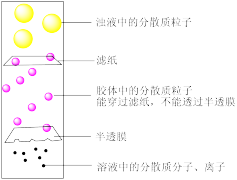
某兴趣小组按如下实验步骤制备Cu(OH)2胶体:用洁净的烧杯取少量蒸馏水,加热至沸腾,向烧杯中慢慢加入数滴浓CuCl2溶液,得到蓝色透明的液体。制备原理用化学方程式表示为:CuCl2+2H2O(沸水)=Cu(OH)2(胶体)+2HCl。
(1)Cu(OH)2胶体中分散质微粒直径范围是_____ 。
(2)Cu(OH)2浊液与Cu(OH)2胶体性质不同,本质原因是_____ 。
(3)下列哪种用于判断胶体制备成功的方法最简单_____ 。
(4)实验过程中,有一位同学向烧杯中一次性加入大量CuCl2溶液,结果没有制得胶体,反而出现了浑浊,请分析他实验失败的原因_____ 。

某兴趣小组按如下实验步骤制备Cu(OH)2胶体:用洁净的烧杯取少量蒸馏水,加热至沸腾,向烧杯中慢慢加入数滴浓CuCl2溶液,得到蓝色透明的液体。制备原理用化学方程式表示为:CuCl2+2H2O(沸水)=Cu(OH)2(胶体)+2HCl。
(1)Cu(OH)2胶体中分散质微粒直径范围是
| A.小于1nm | B.1~10nm | C.1~100 | D.大于100nm |
| A.分散剂的种类不同 | B.颜色和透明程度不同 |
| C.分散质粒子的大小不同 | D.分散质粒子所带电荷不同 |
| A.丁达尔现象 | B.半透膜实验 | C.聚沉 | D.电泳 |
您最近一年使用:0次
2023-01-10更新
|
378次组卷
|
2卷引用:上海市闵行区2022-2023学年高一上学期期末统考化学试题
解题方法
8 . 下列各组实验的叙述正确的是
A.制备 胶体:向稀 胶体:向稀 溶液中滴入饱和 溶液中滴入饱和 溶液 溶液 |
B.检验 与水反应产物:用试管收集产生的气体,靠近火焰,听是否有爆鸣声 与水反应产物:用试管收集产生的气体,靠近火焰,听是否有爆鸣声 |
| C.配制溶液:容量瓶洗涤后无需干燥,可直接配制溶液 |
D.除去 溶液中混有的 溶液中混有的 :取混合物于烧杯中,加入过量盐酸 :取混合物于烧杯中,加入过量盐酸 |
您最近一年使用:0次
2023-01-10更新
|
234次组卷
|
2卷引用:广东省广州市2022-2023学年高一上学期期末化学试题
解题方法
9 . 下列实验方案及现象正确的是
| A.钠与氧气在加热条件下反应,可观察到钠迅速熔化成一个小球,发出黄色火焰,生成白色固体 |
| B.制备Fe(OH)2白色沉淀的方法是:用胶头滴管在试管口向FeSO4溶液中滴加NaOH溶液 |
| C.用洁净的铂丝蘸取某溶液,放在火焰上灼烧,观察到黄色火焰,则证明该溶液中一定有Na+ |
| D.氢氧化铁胶体的制备方法是:在沸水中滴加饱和氯化铁溶液,继续加热直到产生红褐色沉淀,停止加热 |
您最近一年使用:0次
名校
解题方法
10 . 下列说法正确的是
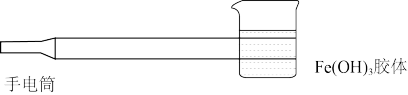

| A.实验室中进行Fe(OH)3胶体丁达尔效应实验时的示意图 |
| B.空气中的细颗粒物(PM2.5)其中细颗粒物的直径小于2.5um,其在空气中形成的分散系属于胶体 |
| C.丁达尔效应:光束通过胶体时有一条光亮的“通路”,原因是胶体粒子对光线散射形成的 |
| D.Fe(OH)3胶体制备的方程式: FeCl3+3H2O=Fe(OH)3↓+3HCl |
您最近一年使用:0次
2022-10-27更新
|
136次组卷
|
2卷引用:吉林省吉林市第二中学2022-2023学年高一上学期1月期末考试化学试题



