名校
1 . 下列实验操作能够达到实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 向乙酸乙酯(含少量乙酸)样品中加入乙醇、浓硫酸 | 除去乙酸乙酯中的少量乙酸 |
| B | 将饱和氯化铁溶液逐滴滴加到稀氨水中 | 制备 胶体 胶体 |
| C | 将硝酸银溶液逐滴滴加到氨水中,溶液恰好澄清 | 配制银氨溶液 |
| D | 用 计测定相同浓度的 计测定相同浓度的 和醋酸钠溶液 和醋酸钠溶液 大小 大小 | 验证 酸性弱于醋酸 酸性弱于醋酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-17更新
|
295次组卷
|
3卷引用:湖南省长沙市一中2024届高三下学期高考适应性演练(三)化学试题
解题方法
2 . 下列关于元素及其化合物的性质说法错误的是
| A.饱和氯化铁溶液可制备氢氧化铁胶体 |
| B.普通玻璃由纯碱、石灰石和石英砂制成,其熔点很高 |
| C.镁在空气中燃烧可生成氧化镁和氮化镁 |
| D.铁、铜与足量的单质硫反应均生成其低价硫化物 |
您最近一年使用:0次
3 . 铁是地壳中占比较高的元素,其化合物在自然界十分常见。
(1)某铁原子可表示为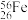 ,其核内中子数是
,其核内中子数是___________ 。
(2)将一个铁球打磨、烧红后放入充满水蒸气的容器中,则发生反应的化学方程式为___________ ;设阿伏加德罗常数的值为 ,当参与反应的
,当参与反应的 的物质的量为
的物质的量为 时,转移的电子数为
时,转移的电子数为___________ 。
(3)服用乳酸亚铁咀嚼片可以缓解缺铁性贫血的症状,其在长期贮存过程中可能因氧化而发生变质,现取少量药片碾碎、溶解、过滤,取滤液加入___________ 溶液并振荡,若滤液变为红色,则药品已变质。
(4)现有甲、乙、丙三名同学分别进行制备 胶体的实验。甲同学向
胶体的实验。甲同学向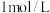 氯化铁溶液中滴入少量的
氯化铁溶液中滴入少量的 溶液;乙同学向
溶液;乙同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液;丙同学直接加热
饱和溶液;丙同学直接加热 饱和
饱和 溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
①操作正确的同学是___________ 。
②写出制备胶体过程中的离子方程式___________ 。欲除去胶体中混有的 杂质,可以采取的操作方法是
杂质,可以采取的操作方法是___________ 。
③丁同学向所得胶体中逐滴滴加稀硫酸,实验现象为___________ 。
(1)某铁原子可表示为
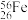 ,其核内中子数是
,其核内中子数是(2)将一个铁球打磨、烧红后放入充满水蒸气的容器中,则发生反应的化学方程式为
 ,当参与反应的
,当参与反应的 的物质的量为
的物质的量为 时,转移的电子数为
时,转移的电子数为(3)服用乳酸亚铁咀嚼片可以缓解缺铁性贫血的症状,其在长期贮存过程中可能因氧化而发生变质,现取少量药片碾碎、溶解、过滤,取滤液加入
(4)现有甲、乙、丙三名同学分别进行制备
 胶体的实验。甲同学向
胶体的实验。甲同学向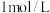 氯化铁溶液中滴入少量的
氯化铁溶液中滴入少量的 溶液;乙同学向
溶液;乙同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液;丙同学直接加热
饱和溶液;丙同学直接加热 饱和
饱和 溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。①操作正确的同学是
②写出制备胶体过程中的离子方程式
 杂质,可以采取的操作方法是
杂质,可以采取的操作方法是③丁同学向所得胶体中逐滴滴加稀硫酸,实验现象为
您最近一年使用:0次
解题方法
4 . 特殊的分散系——胶体
把一种或多种物质分散在另一种物质中所得到的体系称为分散系,接照分散质的大小可将分散系分为溶液、胶体和浊液三类。三者之间无明显界限。胶体是物质的一种分散状态,比较稳定,外观上胶体溶液不浑浊,用肉眼或普通显微镜均不能辨别。很多蛋白质、淀粉、血液、淋巴液等都属于胶体。胶体还可以按照分散剂的状态分为固溶胶如有色玻璃、气溶胶如雾、烟和液溶胶如FeOH3胶体。1.胶体可以稳定存在的主要原因是______。
| A.胶体粒子直径在1~100nm之间 | B.胶体具有丁达尔现象 |
| C.胶粒带电 | D.胶体外观均匀 |
| A.在豆浆中加入盐卤做豆腐 |
| B.河流入海处易形成沙洲 |
| C.一束平行光线照射蛋白质溶液时,从侧面可看到光亮的通路 |
| D.三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀 |
| A.蛋白质溶液 | B.氨水 | C.食盐水 | D.酒精溶液 |
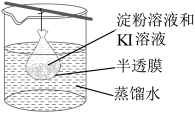
5.在小烧杯中加入20mL蒸馏水加热煮沸后,向沸水申滴入几滴饱和的FeCl3溶液,继续煮沸至溶液呈色即制得FeOH3胶体。
①写出上述胶体制备的化学反应方程式
②取制得的FeOH3胶体装入U形管中,用石墨电极接通直流电,通电一段时间后,发现阴极附近的颜色加深,说明氢氧化铁胶粒带
③另取制得的FeOH3胶体于洁净的试管中,向其中逐滴滴加过量稀硫酸,边滴边振荡,观察到的现象是
您最近一年使用:0次
5 . 历经十年传承积淀,形成精湛的东阿阿胶传统工艺,包括洗皮、泡皮、晾皮、刮毛、铡皮、化皮、打沫、除渣、浓缩、挂旗、凝胶、切胶等工序。下列工序与化学实验中的原理不具有对应关系的是
| 选项 | A | B | C | D |
| 工序 |
|
|
|
|
| 化学实验 |
|
|
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 完成下列实验,选用仪器(非玻璃仪器任选)正确的是
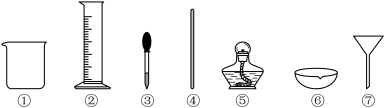

A.由浓硫酸配制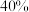 的稀硫酸:①②③④ 的稀硫酸:①②③④ |
B.测定 晶体中结晶水的含量:③⑤ 晶体中结晶水的含量:③⑤ |
C. 胶体的制备:①④⑤ 胶体的制备:①④⑤ |
| D.食盐精制:①③④⑤⑥ |
您最近一年使用:0次
名校
解题方法
7 . 下列实验设计及装置(夹持仪器略去)的使用正确的是


| A.用装置甲测定锌和稀硫酸反应的速率 |
| B.用装置乙量取稀盐酸时读数为24.10mL |
| C.用装置丙探究浓度对反应速率的影响 |
| D.用装置丁制备氢氧化铁胶体 |
您最近一年使用:0次
2024-03-13更新
|
107次组卷
|
2卷引用:湖南省岳阳市岳阳县第一中学2023-2024学年高二下学期开学化学试题
名校
8 . 下列有关实验操作或反应现象的叙述中正确的是
| A.在氢氧化钠溶液中滴入氯化铁饱和溶液,用于制备氢氧化铁胶体 |
| B.进行焰色试验时,若实验室无铂丝或铁丝,可以用玻璃棒代替 |
| C.用玻璃棒蘸取少量新制氯水点在pH试纸上,并与标准比色卡对照,测定其pH |
| D.将足量二氧化硫通入滴有酚酞的氢氧化钠溶液中,溶液褪色 |
您最近一年使用:0次
名校
解题方法
9 . 如图为制取无水氯化铁粉末的装置,已知氯化铁粉末很容易吸水生成含结晶水的化合物。
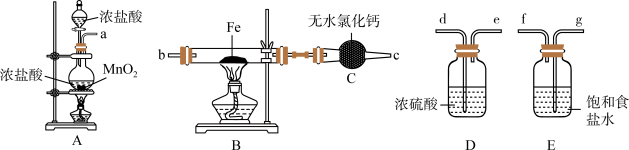
回答下列问题:
(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序):___________ 。
(2)装置A中发生反应的离子方程式为___________ 。
(3)装置E的作用是___________ 。
(4)这套实验装置的缺陷是没有尾气处理装置,应增加一个装有 溶液的烧杯吸收尾气,发生反应的化学方程式为
溶液的烧杯吸收尾气,发生反应的化学方程式为___________ 。
(5)利用制取的无水氯化铁固体配制少量 饱和溶液并制备
饱和溶液并制备 胶体。
胶体。
①溶解制取的无水氯化铁固体时,发现溶液偏浅绿色,取少量溶液于试管中,滴加几滴酸性高锰酸钾溶液,发现高锰酸钾颜色褪去,发生反应的离子方程式为___________ ;溶解所得溶液中含有 的原因可能是
的原因可能是___________ 。
②向沸水中滴加少量 饱和溶液,继续煮沸,至
饱和溶液,继续煮沸,至___________ (填实验现象)时停止,得到 胶体。
胶体。

回答下列问题:
(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序):
(2)装置A中发生反应的离子方程式为
(3)装置E的作用是
(4)这套实验装置的缺陷是没有尾气处理装置,应增加一个装有
 溶液的烧杯吸收尾气,发生反应的化学方程式为
溶液的烧杯吸收尾气,发生反应的化学方程式为(5)利用制取的无水氯化铁固体配制少量
 饱和溶液并制备
饱和溶液并制备 胶体。
胶体。①溶解制取的无水氯化铁固体时,发现溶液偏浅绿色,取少量溶液于试管中,滴加几滴酸性高锰酸钾溶液,发现高锰酸钾颜色褪去,发生反应的离子方程式为
 的原因可能是
的原因可能是②向沸水中滴加少量
 饱和溶液,继续煮沸,至
饱和溶液,继续煮沸,至 胶体。
胶体。
您最近一年使用:0次
2024-03-02更新
|
80次组卷
|
2卷引用:内蒙古自治区乌兰浩特第一中学2023-2024学年高一上学期期末考试化学试题
名校
解题方法
10 . 实验室中将饱和 溶液滴入沸水中可制得胶体,下列说法正确的是
溶液滴入沸水中可制得胶体,下列说法正确的是
 溶液滴入沸水中可制得胶体,下列说法正确的是
溶液滴入沸水中可制得胶体,下列说法正确的是A.从外观上,无法区分 溶液和 溶液和 胶体 胶体 |
B.利用半透膜进行渗析,可除去 胶体中的 胶体中的 |
C. 胶体带正电,故进行电泳实验时,阴极周围的颜色会加深 胶体带正电,故进行电泳实验时,阴极周围的颜色会加深 |
D.利用饱和 溶液与浓氨水反应也可制得 溶液与浓氨水反应也可制得 胶体 胶体 |
您最近一年使用:0次