1 . 高铁酸钾( 极易溶于水)是常见的水处理剂,其原理如图所示。
极易溶于水)是常见的水处理剂,其原理如图所示。
(1) 中铁元素的化合价为
中铁元素的化合价为___________ 价。
(2)过程①中活细菌表现了___________ (填“氧化”或“还原”)性。
(3)净水利用了 胶体聚沉作用,请写出
胶体聚沉作用,请写出 胶体制备化学方程式
胶体制备化学方程式___________ 。
(4)根据上述原理分析,作水处理剂时, 的作用有
的作用有___________ 和净水剂。
(5)还可用干法制备高铁酸钠,主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,(Na2O2中氧元素为-1价)该反应中还原剂是___________ 。(填化学式)
(6)已知铁与水蒸气发生如下反应: ,请用单线桥法表示电子转移的方向和数目:
,请用单线桥法表示电子转移的方向和数目:___________ ;该反应的还原产物是___________ 。
 极易溶于水)是常见的水处理剂,其原理如图所示。
极易溶于水)是常见的水处理剂,其原理如图所示。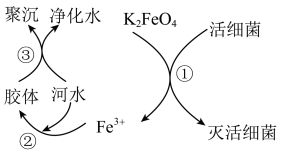
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)过程①中活细菌表现了
(3)净水利用了
 胶体聚沉作用,请写出
胶体聚沉作用,请写出 胶体制备化学方程式
胶体制备化学方程式(4)根据上述原理分析,作水处理剂时,
 的作用有
的作用有(5)还可用干法制备高铁酸钠,主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,(Na2O2中氧元素为-1价)该反应中还原剂是
(6)已知铁与水蒸气发生如下反应:
 ,请用单线桥法表示电子转移的方向和数目:
,请用单线桥法表示电子转移的方向和数目:
您最近一年使用:0次
解题方法
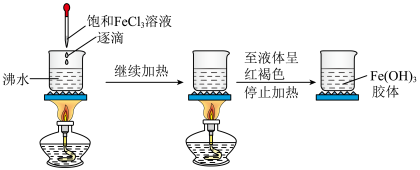
2 . 氢氧化铁胶体的制备实验如图所示。取一小烧杯,加入25mL蒸馏水,加热至沸腾,向沸水中逐滴加入1~2mL饱和氯化铁溶液,继续煮沸至透明的红褐色液体,停止加热。
(1)氢氧化铁胶体中分散质微粒直径的范围是______ 。
(2)写出制备氢氧化铁胶体的化学方程式:______ 。
(3)证明有氢氧化铁胶体生成的实验操作是______ 。
(4)除去氢氧化铁胶体中的氯化铁采用的方法是______ (填写字母)。
a.过滤 b.蒸发 c.渗析
(5)下列关于 胶体的制备和性质的叙述中,正确的是
胶体的制备和性质的叙述中,正确的是______ (填写字母)。
a. 胶体与
胶体与 溶液、
溶液、 沉淀的本质区别是:
沉淀的本质区别是: 胶体具有丁达尔效应
胶体具有丁达尔效应
b.不能用饱和 溶液与浓NaOH溶液反应制备氢氧化铁胶体
溶液与浓NaOH溶液反应制备氢氧化铁胶体
c. 胶体属于纯净物,而
胶体属于纯净物,而 溶液属于混合物
溶液属于混合物
(1)氢氧化铁胶体中分散质微粒直径的范围是
(2)写出制备氢氧化铁胶体的化学方程式:
(3)证明有氢氧化铁胶体生成的实验操作是
(4)除去氢氧化铁胶体中的氯化铁采用的方法是
a.过滤 b.蒸发 c.渗析
(5)下列关于
 胶体的制备和性质的叙述中,正确的是
胶体的制备和性质的叙述中,正确的是a.
 胶体与
胶体与 溶液、
溶液、 沉淀的本质区别是:
沉淀的本质区别是: 胶体具有丁达尔效应
胶体具有丁达尔效应b.不能用饱和
 溶液与浓NaOH溶液反应制备氢氧化铁胶体
溶液与浓NaOH溶液反应制备氢氧化铁胶体c.
 胶体属于纯净物,而
胶体属于纯净物,而 溶液属于混合物
溶液属于混合物
您最近一年使用:0次
解题方法
3 . 下列几种物质:①NaHCO3晶体;②Na2O2;③NaHSO4溶液;④CO2;⑤Ba(OH)2溶液;⑥C2H5OH(酒精);⑦KMnO4;⑧氨水;⑨饱和FeCl3溶液。根据要求回答下列问题:
(1)上述各物质属于电解质的是_____ (填物质编号,下同);属于非电解质的是_____ 。
(2)③中盐的电离方程式为_____ ;
(3)③和⑧在水溶液中反应的离子方程式:_____ 。
(4)将⑨加入到沸水中,继续加热溶液呈红褐色,即制得Fe(OH)3胶体,写出该反应的离子方程式:_____ 。
(1)上述各物质属于电解质的是
(2)③中盐的电离方程式为
(3)③和⑧在水溶液中反应的离子方程式:
(4)将⑨加入到沸水中,继续加热溶液呈红褐色,即制得Fe(OH)3胶体,写出该反应的离子方程式:
您最近一年使用:0次
解题方法
4 . 研究物质性质具有重要的价值,根据所学知识回答下列问题:
(1)FeCl3是黑棕色晶体,主要用于金属蚀刻,污水处理。按照物质的分类方法,FeCl3应属于___________ (填序号)。
①酸;②氯化物;③混合物;④盐;⑤化合物;⑥电解质;⑦易溶于水物质
(2)将饱和FeCl3溶液逐滴加入沸水中,继续煮沸可制取氢氧化铁胶体,氢氧化铁胶体可处理污水,该反应的化学方程式为___________ ;判断胶体制备是否成功可利用胶体的___________ ;
(3)铁元素是组成人体必不可少的元素之一,以下几种常见的铁元素粒子,既有氧化性又有还原性的是___________ 。
A.Fe B.Fe2+ C.Fe3+
(4)火药是中国的四大发明之一,永远值得华夏儿女骄傲。黑火药在发生爆炸时,发生反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。上述反应中氧化剂:___________ ;氧化产物:___________ 。
(1)FeCl3是黑棕色晶体,主要用于金属蚀刻,污水处理。按照物质的分类方法,FeCl3应属于
①酸;②氯化物;③混合物;④盐;⑤化合物;⑥电解质;⑦易溶于水物质
(2)将饱和FeCl3溶液逐滴加入沸水中,继续煮沸可制取氢氧化铁胶体,氢氧化铁胶体可处理污水,该反应的化学方程式为
(3)铁元素是组成人体必不可少的元素之一,以下几种常见的铁元素粒子,既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(4)火药是中国的四大发明之一,永远值得华夏儿女骄傲。黑火药在发生爆炸时,发生反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。上述反应中氧化剂:
您最近一年使用:0次
5 . 按要求填空:
(1)现有以下物质:①NaHCO3;②O2;③CH3COOH溶液;④Ca(OH)2;⑤蔗糖;⑥H2O;⑦NaCl;⑧CO2;⑨氨水。
i.其中能导电的是(填编号,下同):________ ;属于电解质的是________ ;属于非电解质的是:________ ;写出与②互为同素异形体的物质________ ;
ii.请写出③和⑨的离子反应方程式________________ 。
(2)实验室制备Fe(OH)3胶体的化学方程式为________________ 。
(3)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学方程式为________________ 。
(4)KA1(SO4)2•12H2O的俗名为________ ,因其溶于水生成________ (化学式)可以吸附杂质,从而达到净水作用。
(1)现有以下物质:①NaHCO3;②O2;③CH3COOH溶液;④Ca(OH)2;⑤蔗糖;⑥H2O;⑦NaCl;⑧CO2;⑨氨水。
i.其中能导电的是(填编号,下同):
ii.请写出③和⑨的离子反应方程式
(2)实验室制备Fe(OH)3胶体的化学方程式为
(3)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学方程式为
(4)KA1(SO4)2•12H2O的俗名为
您最近一年使用:0次
6 . Ⅰ.现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
①甲同学向1mol·L-1氯化铁溶液中加入少量的NaOH溶液;②乙同学直接加热饱和FeCl3溶液;③丙同学向25mL沸水中逐滴加入几滴FeCl3饱和溶液,继续煮沸至液体呈透明的红褐色,停止加热。
试回答下列问题:
(1)其中操作正确的同学是_____ 。写出此过程中的化学方程式:_____ 。
(2)证明有Fe(OH)3胶体生成的最简单的实验操作是_____ 。
(3)欲除去Fe(OH)3胶体中混有的NaCl,所用主要物品是_____ ;该操作名称是_____ 。
Ⅱ.有一瓶无色澄清溶液,其中可能含H+、Na+、Mg2+、Ba2+、Cl﹣、 、
、 离子。现进行以下实验:
离子。现进行以下实验:
A、用pH试纸检验溶液,发现溶液呈强酸性;
B、取部分溶液逐滴加入NaOH溶液,使溶液由酸性变为碱性,无沉淀产生;
C、取少量B中的碱性溶液,滴加Na2CO3溶液,有白色沉淀产生。
(4)根据上述事实确定:该溶液中肯定存在的离子有_____ ;肯定不存在的离子有_____ 。
(5)写出C中发生反应的离子方程式_____ 。
①甲同学向1mol·L-1氯化铁溶液中加入少量的NaOH溶液;②乙同学直接加热饱和FeCl3溶液;③丙同学向25mL沸水中逐滴加入几滴FeCl3饱和溶液,继续煮沸至液体呈透明的红褐色,停止加热。
试回答下列问题:
(1)其中操作正确的同学是
(2)证明有Fe(OH)3胶体生成的最简单的实验操作是
(3)欲除去Fe(OH)3胶体中混有的NaCl,所用主要物品是
Ⅱ.有一瓶无色澄清溶液,其中可能含H+、Na+、Mg2+、Ba2+、Cl﹣、
 、
、 离子。现进行以下实验:
离子。现进行以下实验:A、用pH试纸检验溶液,发现溶液呈强酸性;
B、取部分溶液逐滴加入NaOH溶液,使溶液由酸性变为碱性,无沉淀产生;
C、取少量B中的碱性溶液,滴加Na2CO3溶液,有白色沉淀产生。
(4)根据上述事实确定:该溶液中肯定存在的离子有
(5)写出C中发生反应的离子方程式
您最近一年使用:0次
解题方法
7 . I.现有下列7种物质:①二氧化硫;②稀硫酸;③铜;④氢氧化钾固体;⑤酒精(C2H5OH);⑥硝酸钾溶液;⑦氧化钠固体,请将上述物质按要求完成下列问题(用相应化学式填空):
(1)属于碱性氧化物的是______ ,属于电解质的有______ 。
Ⅱ.某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
(2)若将饱和FeCl3溶液分别滴入下列液体中,能形成胶体 是
是______ 。
(3)写出制备Fe(OH)3胶体的化学方程式:______ 。
(1)属于碱性氧化物的是
Ⅱ.某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
(2)若将饱和FeCl3溶液分别滴入下列液体中,能形成胶体
 是
是| A.冷水 | B.沸水 | C.NaOH浓溶液 | D.NaCl浓溶液 |
(3)写出制备Fe(OH)3胶体的化学方程式:
您最近一年使用:0次
8 . 现有以下几种物质(或微粒):
① 丝 ②
丝 ② ③
③ ④液态
④液态 ⑤稀
⑤稀 ⑥熔
⑥熔 ⑦
⑦ 溶液 ⑧饱和
溶液 ⑧饱和 溶液 ⑨消毒酒精
溶液 ⑨消毒酒精
回答下列问题:
(1)②和③之间互为___________ 。
(2)以上物质中属于能导电的电解质是___________ 。(填代号)
(3)⑤中溶质的电离方程式为___________ 。
(4)利用⑧制备 胶体的操作方法是
胶体的操作方法是___________ 。(用文字描述)
(5)向⑤中逐渐加入 固体,其反应的离子方程式为
固体,其反应的离子方程式为___________ 。
①
 丝 ②
丝 ② ③
③ ④液态
④液态 ⑤稀
⑤稀 ⑥熔
⑥熔 ⑦
⑦ 溶液 ⑧饱和
溶液 ⑧饱和 溶液 ⑨消毒酒精
溶液 ⑨消毒酒精回答下列问题:
(1)②和③之间互为
(2)以上物质中属于能导电的电解质是
(3)⑤中溶质的电离方程式为
(4)利用⑧制备
 胶体的操作方法是
胶体的操作方法是(5)向⑤中逐渐加入
 固体,其反应的离子方程式为
固体,其反应的离子方程式为
您最近一年使用:0次
9 . I.根据所学知识完成下列问题:
(1)按要求写出下列电离或离子方程式:
① 在水溶液中的电离方程式:
在水溶液中的电离方程式:_______ 。
②将醋酸( )溶液逐滴滴入到
)溶液逐滴滴入到 溶液中,
溶液中,刚开始 时发生的离子方程式是_______ 。
③将饱和 溶液滴入到沸水中,继续加热溶液呈红褐色,即制得
溶液滴入到沸水中,继续加热溶液呈红褐色,即制得 胶体,写出该反应离子方程式:
胶体,写出该反应离子方程式:_______ 。
(2)亚硝酸钠( )是肉制品加工中常用的发色剂。有毒,使用时必须严格控制用量。在酸性条件下,
)是肉制品加工中常用的发色剂。有毒,使用时必须严格控制用量。在酸性条件下, 可将
可将 转变为
转变为 ,自身转化为
,自身转化为 ,写出该过程的离子反应方程式为
,写出该过程的离子反应方程式为_______ 。
II.物质的量是高中化学常用的物理量,请完成以下有关计算:
(3)①某条件下,16g氧气所占的体积为12L,则在该条件下的气体摩尔体积为_______ 。
②16.25g某三价金属的氯化物中含有0.3
 ,则此氯化物的摩尔质量为
,则此氯化物的摩尔质量为_______ 。
(4)取100 0.3
0.3 和200
和200 0.2
0.2 的硫酸溶液注入500
的硫酸溶液注入500 容量瓶中,加水稀释至刻度线,该混合溶液中
容量瓶中,加水稀释至刻度线,该混合溶液中 的物质的量浓度是
的物质的量浓度是_______  。
。
(1)按要求写出下列电离或离子方程式:
①
 在水溶液中的电离方程式:
在水溶液中的电离方程式:②将醋酸(
 )溶液逐滴滴入到
)溶液逐滴滴入到 溶液中,
溶液中,③将饱和
 溶液滴入到沸水中,继续加热溶液呈红褐色,即制得
溶液滴入到沸水中,继续加热溶液呈红褐色,即制得 胶体,写出该反应离子方程式:
胶体,写出该反应离子方程式:(2)亚硝酸钠(
 )是肉制品加工中常用的发色剂。有毒,使用时必须严格控制用量。在酸性条件下,
)是肉制品加工中常用的发色剂。有毒,使用时必须严格控制用量。在酸性条件下, 可将
可将 转变为
转变为 ,自身转化为
,自身转化为 ,写出该过程的离子反应方程式为
,写出该过程的离子反应方程式为II.物质的量是高中化学常用的物理量,请完成以下有关计算:
(3)①某条件下,16g氧气所占的体积为12L,则在该条件下的气体摩尔体积为
②16.25g某三价金属的氯化物中含有0.3

 ,则此氯化物的摩尔质量为
,则此氯化物的摩尔质量为(4)取100
 0.3
0.3 和200
和200 0.2
0.2 的硫酸溶液注入500
的硫酸溶液注入500 容量瓶中,加水稀释至刻度线,该混合溶液中
容量瓶中,加水稀释至刻度线,该混合溶液中 的物质的量浓度是
的物质的量浓度是 。
。
您最近一年使用:0次
10 . 物质的分类是学习化学的一种重要方法,科学合理的分类对于系统掌握知识、提高学习效率、解决问题都有着重要的意义.请回答下列问题:
(1)纯净物根据其组成和性质有如图分类形式,这种分类方法层次分明、简洁直观.
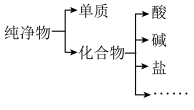
①图中所示所属的分类方法为________________ .
②现有碳、一氧化碳、二氧化碳、碳酸氢钠四种物质,采用下列分类标准,无法将其中两种物质归为一类的是________________ (填字母).
A.能和O2反应 B.属于氧化物
C.碳元素化合价相同 D.属于电解质
③实验室常根据物质分类的原则存放药品,某学校实验室其中的四个药品柜已经存放了如下部分药品,实验室新购进一些晶体碘,应该将它存放在________________ (填字母).
A.甲柜 B.乙柜 C.丙柜 D.丁柜
④“三酸(硫酸、盐酸、硝酸)”与“两碱(氢氧化钠、氢氧化钙)”能发生反应.将一定量的稀硫酸逐滴滴入氢氧化钠溶液中,此过程中发生反应的化学方程式为________________ .
(2)含铁元素的物质有很多,在生产、生活中应用广泛.取少量某油漆的原料Fe2O3(红棕色粉末),加入适量浓盐酸,反应后得到棕黄色溶液,取少量棕黄色溶液置于试管中再滴入NaOH溶液,可观察到有沉淀生成,生成沉淀的化学方程式为________________ ,另在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入2mL上述棕黄色溶液,继续加热至液体呈________ 色,停止加热,证明所得分散系类型的实验方法的名称是________________ ,化学方程式为________________ .
(1)纯净物根据其组成和性质有如图分类形式,这种分类方法层次分明、简洁直观.

①图中所示所属的分类方法为
②现有碳、一氧化碳、二氧化碳、碳酸氢钠四种物质,采用下列分类标准,无法将其中两种物质归为一类的是
A.能和O2反应 B.属于氧化物
C.碳元素化合价相同 D.属于电解质
③实验室常根据物质分类的原则存放药品,某学校实验室其中的四个药品柜已经存放了如下部分药品,实验室新购进一些晶体碘,应该将它存放在
药品柜 | 甲柜 | 乙柜 | 丙柜 | 丁柜 |
药品 | 乙醇、乙酸 | 活性炭、红磷 | 锌粒、铜片 | 氯化钠、氯化钾 |
④“三酸(硫酸、盐酸、硝酸)”与“两碱(氢氧化钠、氢氧化钙)”能发生反应.将一定量的稀硫酸逐滴滴入氢氧化钠溶液中,此过程中发生反应的化学方程式为
(2)含铁元素的物质有很多,在生产、生活中应用广泛.取少量某油漆的原料Fe2O3(红棕色粉末),加入适量浓盐酸,反应后得到棕黄色溶液,取少量棕黄色溶液置于试管中再滴入NaOH溶液,可观察到有沉淀生成,生成沉淀的化学方程式为
您最近一年使用:0次



