解题方法
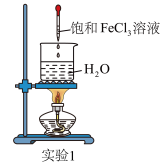
1 . 制取Fe(OH)3胶体的方案如下:向40mL沸腾的蒸馏水中滴入5滴饱和FeCl3溶液(质量分数约为30%)___________ 判断溶液中是否成功制备胶体,能产生该现象的原因是胶体粒子对光波的___________ 所致。
(2)将稀盐酸逐滴加入制得的Fe(OH)3胶体中,实验现象为___________ ,反应方程式为___________ 。
(3)制得的Fe(OH)3胶体中往往混有 和
和 ,可以利用
,可以利用___________ 的方法来提纯Fe(OH)3胶体。
(2)将稀盐酸逐滴加入制得的Fe(OH)3胶体中,实验现象为
(3)制得的Fe(OH)3胶体中往往混有
 和
和 ,可以利用
,可以利用
您最近一年使用:0次
解题方法
2 . I.某课外活动小组进行 胶体的制备实验并检验其相关性质。
胶体的制备实验并检验其相关性质。
(1)若将饱和 溶液分别滴入下列物质中,能形成胶体的是_______(填字母)。
溶液分别滴入下列物质中,能形成胶体的是_______(填字母)。
(2)写出制备 胶体的化学反应方程式:
胶体的化学反应方程式:_______ 。
(3)怎样证明制得的物质是胶体?请简述操作过程:_______ 。
Ⅱ.某兴趣小组的同学向一定体积的 ,溶液中逐滴加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图所示。
,溶液中逐滴加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图所示。 溶液与稀硫酸反应的离子方程式:
溶液与稀硫酸反应的离子方程式:_______ 。
(5)该小组的同学关于上图的下列说法中,不正确的是_______ (填序号)。
①B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子
② 段溶液的导电能力不断减弱,说明生成的
段溶液的导电能力不断减弱,说明生成的 不是电解质
不是电解质
③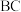 段溶液的导电能力不断增大,主要是由于过量的稀硫酸电离出的离子导电
段溶液的导电能力不断增大,主要是由于过量的稀硫酸电离出的离子导电
④a时刻 溶液与稀硫酸恰好完全中和
溶液与稀硫酸恰好完全中和
(6)氢氧化钠溶液中逐滴加入硫酸与上述导电能力随时间变化的曲线图一致吗?_______ (填“是”或“否”),请说明原因:_______ 。
 胶体的制备实验并检验其相关性质。
胶体的制备实验并检验其相关性质。(1)若将饱和
 溶液分别滴入下列物质中,能形成胶体的是_______(填字母)。
溶液分别滴入下列物质中,能形成胶体的是_______(填字母)。| A.冷水 | B.沸水 | C. 浓溶液 浓溶液 | D. 浓溶液 浓溶液 |
(2)写出制备
 胶体的化学反应方程式:
胶体的化学反应方程式:(3)怎样证明制得的物质是胶体?请简述操作过程:
Ⅱ.某兴趣小组的同学向一定体积的
 ,溶液中逐滴加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图所示。
,溶液中逐滴加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图所示。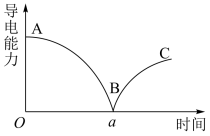
 溶液与稀硫酸反应的离子方程式:
溶液与稀硫酸反应的离子方程式:(5)该小组的同学关于上图的下列说法中,不正确的是
①B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子
②
 段溶液的导电能力不断减弱,说明生成的
段溶液的导电能力不断减弱,说明生成的 不是电解质
不是电解质③
 段溶液的导电能力不断增大,主要是由于过量的稀硫酸电离出的离子导电
段溶液的导电能力不断增大,主要是由于过量的稀硫酸电离出的离子导电④a时刻
 溶液与稀硫酸恰好完全中和
溶液与稀硫酸恰好完全中和(6)氢氧化钠溶液中逐滴加入硫酸与上述导电能力随时间变化的曲线图一致吗?
您最近一年使用:0次
解题方法
3 . 小明同学用如图所示装置制备氢氧化铁胶体(部分夹持装置已略去)。
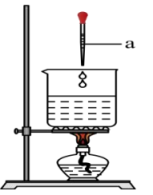
根据所学知识回答下列问题:
(1)仪器a的名称为___________ 。
(2)氢氧化铁胶体的制备:
①烧杯中发生反应的化学方程式为___________ ,反应类型为___________ (填基本反应类型)。
②证明有 胶体生成的方法是
胶体生成的方法是___________ 。(写出具体操作步骤)
③若小明同学制备出的液体呈浑浊状,则可能造成的原因是___________ (任写一种)。
(3)写出下列反应的离子方程式:
①锌和稀盐酸反应制氢气:___________ 。
②大理石和稀盐酸反应制 :
:___________ 。

根据所学知识回答下列问题:
(1)仪器a的名称为
(2)氢氧化铁胶体的制备:
①烧杯中发生反应的化学方程式为
②证明有
 胶体生成的方法是
胶体生成的方法是③若小明同学制备出的液体呈浑浊状,则可能造成的原因是
(3)写出下列反应的离子方程式:
①锌和稀盐酸反应制氢气:
②大理石和稀盐酸反应制
 :
:
您最近一年使用:0次
4 . 通过如图装置完成氢氧化铁胶体的制备及性质实验。
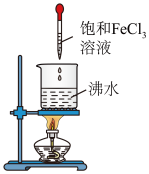
①向沸水中加入几滴饱和 溶液,继续煮沸至液体呈红褐色停止加热。
溶液,继续煮沸至液体呈红褐色停止加热。
②把盛有 溶液和
溶液和 胶体的烧杯置于暗处,用红色激光笔照射两烧杯中的液体,观察现象。
胶体的烧杯置于暗处,用红色激光笔照射两烧杯中的液体,观察现象。
(1)图中盛有饱和 溶液的仪器名称为
溶液的仪器名称为__________ 。
(2) 胶体
胶体__________ (填“能”或“不能”)透过滤纸,请写出制备 胶体的化学方程式:
胶体的化学方程式:__________ 。
(3)步骤②中能观察到的现象为__________ ,胶体产生的现象称为__________ 。分离胶体与溶液的操作名称是__________ 。
(4)若将实验改为向饱和 溶液中加入
溶液中加入 溶液,则观察到的现象为
溶液,则观察到的现象为__________ ,该反应的离子方程式为__________ 。

①向沸水中加入几滴饱和
 溶液,继续煮沸至液体呈红褐色停止加热。
溶液,继续煮沸至液体呈红褐色停止加热。②把盛有
 溶液和
溶液和 胶体的烧杯置于暗处,用红色激光笔照射两烧杯中的液体,观察现象。
胶体的烧杯置于暗处,用红色激光笔照射两烧杯中的液体,观察现象。(1)图中盛有饱和
 溶液的仪器名称为
溶液的仪器名称为(2)
 胶体
胶体 胶体的化学方程式:
胶体的化学方程式:(3)步骤②中能观察到的现象为
(4)若将实验改为向饱和
 溶液中加入
溶液中加入 溶液,则观察到的现象为
溶液,则观察到的现象为
您最近一年使用:0次
解题方法
5 . 在化学活动周中,某校兴趣小组的同学在老师指导下探究铁元素相关物质的性质。回答下列问题:
(1)实验室现有一瓶 饱和溶液,甲同学向
饱和溶液,甲同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液,煮沸至液体呈红褐色,停止加热,写出此过程中的离子方程式
饱和溶液,煮沸至液体呈红褐色,停止加热,写出此过程中的离子方程式_______ 。为了证明制得的红褐色液体属于胶体,可以使用的方法是_______ ;乙同学将少量钠单质投入氯化铁溶液中制得铁单质,请评价这一实验方案的可行性_______ (若可行,请写出发生反应的离子方程式,若不可行,请说明理由)。
(2)丙同学意图用干燥、纯净的一氧化碳还原氧化铁。实验装置如图,其中装置 是实验室用草酸
是实验室用草酸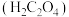 和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:
和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:
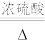
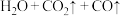 。
。
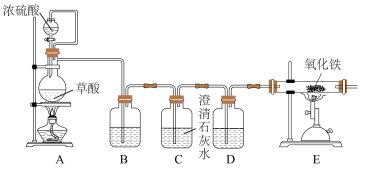
①装置B中盛放的药品为_______ ,装置D的作用为_______ 。
②在实验开始前,应先打开装置_______ (选填“A”或“E”)中的加热装置。写出装置 中发生反应的化学方程式并用双线桥法标出电子转移
中发生反应的化学方程式并用双线桥法标出电子转移_______ ,其中氧化产物与还原产物的质量比为_______ 。
③该装置的主要缺陷是_______ 。
(1)实验室现有一瓶
 饱和溶液,甲同学向
饱和溶液,甲同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液,煮沸至液体呈红褐色,停止加热,写出此过程中的离子方程式
饱和溶液,煮沸至液体呈红褐色,停止加热,写出此过程中的离子方程式(2)丙同学意图用干燥、纯净的一氧化碳还原氧化铁。实验装置如图,其中装置
 是实验室用草酸
是实验室用草酸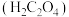 和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:
和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:
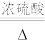
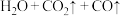 。
。
①装置B中盛放的药品为
②在实验开始前,应先打开装置
 中发生反应的化学方程式并用双线桥法标出电子转移
中发生反应的化学方程式并用双线桥法标出电子转移③该装置的主要缺陷是
您最近一年使用:0次
名校
6 . 化学是一门以实验为基础的学科。回答下列问题:
Ⅰ.影响化学平衡的因素
 溶液中存在平衡:
溶液中存在平衡: (蓝色)
(蓝色)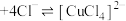 (黄色)
(黄色)
(1)取两支试管,分别加入2 mL 0.5 mol/L 溶液,溶液呈绿色,其原因为
溶液,溶液呈绿色,其原因为____________ 。
(2)将其中一支试管加热,溶液变为黄绿色,则该反应的
______ 0(填“>”或“<”),在另一支试管中加入5滴 溶液,静置,上层清液呈
溶液,静置,上层清液呈______ 色。
Ⅱ.电离平衡常数
(3) 是二元弱酸,其电离平衡常数
是二元弱酸,其电离平衡常数 的表达式为
的表达式为______ 。
(4)向盛有2 mL 1 mol/L醋酸的试管中滴加1 mol/L 溶液,观察到试管中有气泡产生,由此推断的
溶液,观察到试管中有气泡产生,由此推断的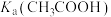
______ 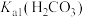 (填“>”或“<”),发生反应的离子方程式为
(填“>”或“<”),发生反应的离子方程式为____________ 。
Ⅲ.盐类水解的应用
(5)向一支试管中加入少量 晶体,然后加入5 mL蒸馏水、振荡,观察到
晶体,然后加入5 mL蒸馏水、振荡,观察到 慢慢溶解,但有少量浑浊,此溶液的pH
慢慢溶解,但有少量浑浊,此溶液的pH______ 7(填“>”“<”或“=”),配制 溶液的正确方法是
溶液的正确方法是____________ 。
(6)向一个烧杯中加入40 mL蒸馏水,加热至水沸腾,然后向沸水中逐滴加入5~6滴饱和 溶液,继续煮沸制得
溶液,继续煮沸制得 胶体。该反应的化学方程式为
胶体。该反应的化学方程式为____________ , 胶体呈
胶体呈______ 色。
Ⅳ.亚铁离子的检验
(7) 与
与______ 色的 溶液反应有特征蓝色沉淀产生,这是检验溶液中
溶液反应有特征蓝色沉淀产生,这是检验溶液中 的常用方法。写出该反应的离子方程式:
的常用方法。写出该反应的离子方程式:____________ 。
Ⅰ.影响化学平衡的因素
 溶液中存在平衡:
溶液中存在平衡: (蓝色)
(蓝色)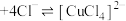 (黄色)
(黄色)
(1)取两支试管,分别加入2 mL 0.5 mol/L
 溶液,溶液呈绿色,其原因为
溶液,溶液呈绿色,其原因为(2)将其中一支试管加热,溶液变为黄绿色,则该反应的

 溶液,静置,上层清液呈
溶液,静置,上层清液呈Ⅱ.电离平衡常数
(3)
 是二元弱酸,其电离平衡常数
是二元弱酸,其电离平衡常数 的表达式为
的表达式为(4)向盛有2 mL 1 mol/L醋酸的试管中滴加1 mol/L
 溶液,观察到试管中有气泡产生,由此推断的
溶液,观察到试管中有气泡产生,由此推断的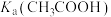
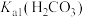 (填“>”或“<”),发生反应的离子方程式为
(填“>”或“<”),发生反应的离子方程式为Ⅲ.盐类水解的应用
(5)向一支试管中加入少量
 晶体,然后加入5 mL蒸馏水、振荡,观察到
晶体,然后加入5 mL蒸馏水、振荡,观察到 慢慢溶解,但有少量浑浊,此溶液的pH
慢慢溶解,但有少量浑浊,此溶液的pH 溶液的正确方法是
溶液的正确方法是(6)向一个烧杯中加入40 mL蒸馏水,加热至水沸腾,然后向沸水中逐滴加入5~6滴饱和
 溶液,继续煮沸制得
溶液,继续煮沸制得 胶体。该反应的化学方程式为
胶体。该反应的化学方程式为 胶体呈
胶体呈Ⅳ.亚铁离子的检验
(7)
 与
与 溶液反应有特征蓝色沉淀产生,这是检验溶液中
溶液反应有特征蓝色沉淀产生,这是检验溶液中 的常用方法。写出该反应的离子方程式:
的常用方法。写出该反应的离子方程式:
您最近一年使用:0次
2024-02-11更新
|
82次组卷
|
2卷引用:天津市南开区2023-2024学年高二上学期期末测试化学试题
7 . 氯化铁 FeCl3是一种化学常用试剂,在化学实验和工农业生产有着重要的用途。
(1)实验室常用饱和FeCl3溶液来制备Fe(OH)3胶体。
已知:在25℃时,FeCl3的溶解度为90g/100g水。
实验Ⅰ:配置20.0g饱和FeCl3溶液。
①需要用到的仪器有:药匙、托盘天平、玻璃棒、___________ 、___________ 、烧杯。
②该实验需称量FeCl3固体___________ g。
实验Ⅱ:制备Fe(OH)3胶体。
甲同学取一小烧杯,加入25mL蒸馏水,加热至沸腾,向沸水中逐滴加入1~2mL饱和氯化铁溶液,继续煮沸至液体呈红褐色,停止加热。
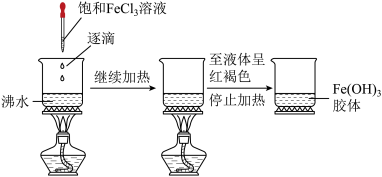
③写出此过程中的化学方程式:___________ 。
④除去氢氧化铁胶体中的氯化铁采用的方法是___________ (填写字母)。
A.过滤 B.渗析 C.蒸发
(2)工业上制印刷电路板时常用FeCl3溶液做“腐蚀液”,原理为利用FeCl3溶液将Cu溶解。某化学兴趣小组根据此原理在覆铜板上制作“化学”字样的图案。
实验Ⅲ:利用覆铜板制作图案
①写出制作过程发生反应的离子方程式:___________ 。
②使用过的“腐蚀液”会失效,但还可以回收利用,其中有一步反应需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是___________ (填序号)。
A.氯气 B.铁 C.酸性KMnO4溶液 D.稀硫酸
(1)实验室常用饱和FeCl3溶液来制备Fe(OH)3胶体。
已知:在25℃时,FeCl3的溶解度为90g/100g水。
实验Ⅰ:配置20.0g饱和FeCl3溶液。
①需要用到的仪器有:药匙、托盘天平、玻璃棒、
②该实验需称量FeCl3固体
实验Ⅱ:制备Fe(OH)3胶体。
甲同学取一小烧杯,加入25mL蒸馏水,加热至沸腾,向沸水中逐滴加入1~2mL饱和氯化铁溶液,继续煮沸至液体呈红褐色,停止加热。

③写出此过程中的化学方程式:
④除去氢氧化铁胶体中的氯化铁采用的方法是
A.过滤 B.渗析 C.蒸发
(2)工业上制印刷电路板时常用FeCl3溶液做“腐蚀液”,原理为利用FeCl3溶液将Cu溶解。某化学兴趣小组根据此原理在覆铜板上制作“化学”字样的图案。
实验Ⅲ:利用覆铜板制作图案
| 实验原理 | 利用FeCl3溶液做“腐蚀液”,将覆铜板上不需要的铜腐蚀。 |
| 实验操作 | 1.取一小块覆铜板,用油性笔在覆铜板画上设计好的“化学”图案; 2.浸入盛有FeCl3溶液的小烧杯中; 3.一段时间后,取出覆铜板并用水清洗干净; 4.观察实验现象,并展示制作的图案。  |
| 实验现象 | 用油性笔画出的图案处不被腐蚀,洗净后板上留下设计的“化学”图案。 |
| 离子方程式 | |
| 实验结论 | 铜可以被FeCl3溶液腐蚀。 |
②使用过的“腐蚀液”会失效,但还可以回收利用,其中有一步反应需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是
A.氯气 B.铁 C.酸性KMnO4溶液 D.稀硫酸
您最近一年使用:0次
解题方法
8 . 下列是制备 胶体三种方法。
胶体三种方法。
(1)实验②与实验①对比,优点是_______ ,_______ 。
(2)综合上述实验可知,制备 胶体提供
胶体提供 的物质可以是
的物质可以是 或
或_______ ,控制反应条件即可制得。
(3)实验②制备的 胶体中常含有
胶体中常含有 ,可选择下列装置中的
,可选择下列装置中的_______ 分离提纯。
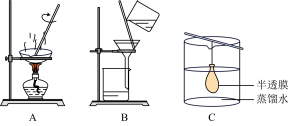
(4)向 胶体中逐滴加入稀硫酸,产生的现象依次是:①
胶体中逐滴加入稀硫酸,产生的现象依次是:①_______ ,②_______ 。
(5)用离子方程式表示现象②的原理_______ 。
(6)电解质对胶体的聚沉作用,主要是由与胶粒电性相反的离子引起的,这种离子所带电荷越多,聚沉能力越强。下列物质对 胶体聚沉能力最强的是_______。
胶体聚沉能力最强的是_______。
 胶体三种方法。
胶体三种方法。| 实验 | 实验操作 | 出现胶体 |
| ① | 向 沸腾的蒸馏水中滴入5滴饱和 沸腾的蒸馏水中滴入5滴饱和 溶液(浓度约为30%) 溶液(浓度约为30%) | 迅速出现 |
| ② | 向 蒸馏水中滴入5滴10% 蒸馏水中滴入5滴10% 溶液,然后滴入1滴10% 溶液,然后滴入1滴10% 溶液,边滴边搅拌 溶液,边滴边搅拌 | 迅速出现 |
| ③ | 加热 饱和 饱和 溶液 溶液 | 一段时间后出现 |
(1)实验②与实验①对比,优点是
(2)综合上述实验可知,制备
 胶体提供
胶体提供 的物质可以是
的物质可以是 或
或(3)实验②制备的
 胶体中常含有
胶体中常含有 ,可选择下列装置中的
,可选择下列装置中的
(4)向
 胶体中逐滴加入稀硫酸,产生的现象依次是:①
胶体中逐滴加入稀硫酸,产生的现象依次是:①(5)用离子方程式表示现象②的原理
(6)电解质对胶体的聚沉作用,主要是由与胶粒电性相反的离子引起的,这种离子所带电荷越多,聚沉能力越强。下列物质对
 胶体聚沉能力最强的是_______。
胶体聚沉能力最强的是_______。A. | B. | C. | D. |
您最近一年使用:0次
名校
解题方法
9 . 现有甲、乙、丙三名同学分别进行 胶体的制备实验。
胶体的制备实验。
①甲同学向 氯化铁溶液中加入少量的
氯化铁溶液中加入少量的 溶液;
溶液;
②乙同学直接加热饱和 溶液;
溶液;
③丙同学向 沸水中逐滴加入几滴
沸水中逐滴加入几滴 饱和溶液,继续煮沸至液体呈透明的红褐色,停止加热。
饱和溶液,继续煮沸至液体呈透明的红褐色,停止加热。
(1)其中操作正确的同学是_______ 。
(2)证明有 胶体生成的最简单的实验操作是
胶体生成的最简单的实验操作是_______ 。
(3)丁同学利用所制得的 胶体进行下列实验:
胶体进行下列实验:
①将其装入U形管内,用石墨作为电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明 胶粒带
胶粒带_______ 电荷。
②向其中加入饱和 溶液,产生的现象是
溶液,产生的现象是_______ 。
③向所得 胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为
胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为_______ ;继续滴加,沉淀最终消失且得棕黄色溶液,写出反应的化学方程式:_______ 。
④欲除去 胶体中混有的
胶体中混有的 ,该操作名称是
,该操作名称是_______ 。
 胶体的制备实验。
胶体的制备实验。①甲同学向
 氯化铁溶液中加入少量的
氯化铁溶液中加入少量的 溶液;
溶液;②乙同学直接加热饱和
 溶液;
溶液;③丙同学向
 沸水中逐滴加入几滴
沸水中逐滴加入几滴 饱和溶液,继续煮沸至液体呈透明的红褐色,停止加热。
饱和溶液,继续煮沸至液体呈透明的红褐色,停止加热。(1)其中操作正确的同学是
(2)证明有
 胶体生成的最简单的实验操作是
胶体生成的最简单的实验操作是(3)丁同学利用所制得的
 胶体进行下列实验:
胶体进行下列实验:①将其装入U形管内,用石墨作为电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明
 胶粒带
胶粒带②向其中加入饱和
 溶液,产生的现象是
溶液,产生的现象是③向所得
 胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为
胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为④欲除去
 胶体中混有的
胶体中混有的 ,该操作名称是
,该操作名称是
您最近一年使用:0次
名校
10 . Ⅰ.现有以下物质:①Ca(HCO3)2溶液;②干冰;③熔融Na2CO3;④NaOH溶液;⑤SO2;⑥Fe(OH)3胶体;⑦氨水(溶质为NH3·H2O,NH3·H2O为弱碱);⑧Na2O2固体;⑨FeCl3溶液
(1)其中在该状态下能导电且该物质为电解质的是______ (填编号,下同),属于非电解质的是______ 。
(2)请写出⑦和⑨反应的离子反应方程式______ 。
(3)⑤为酸性氧化物,写出足量④与少量⑤反应的离子方程式______ 。
Ⅱ.现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
①甲同学向稀氯化铁溶液中加入少量的NaOH溶液;
②乙同学直接加热饱和FeCl3溶液;
③丙同学向25mL沸水中逐滴加入几滴FeCl3饱和溶液,继续煮沸至液体呈透明的红褐色,停止加热。
试回答下列问题:
(4)其中操作正确的同学是______ (填甲、乙、丙)。写出此过程中的化学方程式:______ 。
(5)证明有Fe(OH)3胶体生成的最简单的实验方法是______ 。
(6)丁同学利用所制得的Fe(OH)3胶体进行下列实验:
①向所得Fe(OH)3胶体中逐滴滴加稀盐酸溶液,开始产生红褐色沉淀;继续滴加,沉淀最终消失且得棕黄色溶液,写出反应的离子方程式:______ 。
②欲除去Fe(OH)3胶体中混有的KNO3,所需要进行的操作名称是______ 。
(1)其中在该状态下能导电且该物质为电解质的是
(2)请写出⑦和⑨反应的离子反应方程式
(3)⑤为酸性氧化物,写出足量④与少量⑤反应的离子方程式
Ⅱ.现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
①甲同学向稀氯化铁溶液中加入少量的NaOH溶液;
②乙同学直接加热饱和FeCl3溶液;
③丙同学向25mL沸水中逐滴加入几滴FeCl3饱和溶液,继续煮沸至液体呈透明的红褐色,停止加热。
试回答下列问题:
(4)其中操作正确的同学是
(5)证明有Fe(OH)3胶体生成的最简单的实验方法是
(6)丁同学利用所制得的Fe(OH)3胶体进行下列实验:
①向所得Fe(OH)3胶体中逐滴滴加稀盐酸溶液,开始产生红褐色沉淀;继续滴加,沉淀最终消失且得棕黄色溶液,写出反应的离子方程式:
②欲除去Fe(OH)3胶体中混有的KNO3,所需要进行的操作名称是
您最近一年使用:0次



