1 . 下列实验操作描述正确的是
| A.制备氢氧化铁胶体实验时,用玻璃棒搅拌可加快反应速率 |
| B.进行焰色试验时如无铂丝,可以用洁净的铁丝代替 |
| C.实验剩余的药品都不可以放回原瓶 |
| D.坩埚不可以用明火直接加热 |
您最近一年使用:0次
2024-02-10更新
|
209次组卷
|
2卷引用:云南省师范大学附属中学2023-2024学年高一上学期 期末化学试卷
解题方法
2 . 化学是以实验为主的自然科学,实验操作有严格的规范。下列实验操作的描述错误的是
| A.向沸水中滴加饱和FeCl3溶液,用玻璃棒不断搅拌并继续煮沸至溶液呈透明的红褐色即可制得氢氧化铁胶体 |
| B.配制一定体积某浓度的稀硫酸,将浓硫酸稀释后立即转移入容量瓶并定容,所配溶液浓度偏大 |
| C.容量瓶检漏方法:向容量瓶中加水,塞好瓶塞,将容量瓶倒转过来,若不漏水,将容量瓶正立后,将瓶塞旋转180°,再倒转,看是否漏水 |
| D.用质量分数为98%,密度为1.84g·mL-1浓硫酸,配240mL 2mol·L-1稀硫酸,需用量筒量取浓硫酸26.1mL |
您最近一年使用:0次
3 . 生活处处有化学,化学知识无处不在。用所学知识解释工业、生产、生活与科研中的相关现象。
(1)写出H2C2O4在溶液中发生第一步电离的方程式:_______ ,写出该步电离常数的表达式Ka1=_______ 。
(2)水的离子积表达式Kw=_______ 。常温下0.01 mol/L HCl 溶液的水电离出的 c(H +)=_______ pH=11的CH3 COONa 溶液中由水电离产生的 c(OH-)=_______ 。
(3)CH3COONa溶液呈碱性的原因_______ (用离子方程式)。
(4)将饱和FeCl3的水溶液加入沸水中可以制备胶体,原因是:_______ (用离子方程式表示)。如果加热制备所得胶体,观察到颜色变化为_______ 。
(5)学过的平衡常数有化学平衡常数(K)、电离平衡常数(Ka\Kb)、水的离子积常数(Kw)、盐的水解常数(Kh),后面还会学习沉淀溶解平衡,其常数叫溶度积Ksp。其实这些常数有很多相似之处。任写一点_______ 。(符合题意的答案,均可给分)
(6)如除去MgCl2溶液中Fe3+需要的除杂试剂是_______ 。
(7)泡沫灭火器中筒体内的硫酸铝酸性溶液与碳酸氢钠碱性溶液混合发生化学反应,将生成的泡沫压出喷嘴, 喷射出去进行灭火的。写出对应的离子方程式_______ 。
(1)写出H2C2O4在溶液中发生第一步电离的方程式:
(2)水的离子积表达式Kw=
(3)CH3COONa溶液呈碱性的原因
(4)将饱和FeCl3的水溶液加入沸水中可以制备胶体,原因是:
(5)学过的平衡常数有化学平衡常数(K)、电离平衡常数(Ka\Kb)、水的离子积常数(Kw)、盐的水解常数(Kh),后面还会学习沉淀溶解平衡,其常数叫溶度积Ksp。其实这些常数有很多相似之处。任写一点
(6)如除去MgCl2溶液中Fe3+需要的除杂试剂是
(7)泡沫灭火器中筒体内的硫酸铝酸性溶液与碳酸氢钠碱性溶液混合发生化学反应,将生成的泡沫压出喷嘴, 喷射出去进行灭火的。写出对应的离子方程式
您最近一年使用:0次
4 . Ⅰ.物质性质研究是化学研究的一项重要内容,按要求回答下列问题:
有下列物质:①熔融 ;②
;② 固体;③盐酸;④
固体;③盐酸;④ ;⑤
;⑤ 溶液;⑥
溶液;⑥ ;⑦蔗糖。请用序号填空:
;⑦蔗糖。请用序号填空:
(1)上述状态下的物质可导电的是______ (填序号,下同),属于非电解质的是______ ;
(2)②属于______ (填“酸”、“碱”或“盐”),请写出②在熔融状态下的电离方程式____________ 。
(3)写出①的溶液与③反应的离子方程式____________ 。
Ⅱ.按题目要求填空:
(4)将饱和 滴入沸水中,制备氢氧化铁胶体的化学方程式:
滴入沸水中,制备氢氧化铁胶体的化学方程式:____________ ;
(5)如何除去碳酸钠固体中的碳酸氢钠,相关化学方程式为____________ ;
(6)已知 属于二元酸,请写出
属于二元酸,请写出 与过量氢氧化钠溶液反应的化学方程式为
与过量氢氧化钠溶液反应的化学方程式为____________ 。
有下列物质:①熔融
 ;②
;② 固体;③盐酸;④
固体;③盐酸;④ ;⑤
;⑤ 溶液;⑥
溶液;⑥ ;⑦蔗糖。请用序号填空:
;⑦蔗糖。请用序号填空:(1)上述状态下的物质可导电的是
(2)②属于
(3)写出①的溶液与③反应的离子方程式
Ⅱ.按题目要求填空:
(4)将饱和
 滴入沸水中,制备氢氧化铁胶体的化学方程式:
滴入沸水中,制备氢氧化铁胶体的化学方程式:(5)如何除去碳酸钠固体中的碳酸氢钠,相关化学方程式为
(6)已知
 属于二元酸,请写出
属于二元酸,请写出 与过量氢氧化钠溶液反应的化学方程式为
与过量氢氧化钠溶液反应的化学方程式为
您最近一年使用:0次
解题方法
5 . 下列方程式与所给事实不相符的是
A.服用胃舒平[主要成分是 ]可治疗胃酸过多,反应的离子方程式为: ]可治疗胃酸过多,反应的离子方程式为: |
B.用饱和 溶液和沸水制备 溶液和沸水制备 胶体的化学方程式为: 胶体的化学方程式为: |
C.金属镁着火不能用泡酒灭火器(主要成分是 )灭火的原因为: )灭火的原因为: |
D.磷酸( )是三元中强酸,其与足量的NaOH溶液反应的化学反应方程式为: )是三元中强酸,其与足量的NaOH溶液反应的化学反应方程式为: |
您最近一年使用:0次
解题方法
6 . 在化学活动周中,某校兴趣小组的同学在老师指导下探究铁元素相关物质的性质。回答下列问题:
(1)实验室现有一瓶 饱和溶液,甲同学向
饱和溶液,甲同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液,煮沸至液体呈红褐色,停止加热,写出此过程中的离子方程式
饱和溶液,煮沸至液体呈红褐色,停止加热,写出此过程中的离子方程式_______ 。为了证明制得的红褐色液体属于胶体,可以使用的方法是_______ ;乙同学将少量钠单质投入氯化铁溶液中制得铁单质,请评价这一实验方案的可行性_______ (若可行,请写出发生反应的离子方程式,若不可行,请说明理由)。
(2)丙同学意图用干燥、纯净的一氧化碳还原氧化铁。实验装置如图,其中装置 是实验室用草酸
是实验室用草酸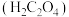 和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:
和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:
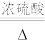
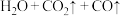 。
。
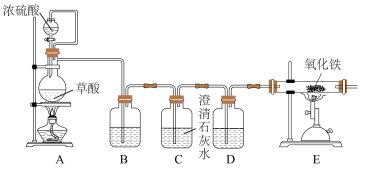
①装置B中盛放的药品为_______ ,装置D的作用为_______ 。
②在实验开始前,应先打开装置_______ (选填“A”或“E”)中的加热装置。写出装置 中发生反应的化学方程式并用双线桥法标出电子转移
中发生反应的化学方程式并用双线桥法标出电子转移_______ ,其中氧化产物与还原产物的质量比为_______ 。
③该装置的主要缺陷是_______ 。
(1)实验室现有一瓶
 饱和溶液,甲同学向
饱和溶液,甲同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液,煮沸至液体呈红褐色,停止加热,写出此过程中的离子方程式
饱和溶液,煮沸至液体呈红褐色,停止加热,写出此过程中的离子方程式(2)丙同学意图用干燥、纯净的一氧化碳还原氧化铁。实验装置如图,其中装置
 是实验室用草酸
是实验室用草酸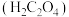 和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:
和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:
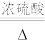
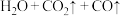 。
。
①装置B中盛放的药品为
②在实验开始前,应先打开装置
 中发生反应的化学方程式并用双线桥法标出电子转移
中发生反应的化学方程式并用双线桥法标出电子转移③该装置的主要缺陷是
您最近一年使用:0次
7 . 下列说法不正确的是
| A.激光、焰火都与电子跃迁过程中释放能量有关 |
| B.向氨水中滴入适量饱和FeCl3溶液,继续煮沸至溶液呈红褐色,然后停止加热,制备Fe(OH)3胶体 |
| C.分别向等体积的饱和的AgCl、AgBr溶液中加入足量的Na2S固体,前者产生的硫化银较多 |
| D.利用阳极氧化处理铝制品的表面,使之形成致密的氧化膜而钝化 |
您最近一年使用:0次
名校
8 . 化学是一门以实验为基础的学科。回答下列问题:
Ⅰ.影响化学平衡的因素
 溶液中存在平衡:
溶液中存在平衡: (蓝色)
(蓝色)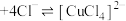 (黄色)
(黄色)
(1)取两支试管,分别加入2 mL 0.5 mol/L 溶液,溶液呈绿色,其原因为
溶液,溶液呈绿色,其原因为____________ 。
(2)将其中一支试管加热,溶液变为黄绿色,则该反应的
______ 0(填“>”或“<”),在另一支试管中加入5滴 溶液,静置,上层清液呈
溶液,静置,上层清液呈______ 色。
Ⅱ.电离平衡常数
(3) 是二元弱酸,其电离平衡常数
是二元弱酸,其电离平衡常数 的表达式为
的表达式为______ 。
(4)向盛有2 mL 1 mol/L醋酸的试管中滴加1 mol/L 溶液,观察到试管中有气泡产生,由此推断的
溶液,观察到试管中有气泡产生,由此推断的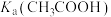
______ 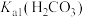 (填“>”或“<”),发生反应的离子方程式为
(填“>”或“<”),发生反应的离子方程式为____________ 。
Ⅲ.盐类水解的应用
(5)向一支试管中加入少量 晶体,然后加入5 mL蒸馏水、振荡,观察到
晶体,然后加入5 mL蒸馏水、振荡,观察到 慢慢溶解,但有少量浑浊,此溶液的pH
慢慢溶解,但有少量浑浊,此溶液的pH______ 7(填“>”“<”或“=”),配制 溶液的正确方法是
溶液的正确方法是____________ 。
(6)向一个烧杯中加入40 mL蒸馏水,加热至水沸腾,然后向沸水中逐滴加入5~6滴饱和 溶液,继续煮沸制得
溶液,继续煮沸制得 胶体。该反应的化学方程式为
胶体。该反应的化学方程式为____________ , 胶体呈
胶体呈______ 色。
Ⅳ.亚铁离子的检验
(7) 与
与______ 色的 溶液反应有特征蓝色沉淀产生,这是检验溶液中
溶液反应有特征蓝色沉淀产生,这是检验溶液中 的常用方法。写出该反应的离子方程式:
的常用方法。写出该反应的离子方程式:____________ 。
Ⅰ.影响化学平衡的因素
 溶液中存在平衡:
溶液中存在平衡: (蓝色)
(蓝色)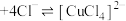 (黄色)
(黄色)
(1)取两支试管,分别加入2 mL 0.5 mol/L
 溶液,溶液呈绿色,其原因为
溶液,溶液呈绿色,其原因为(2)将其中一支试管加热,溶液变为黄绿色,则该反应的

 溶液,静置,上层清液呈
溶液,静置,上层清液呈Ⅱ.电离平衡常数
(3)
 是二元弱酸,其电离平衡常数
是二元弱酸,其电离平衡常数 的表达式为
的表达式为(4)向盛有2 mL 1 mol/L醋酸的试管中滴加1 mol/L
 溶液,观察到试管中有气泡产生,由此推断的
溶液,观察到试管中有气泡产生,由此推断的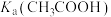
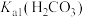 (填“>”或“<”),发生反应的离子方程式为
(填“>”或“<”),发生反应的离子方程式为Ⅲ.盐类水解的应用
(5)向一支试管中加入少量
 晶体,然后加入5 mL蒸馏水、振荡,观察到
晶体,然后加入5 mL蒸馏水、振荡,观察到 慢慢溶解,但有少量浑浊,此溶液的pH
慢慢溶解,但有少量浑浊,此溶液的pH 溶液的正确方法是
溶液的正确方法是(6)向一个烧杯中加入40 mL蒸馏水,加热至水沸腾,然后向沸水中逐滴加入5~6滴饱和
 溶液,继续煮沸制得
溶液,继续煮沸制得 胶体。该反应的化学方程式为
胶体。该反应的化学方程式为 胶体呈
胶体呈Ⅳ.亚铁离子的检验
(7)
 与
与 溶液反应有特征蓝色沉淀产生,这是检验溶液中
溶液反应有特征蓝色沉淀产生,这是检验溶液中 的常用方法。写出该反应的离子方程式:
的常用方法。写出该反应的离子方程式:
您最近一年使用:0次
2024-02-11更新
|
82次组卷
|
2卷引用:天津市南开区2023-2024学年高二上学期期末测试化学试题
9 . 下列实验的颜色变化中,与氧化还原无关的是
A.将2~3滴饱和 溶液滴入到沸腾的蒸馏水中,液体变成红褐色 溶液滴入到沸腾的蒸馏水中,液体变成红褐色 |
B.将氯气通入 溶液中,充分反应后加入 溶液中,充分反应后加入 ,振荡静置,溶液分层,下层呈紫色 ,振荡静置,溶液分层,下层呈紫色 |
C.将 气体通入酸性高锰酸钾溶液中,溶液紫色褪去 气体通入酸性高锰酸钾溶液中,溶液紫色褪去 |
D.将铁粉加入到 溶液中,溶液颜色由黄色变为浅绿色 溶液中,溶液颜色由黄色变为浅绿色 |
您最近一年使用:0次
名校
解题方法
10 . 根据下列实验设计进行操作能达到实验目的的是
| 选项 | 实验目的 | 实验设计 |
| A | 除去KNO3溶液中混有的Ca(NO3)2 | 加入过量Na2CO3溶液,过滤、洗涤,后向滤液中滴加适量稀硝酸 |
| B | 制备Fe(OH)3胶体 | 向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液 |
| C | 验证碘在浓KI溶液的溶解能力大于在CCl4中的溶解能力 | 往碘的CCl4溶液中加入等体积浓KI溶液,振荡分层,实验现象为:下层由紫红色变成浅粉红色,上层呈棕黄色 |
| D | 测定浓硫酸的pH | 用玻璃棒蘸取浓硫酸点在pH试纸上,再与标准比色卡比对 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



