名校
1 . 下表是某些短周期元素的电负性数值(鲍林标度)。
(1)根据表中数据归纳元素的电负性的变化规律。__________
(2)试推测,前四周期元素中电负性最小的元素与电负性最大的元素分别是__________ 元素,写出这两种元素形成的化合物的电子式__________ 。
(3)预测 元素电负性的范围
元素电负性的范围__________ 。
(4)一般认为,如果两种成键元素之间的电负性差值大于1.7,它们的原子之间通常形成离子键,电负性差值小于1.7通常形成共价键。请据此预测 属于离子化合物还是共价化合物
属于离子化合物还是共价化合物__________ 。
| 元素符号 |  |  | N | O | F |  |  |  | P | S |  |
| 电负性数值 | 1.0 | 1.5 | 3.0 | 3.5 | 4.0 | 0.9 | 1.2 | 1.5 | 2.1 | 2.5 | 3.0 |
(2)试推测,前四周期元素中电负性最小的元素与电负性最大的元素分别是
(3)预测
 元素电负性的范围
元素电负性的范围(4)一般认为,如果两种成键元素之间的电负性差值大于1.7,它们的原子之间通常形成离子键,电负性差值小于1.7通常形成共价键。请据此预测
 属于离子化合物还是共价化合物
属于离子化合物还是共价化合物
您最近半年使用:0次
2022-11-27更新
|
245次组卷
|
2卷引用:2019鲁科版高中化学选择性必修2第1章第3节 原子结构与元素性质课后习题
解题方法
2 . 下列选项中,所叙述的粒子按半径由大到小排列时,顺序正确的是
①基态X的原子结构示意图为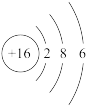
②基态Y原子的价电子排布式为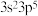
③基态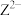 的轨道表示式为
的轨道表示式为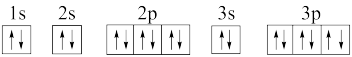
④基态T原子有2个电子层,电子式为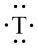
①基态X的原子结构示意图为

②基态Y原子的价电子排布式为
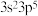
③基态
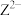 的轨道表示式为
的轨道表示式为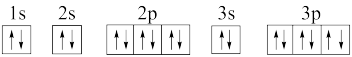
④基态T原子有2个电子层,电子式为
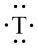
A.① ② ② ③ ③ ④ ④ | B.③ ④ ④ ① ① ② ② |
C.③ ① ① ② ② ④ ④ | D.① ② ② ④ ④ ③ ③ |
您最近半年使用:0次
2022-11-27更新
|
348次组卷
|
3卷引用:2019鲁科版高中化学选择性必修2第1章第3节 原子结构与元素性质课后习题
解题方法
3 . 部分元素的性质与原子(或分子)结构如下表:
(1)请画出T元素的原子结构示意图:___________ 。
(2)Y元素与Z元素相比,金属性较强的是_________ (用元素符号表示)。下列表述中,能证明这一事实的是__________ (填序号)。
A.Y元素的单质的熔点比Z元素的单质的低
B.Y元素的最高正化合价比Z元素的低
C.Y元素的单质与水反应比Z元素的单质与水反应剧烈
D.Y元素的最高价氧化物对应的水化物的碱性比Z元素的强
元素 | 编号元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质由双原子分子构成,1个分子中有14个电子 |
Y | M层比K层少1个电子 |
Z | 是第3周期元素的简单离子中半径最小的 |
(2)Y元素与Z元素相比,金属性较强的是
A.Y元素的单质的熔点比Z元素的单质的低
B.Y元素的最高正化合价比Z元素的低
C.Y元素的单质与水反应比Z元素的单质与水反应剧烈
D.Y元素的最高价氧化物对应的水化物的碱性比Z元素的强
您最近半年使用:0次
解题方法
4 . 已知A、B、C、D、E是短周期中的五种非金属元素,它们的原子序数依次增大。A元素的原子形成的离子核外电子数为0,B元素的原子的最外层电子数是内层电子数的2倍,C、D元素在元素周期表中处于相邻的位置,E元素与D元素处于同一主族,E元素的单质为黄色晶体。
(1)请写出元素符号:A__________ ,B__________ ,C__________ ,D__________ ,E__________ 。
(2)请画出E元素的阴离子的结构示意图:____________ 。
(3)A元素的单质和C元素的单质能在一定条件下反应生成化合物X,该反应的化学方程式为__________ 。向X的水溶液中滴入酚酞溶液,会观察到________ 。
(1)请写出元素符号:A
(2)请画出E元素的阴离子的结构示意图:
(3)A元素的单质和C元素的单质能在一定条件下反应生成化合物X,该反应的化学方程式为
您最近半年使用:0次
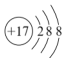
5 . 下列原子或离子的结构示意图表示的各是什么微粒?
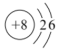
_______ ; 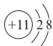
_______ ; 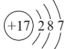
_______ ; 
_______ 。
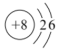
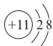
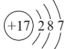

您最近半年使用:0次
解题方法
6 . 下列原子结构示意图是否正确?如有错误,指出错误的原因并改正。
F
_______ ;Na
_______ ;Mg
_______ ;Si
_______ ;S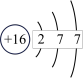
_______ 。
F





您最近半年使用:0次
7 . A、B、C、D四种元素的核电荷数依次增大,它们的离子的电子层数相同且最外层电子数均为8.A原子的L层电子数与K、M层电子数之和相等,D原子的K、L层电子数之和等于电子总数的一半。请据此回答下列问题。
(1)请写出四种元素的符号:A_______ ,B_______ ,C_______ ,D_______ 。它们的原子半径由大到小的顺序是_______ 。
(2)请画出四种元素的离子结构示意图:A_______ ,B_______ ,C_______ ,D_______ 。它们的离子半径由大到小的顺序是_______ ,请从离子结构的角度进行解释:_______ 。
(1)请写出四种元素的符号:A
(2)请画出四种元素的离子结构示意图:A
您最近半年使用:0次
解题方法
8 . 搭建乙烯分子的球棍模型,并用模型模拟乙烯与溴单质反应生成1,2-二溴乙烷的结构转变_______ 。
您最近半年使用:0次
解题方法
9 . 填表。
| 结构式 | 结构简式 | 键线式 |
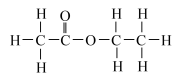 | ||
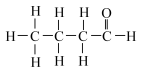 | ||
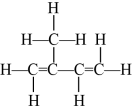 |
您最近半年使用:0次
解题方法
10 . 写出下列化合物的结构简式。
(1)三乙胺_________ 。
(2)对甲基苯胺_________ 。
(3)N,N-二甲基甲酰胺_________ 。
(4)丙烯酰胺_________ 。
(1)三乙胺
(2)对甲基苯胺
(3)N,N-二甲基甲酰胺
(4)丙烯酰胺
您最近半年使用:0次
2022-11-25更新
|
99次组卷
|
2卷引用:苏教2020版选择性必修3专题5第二单元 胺和酰胺课后习题



