名校
解题方法
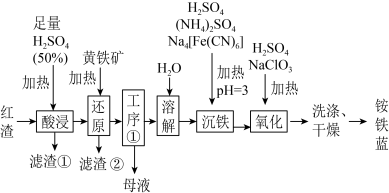
1 . 以焙烧黄铁矿FeS2(杂质为石英等)产生的红渣为原料生产制备铵铁蓝Fe(NH4)[Fe(CN)6]颜料的工艺流程如图:_______ (填化学式),滤渣①的主要成分是_______ (填化学式)。
(2)黄铁矿研细的目的是_______ 。
(3)工序①经过_______ 、过滤、洗涤得到一种含7个结晶水的晶体,该晶体为_______ (填化学式)。
(4)沉铁工序中生成一种白色沉淀为Fe(NH4)2[Fe(CN)6]。
①该物质的阴离子是由Fe2+和CN-结合形成的,CN-的电子式与氮气的电子式相似,请写出CN-的电子式:_______ 。
②该物质在酸性条件下加入NaClO3溶液,充分反应得到铵铁蓝,试补全下列离子方程式:_______ 。6Fe(NH4)2[Fe(CN)6]+ClO +_______=6FeNH4[Fe(CN)6]+ _______+_______NH
+_______=6FeNH4[Fe(CN)6]+ _______+_______NH +3H2O。
+3H2O。
(2)黄铁矿研细的目的是
(3)工序①经过
(4)沉铁工序中生成一种白色沉淀为Fe(NH4)2[Fe(CN)6]。
①该物质的阴离子是由Fe2+和CN-结合形成的,CN-的电子式与氮气的电子式相似,请写出CN-的电子式:
②该物质在酸性条件下加入NaClO3溶液,充分反应得到铵铁蓝,试补全下列离子方程式:
 +_______=6FeNH4[Fe(CN)6]+ _______+_______NH
+_______=6FeNH4[Fe(CN)6]+ _______+_______NH +3H2O。
+3H2O。
您最近一年使用:0次
2024-03-01更新
|
85次组卷
|
2卷引用:山西省运城市康杰中学2023-2024学年高一下学期化学试题
名校
解题方法
2 . LiNiO2是一种应用广泛的电动汽车电极材料,以铁镍合金的废角料(含少量铜)为原料,生产电极材料LiNiO2的部分工艺流程如下:

已知:①表中列出了几种金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L-1计算)。
② ;
;
回答下列问题:
(1)“酸溶”时温度要控制在70~80℃,温度不宜过低和过高,其原因是___________ ;为提高“酸溶”的速率,可采取的措施___________ (写出一种)。
(2)H2O2的电子式为___________ ;“氧化”时加入H2O2的目的是(用离子方程式表示)___________ 。
(3)加入NaOH的目的是通过调pH使Fe3+沉淀,其pH的范围是___________ 。
(4)“除铜”时若选用NaOH,会导致部分Ni2+也产生沉淀,当溶液中Ni(OH)2、Cu(OH)2沉淀同时存在时,溶液中c(Ni2+):c(Cu2+)=___________ 。
(5)“沉镍”时可用碳酸氢钠代替碳酸钠得到碳酸镍(NiCO3)沉淀,写出该反应的离子方程式___________ 。

已知:①表中列出了几种金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L-1计算)。
| 开始沉淀的pH | 沉淀完全的pH | |
| Ni2+ | 6.7 | 9.5 |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
 ;
;
回答下列问题:
(1)“酸溶”时温度要控制在70~80℃,温度不宜过低和过高,其原因是
(2)H2O2的电子式为
(3)加入NaOH的目的是通过调pH使Fe3+沉淀,其pH的范围是
(4)“除铜”时若选用NaOH,会导致部分Ni2+也产生沉淀,当溶液中Ni(OH)2、Cu(OH)2沉淀同时存在时,溶液中c(Ni2+):c(Cu2+)=
(5)“沉镍”时可用碳酸氢钠代替碳酸钠得到碳酸镍(NiCO3)沉淀,写出该反应的离子方程式
您最近一年使用:0次



