名校
1 . 某兴趣小组在化学实验室找到了敞口放置较长时间的市售漂白粉,包装袋上标明其成分为CaCl2和Ca(ClO)2,有效成分含量为40%。已知Ca(ClO)2在空气中易变质为CaCO3,为探究漂白粉的变质情况,小组成员小昕用电子天平称取了1.887g的固体,向其中加入足量稀硝酸,把生成的气体全部通入:250mL 的澄清石灰水中使之充分反应,将所得沉淀过滤,洗涤,烘干之后,称量得到其质量为0.400g。小昕通过计算得出结论,此时的漂白粉中必定存在部分未变质的Ca(ClO)2。
的澄清石灰水中使之充分反应,将所得沉淀过滤,洗涤,烘干之后,称量得到其质量为0.400g。小昕通过计算得出结论,此时的漂白粉中必定存在部分未变质的Ca(ClO)2。
(1)你认为小昕的说法正确吗?___________ 。并说明理由___________ 。
(2)书写S原子的结构示意图:___________ 。
(3)乔同学和樊同学想用84消毒液杀死真菌,为了提高效果,乔同学向“84”中加入了洁厕灵(主要成分为HCl),结果导致两人双双中毒紧急送进医院,请写出相关方程式___________ 。
(4)在石灰窑中烧制生石灰,lmolCaCO3完全分解所需要的能量,可燃烧0.453mol碳来提供。设空气中O2体积分数为0.21,N2为0.79,则石灰窑产生的气体中CO2的体积分数最大值是___________ 。
(5)某固体仅由一种元素组成,其密度为: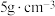 ,用X射线研究该固体的结果表明:在边长为
,用X射线研究该固体的结果表明:在边长为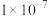 cm的立方体中含有20个原子,则此元素的相对原子质量约为
cm的立方体中含有20个原子,则此元素的相对原子质量约为___________ (取整数)。
 的澄清石灰水中使之充分反应,将所得沉淀过滤,洗涤,烘干之后,称量得到其质量为0.400g。小昕通过计算得出结论,此时的漂白粉中必定存在部分未变质的Ca(ClO)2。
的澄清石灰水中使之充分反应,将所得沉淀过滤,洗涤,烘干之后,称量得到其质量为0.400g。小昕通过计算得出结论,此时的漂白粉中必定存在部分未变质的Ca(ClO)2。(1)你认为小昕的说法正确吗?
(2)书写S原子的结构示意图:
(3)乔同学和樊同学想用84消毒液杀死真菌,为了提高效果,乔同学向“84”中加入了洁厕灵(主要成分为HCl),结果导致两人双双中毒紧急送进医院,请写出相关方程式
(4)在石灰窑中烧制生石灰,lmolCaCO3完全分解所需要的能量,可燃烧0.453mol碳来提供。设空气中O2体积分数为0.21,N2为0.79,则石灰窑产生的气体中CO2的体积分数最大值是
(5)某固体仅由一种元素组成,其密度为:
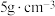 ,用X射线研究该固体的结果表明:在边长为
,用X射线研究该固体的结果表明:在边长为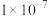 cm的立方体中含有20个原子,则此元素的相对原子质量约为
cm的立方体中含有20个原子,则此元素的相对原子质量约为
您最近一年使用:0次
名校
解题方法
2 . 现有2molCH4,它的摩尔质量是_______ ,这些CH4完全燃烧,需消耗氧气________ g。
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
3 . 白玉的化学式可用CaxMgySipO22(OH)2表示(也可用Ca、Mg、Si、H的氧化物表示)。取8.10g白玉粉末灼烧至恒重,固体减少了0.18g,则白玉的摩尔质量为_______ 。
您最近一年使用:0次
4 . 请计算:
(1)10.6克Na2CO3的物质的量是多少?_______
(2)2.5 mol NaOH的质量是多少?_______
(1)10.6克Na2CO3的物质的量是多少?
(2)2.5 mol NaOH的质量是多少?
您最近一年使用:0次
5 . 回答下列问题
(1)1.5molH2SO4的质量是_______ ,其中含有_______ molH,含有_______ g氧。
(2)4.4gCO2的物质的量是_______ ,其中含有二氧化碳分子_______ 个,电子_______ 个,它在标况下占有的体积为_______ 。
(3)等质量的HCl、NH3、CO2、O2四种气体,在相同温度和相同压强条件下,体积最大的是_______ 。
(4)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为_______ ,R的相对原子质量为_______ 。
(5)实验室需要0.1mol/L的氢氧化钠溶液100mL,其中需要2mol/L的氢氧化钠溶液_______ mL,将71 g Na2SO4溶于水配成1 L溶液,该溶液中Na2 SO4的物质的量浓度为_______ ,溶液中Na+的物质的量浓度为_______
(1)1.5molH2SO4的质量是
(2)4.4gCO2的物质的量是
(3)等质量的HCl、NH3、CO2、O2四种气体,在相同温度和相同压强条件下,体积最大的是
(4)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为
(5)实验室需要0.1mol/L的氢氧化钠溶液100mL,其中需要2mol/L的氢氧化钠溶液
您最近一年使用:0次
6 . 回答下列问题:
(1)Mg2+的摩尔质量是_________________ 。
(2)0.5molH2O中含有________ 个水分子,含有________ mol电子。
(3)3.01×1023 个CO2分子中含有氧原子的个数为________ ;CO2气体的质量为___________ g。
(4)标准状况下,92gNO2气体含有的原子数为_________________ ;体积为________ L。
(1)Mg2+的摩尔质量是
(2)0.5molH2O中含有
(3)3.01×1023 个CO2分子中含有氧原子的个数为
(4)标准状况下,92gNO2气体含有的原子数为
您最近一年使用:0次
7 . 回答下列问题
(1)32 g SO2标况下的体积为_______ L,含有_______ 个氧原子。
(2)1.204×1024个CO2分子的摩尔质量是_______ 。
(3)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为_______ ,R的相对原子质量为_______ 。
(4)1.204×1024个NH3分子所含的氢原子数与_______ mol CH4含有的氢原子数相同。
(1)32 g SO2标况下的体积为
(2)1.204×1024个CO2分子的摩尔质量是
(3)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为
(4)1.204×1024个NH3分子所含的氢原子数与
您最近一年使用:0次
8 . 计算下列物质的摩尔质量。
(1)已知氨气的相对分子质量为17,则氨气的摩尔质量为_______ 。
(2)1.28 g某气体含有的分子数目为1.204×1022,则该气体的摩尔质量为_______ 。
(3)已知一个铁原子的质量为b g,则铁的摩尔质量为_______ 。
(4)NA为阿伏加德罗常数,已知a g某气体中含分子数为b,则该气体的摩尔质量为_______ 。
(1)已知氨气的相对分子质量为17,则氨气的摩尔质量为
(2)1.28 g某气体含有的分子数目为1.204×1022,则该气体的摩尔质量为
(3)已知一个铁原子的质量为b g,则铁的摩尔质量为
(4)NA为阿伏加德罗常数,已知a g某气体中含分子数为b,则该气体的摩尔质量为
您最近一年使用:0次
9 . (1)0.2molNH3的质量为_______ g
(2)配制250mL1.0mol/LH2SO4溶液,需要18mol/LH2SO4溶液体积是___ 。
(3)我国古代四大发明之一的黑火药是由硫粉、硝酸钾和木炭按一定比例混合而成,爆炸时的反应为S+2KNO3+3C=K2S+N2↑+3CO2↑,反应中被还原的物质是____ (填化学式);1mol硫参加反应时转移电子数为_____ 。
(4)已知NH3和Cl2可以发生氧化还原反应,配平该方程式:NH3+Cl2=N2+HCl,_______ 。
(2)配制250mL1.0mol/LH2SO4溶液,需要18mol/LH2SO4溶液体积是
(3)我国古代四大发明之一的黑火药是由硫粉、硝酸钾和木炭按一定比例混合而成,爆炸时的反应为S+2KNO3+3C=K2S+N2↑+3CO2↑,反应中被还原的物质是
(4)已知NH3和Cl2可以发生氧化还原反应,配平该方程式:NH3+Cl2=N2+HCl,
您最近一年使用:0次
名校
10 . (1)9g水与_______ g硫酸所含的分子数相等,它们所含氧原子数之比是_______ ,氢原子数之比是_______ ;
(2)已知8gA能与32gB恰好完全反应,生成22gC和一定量的D,现将16gA与70gB的混合物充分反应后,生成2molD和一定量的C,则D的摩尔质量是_______ g/mol;
(2)已知8gA能与32gB恰好完全反应,生成22gC和一定量的D,现将16gA与70gB的混合物充分反应后,生成2molD和一定量的C,则D的摩尔质量是
您最近一年使用:0次



