解题方法
1 . 填空题。
(1)有下列七种物质:①石灰水②KOH③稀硫酸④液氯⑤蔗糖⑥CuSO4•5H2O⑦SO2。其中属于氧化物的是_______ (填序号,下同);属于混合物的是_______ ;属于电解质的是_______ ;属于非电解质的是_______ 。
(2)3.4克NH3中所含氢原子数目与标准状况下约______ LH2S所含氢原子数目相等。
(3)15.6gNa2X中含有Na+0.4mol,则X的摩尔质量为_______ 。
(4)标准状态下,672mL某气体质量为1.92g,该气体的摩尔质量为_______ 。
(5)同温同压下,同质量的甲烷(CH4)和氨气物质的量之比为_______ ;氢原子总数之比为_______ ;体积之比为_______ ;密度之比为_______ 。
(1)有下列七种物质:①石灰水②KOH③稀硫酸④液氯⑤蔗糖⑥CuSO4•5H2O⑦SO2。其中属于氧化物的是
(2)3.4克NH3中所含氢原子数目与标准状况下约
(3)15.6gNa2X中含有Na+0.4mol,则X的摩尔质量为
(4)标准状态下,672mL某气体质量为1.92g,该气体的摩尔质量为
(5)同温同压下,同质量的甲烷(CH4)和氨气物质的量之比为
您最近一年使用:0次
名校
2 . 回答下列问题
(1)在标准状况下,①14g氮气 ②44.8L CO ③9.03×1023个NH3分子,含原子数最多的是(填序号,下同)_______ ,质量最大的是_______ ,体积最小的是_______ 。
(2)同温同压下,质量相同的CO和CH4气体的体积之比为_______ 。
(3)用足量BaCl2溶液分别与相同体积的硫酸铝、硫酸锌和硫酸钠三种溶液充分反应,生成BaSO4沉淀的质量相等,则三种溶液中溶质的物质的量浓度之比依次是_______ 。
(1)在标准状况下,①14g氮气 ②44.8L CO ③9.03×1023个NH3分子,含原子数最多的是(填序号,下同)
(2)同温同压下,质量相同的CO和CH4气体的体积之比为
(3)用足量BaCl2溶液分别与相同体积的硫酸铝、硫酸锌和硫酸钠三种溶液充分反应,生成BaSO4沉淀的质量相等,则三种溶液中溶质的物质的量浓度之比依次是
您最近一年使用:0次
名校
解题方法
3 .
(1)标准状况下,相对分子质量为M的某气体密度为______ g·L-1;
(2)15克A与10.5克B恰好完全反应,生成7.2克C、1.8克D和0.3 mol E,则E的摩尔质量是______ ;
(3)在标准状况下,若ag气体X与bg气体Y的分子数相同,则X和Y的密度比为______ ;则1g气体X和1g气体Y的体积之比是______ 。
(1)标准状况下,相对分子质量为M的某气体密度为
(2)15克A与10.5克B恰好完全反应,生成7.2克C、1.8克D和0.3 mol E,则E的摩尔质量是
(3)在标准状况下,若ag气体X与bg气体Y的分子数相同,则X和Y的密度比为
您最近一年使用:0次
4 . 物质的量在计算中有广泛的应用,请完成下列各小题:
(1)40.5g金属氯化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为___________ ;
(2)由CO、CO2两气体组成的混合气体12.8g,标准状况下体积为8.96L,则CO、CO2的物质的量之比为___________ ;
(3)甲、乙两烧杯中分别盛有200mL浓度均为2mol/L的HCl溶液与NaOH溶液,向两烧杯中分别加入等质量的Al,反应结束后测得同温同压下生成气体的体积之比为2:5,加入Al的质量为___________ ;(保留两位有效数字)
(4)室温下,某容积固定的密闭容器由可移动的挡板(厚度可忽略)隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示。

①A室混合气体的物质的量为___________ ;
②实验测得A室混合气体的质量为34g,若将A室H2、O2的混合气体点燃,恢复原温度后,最终挡板停留的位置在___________ 刻度,容器内气体压强与反应前气体压强之比为___________ 。
(1)40.5g金属氯化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为
(2)由CO、CO2两气体组成的混合气体12.8g,标准状况下体积为8.96L,则CO、CO2的物质的量之比为
(3)甲、乙两烧杯中分别盛有200mL浓度均为2mol/L的HCl溶液与NaOH溶液,向两烧杯中分别加入等质量的Al,反应结束后测得同温同压下生成气体的体积之比为2:5,加入Al的质量为
(4)室温下,某容积固定的密闭容器由可移动的挡板(厚度可忽略)隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示。

①A室混合气体的物质的量为
②实验测得A室混合气体的质量为34g,若将A室H2、O2的混合气体点燃,恢复原温度后,最终挡板停留的位置在
您最近一年使用:0次
名校
解题方法
5 . 化学计量在化学中占有重要地位。请回答下列问题:
(1)青蒿素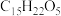 的摩尔质量为
的摩尔质量为___________ 。
(2)___________ 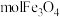 中含有
中含有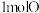 ,含有
,含有___________ 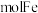 。
。
(3)在标准状况下, 由
由 和
和 组成的混合气体中,含有的分子总数约为
组成的混合气体中,含有的分子总数约为___________ 。
(4)在标准状况下,含有 个氦原子的氦气的体积约为
个氦原子的氦气的体积约为___________ 。
(5)某消毒小组人员用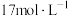 的浓硫酸配制
的浓硫酸配制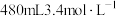 的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为
的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为___________  ;所配溶液中的
;所配溶液中的 的物质的量浓度为
的物质的量浓度为___________ 。
(6)如图所示,气缸的总体积一定,内部被活塞隔成I、II两部分,活塞可以自由移动,也可以固定。 时向I中充入
时向I中充入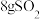 ,II中充入
,II中充入
 ,则当活塞不再移动时,I、II两部分体积比为
,则当活塞不再移动时,I、II两部分体积比为___________ 。

(1)青蒿素
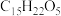 的摩尔质量为
的摩尔质量为(2)
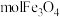 中含有
中含有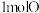 ,含有
,含有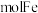 。
。(3)在标准状况下,
 由
由 和
和 组成的混合气体中,含有的分子总数约为
组成的混合气体中,含有的分子总数约为(4)在标准状况下,含有
 个氦原子的氦气的体积约为
个氦原子的氦气的体积约为(5)某消毒小组人员用
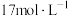 的浓硫酸配制
的浓硫酸配制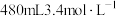 的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为
的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为 ;所配溶液中的
;所配溶液中的 的物质的量浓度为
的物质的量浓度为(6)如图所示,气缸的总体积一定,内部被活塞隔成I、II两部分,活塞可以自由移动,也可以固定。
 时向I中充入
时向I中充入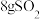 ,II中充入
,II中充入
 ,则当活塞不再移动时,I、II两部分体积比为
,则当活塞不再移动时,I、II两部分体积比为
您最近一年使用:0次
2023-12-23更新
|
53次组卷
|
2卷引用:甘肃省永昌县第一高级中学2023-2024学年高一上学期期中考试化学试题
名校
6 . 填空
(1)标准状况下有①44.8LCH4,② 个NH3分子,③85gH2S三种气体,这三种气体的物质的量从大到小的顺序是
个NH3分子,③85gH2S三种气体,这三种气体的物质的量从大到小的顺序是______ 。
(2)40.5g某金属氯化物MCl2中含有0.6molCl-,则M的相对原子质量为______ 。
(3)amLAl2(SO4)3溶液中含 bg,则溶液中Al3+的物质的量浓度
bg,则溶液中Al3+的物质的量浓度______ 。
(4)将一定量的CO2和SO2混合,测得混合气体中碳元素和硫元素的质量之比为3∶8,则该混合气体中CO2与SO2的物质的量之比为______ ,该混合气体的密度是同温同压下氢气密度的______ 倍。
(5)把VL含有MgSO4与K2SO4的混合溶液分成两等份,一份加入含amolNaOH的溶液,恰好使镁离子完全沉淀为Mg(OH)2;另一份加入含bmolBaCl2的溶液,恰好使 完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为
完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为______ 。
(1)标准状况下有①44.8LCH4,②
 个NH3分子,③85gH2S三种气体,这三种气体的物质的量从大到小的顺序是
个NH3分子,③85gH2S三种气体,这三种气体的物质的量从大到小的顺序是(2)40.5g某金属氯化物MCl2中含有0.6molCl-,则M的相对原子质量为
(3)amLAl2(SO4)3溶液中含
 bg,则溶液中Al3+的物质的量浓度
bg,则溶液中Al3+的物质的量浓度(4)将一定量的CO2和SO2混合,测得混合气体中碳元素和硫元素的质量之比为3∶8,则该混合气体中CO2与SO2的物质的量之比为
(5)把VL含有MgSO4与K2SO4的混合溶液分成两等份,一份加入含amolNaOH的溶液,恰好使镁离子完全沉淀为Mg(OH)2;另一份加入含bmolBaCl2的溶液,恰好使
 完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为
完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为
您最近一年使用:0次
2023-12-19更新
|
110次组卷
|
2卷引用:黑龙江省齐齐哈尔市第八中学校2023-2024学年高一上学期12月月考化学试题
解题方法
7 . NA为阿伏加德罗常数,如需要用NA表示:
(1)1.204×1024个 的物质的量为
的物质的量为___________ ,含有的电子数为___________ ;
(2)同温同压下,体积相同的HCl、NH3、CO2气体中,质量最大的是___________ 。
(1)1.204×1024个
 的物质的量为
的物质的量为(2)同温同压下,体积相同的HCl、NH3、CO2气体中,质量最大的是
您最近一年使用:0次
名校
解题方法
8 . 物质的量是宏观量与微观量相互联系的桥梁,回答下列问题。
(1)等质量的 和
和 所含分子个数比为
所含分子个数比为___________ ;常温常压下,等体积的 和
和 两种气体所含原子个数比为
两种气体所含原子个数比为___________ ,质量比为___________ 。
(2)将6L标准状况下的氯化氢气体溶于100mL水中(水的密度近似为 ),得到密度为
),得到密度为 的盐酸,则该盐酸的物质的量浓度是
的盐酸,则该盐酸的物质的量浓度是___________  (列出计算式)。
(列出计算式)。
(3)铜有两种常见的氧化物CuO和 。某学习小组用电子天平称取
。某学习小组用电子天平称取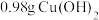 固体,加热至
固体,加热至 完全分解成铜的氧化物,其质量随温度的变化如图所示,计算N点各成分的质量:CuO
完全分解成铜的氧化物,其质量随温度的变化如图所示,计算N点各成分的质量:CuO___________ g,
___________ g。

(1)等质量的
 和
和 所含分子个数比为
所含分子个数比为 和
和 两种气体所含原子个数比为
两种气体所含原子个数比为(2)将6L标准状况下的氯化氢气体溶于100mL水中(水的密度近似为
 ),得到密度为
),得到密度为 的盐酸,则该盐酸的物质的量浓度是
的盐酸,则该盐酸的物质的量浓度是 (列出计算式)。
(列出计算式)。(3)铜有两种常见的氧化物CuO和
 。某学习小组用电子天平称取
。某学习小组用电子天平称取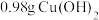 固体,加热至
固体,加热至 完全分解成铜的氧化物,其质量随温度的变化如图所示,计算N点各成分的质量:CuO
完全分解成铜的氧化物,其质量随温度的变化如图所示,计算N点各成分的质量:CuO

您最近一年使用:0次
名校
解题方法
9 . 物质的量是一个联系宏观和微观的重要物理量。请回答下列有关问题。
(1)同温同压下,A2气体与B2气体化合,生成AxBy气体,已知反应前后气体的密度不变,则AxBy的分子式为___________ 。
(2)已知 的电子数为a,M的质量数为A,则2 mol的M的中子数为
的电子数为a,M的质量数为A,则2 mol的M的中子数为___________ 。
(3)质量之比为16∶7∶6的三种气体SO2、CO、NO。分子个数之比为___________ ;氧原子个数之比为___________ ;相同条件下的体积之比为___________ 。
(4)稀硫酸与铝恰好完全反应,所得V mL Al2(SO4)3溶液中含有m g Al3+,则该溶液中 物质的量浓度为
物质的量浓度为___________ mol·L-1。
(5)标准状况下,将体积比为9∶1∶4的H2、Cl2、O2在密闭容器中用电火花点燃充分反应,恢复到原状态后,形成溶液的质量分数为___________ 。(保留三位小数)
(1)同温同压下,A2气体与B2气体化合,生成AxBy气体,已知反应前后气体的密度不变,则AxBy的分子式为
(2)已知
 的电子数为a,M的质量数为A,则2 mol的M的中子数为
的电子数为a,M的质量数为A,则2 mol的M的中子数为(3)质量之比为16∶7∶6的三种气体SO2、CO、NO。分子个数之比为
(4)稀硫酸与铝恰好完全反应,所得V mL Al2(SO4)3溶液中含有m g Al3+,则该溶液中
 物质的量浓度为
物质的量浓度为(5)标准状况下,将体积比为9∶1∶4的H2、Cl2、O2在密闭容器中用电火花点燃充分反应,恢复到原状态后,形成溶液的质量分数为
您最近一年使用:0次
10 . 物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积______ 。
(2)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则R的相对原子质量为______ 。
(3)标准状况下,1.7gNH3与______ LH2S气体含有的氢原子数相同,
(4)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L该混合气体中NH3的体积分数为______ ,该混合气体对氢气的相对密度为______ 。
(1)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积
(2)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则R的相对原子质量为
(3)标准状况下,1.7gNH3与
(4)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L该混合气体中NH3的体积分数为
您最近一年使用:0次



