名校
1 . 设 为阿伏加德罗常数的值,下列说法中正确的是
为阿伏加德罗常数的值,下列说法中正确的是
 为阿伏加德罗常数的值,下列说法中正确的是
为阿伏加德罗常数的值,下列说法中正确的是A. 和 和 的固体混合物中含 的固体混合物中含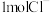 ,则混合物中质子数为 ,则混合物中质子数为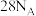 |
B.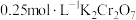 溶液中含有的 溶液中含有的 的数目为 的数目为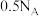 |
C.一定条件下, 与 与 充分反应,转移的电子数为 充分反应,转移的电子数为 |
D.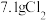 溶于水,所得溶液中 溶于水,所得溶液中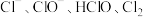 的粒子数之和为 的粒子数之和为 |
您最近一年使用:0次
2024-03-01更新
|
101次组卷
|
2卷引用:山东省济宁市第一中学2023-2024学年高一下学期开学考试化学试题
2 . 设NA为阿伏加德罗常数的数值,下列说法正确的是
A.常温下,44gCO2含有NA个 原子 原子 |
| B.1L0.1mol•L-1Na2SO4溶液中含有0.1NA个Na+ |
| C.0.1molNa与足量Cl2反应,转移0.2NA个电子 |
| D.标准状况下,22.4L的H2O含有3NA个原子 |
您最近一年使用:0次
2024-03-01更新
|
62次组卷
|
2卷引用:北京九中2023-2024学年高一下学期开学测试化学试题
名校
3 . 用  表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是
A. 含有的原子数为 含有的原子数为  |
B.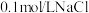 溶液含有 溶液含有  个数为 个数为  |
C.标准状况下, 和 和  的混合气体 的混合气体  含有的分子数为 含有的分子数为  |
D. 与 与 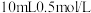 盐酸充分反应,转移电子数为 盐酸充分反应,转移电子数为  |
您最近一年使用:0次
2024-02-19更新
|
166次组卷
|
3卷引用:安徽省宿州市泗县第一中学2023-2024学年高一下学期开学考试化学试题
名校
4 . 用 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A. 的 的 溶液中 溶液中 数目为 数目为 |
B.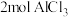 完全与水反应生成的 完全与水反应生成的 胶体粒子数目为 胶体粒子数目为 |
C.由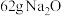 与 与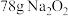 组成的混合物中阴离子总数为 组成的混合物中阴离子总数为 |
D.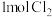 与足量Fe充分反应,转移 与足量Fe充分反应,转移 个电子 个电子 |
您最近一年使用:0次
2024-01-25更新
|
95次组卷
|
3卷引用:吉林省通化市梅河口市第五中学2023-2024学年高一下学期开学化学试题
5 . 设NA为阿伏加德罗常数,下列叙述中正确的是
| A.标准状况下,22.4L水中含分子数为NA |
| B.1molNa2O2中含有的离子数目为4NA |
| C.常温下64gS4和S8混合物中含有原子数为2NA |
| D.56gFe与足量氯气反应,转移的电子数为2NA |
您最近一年使用:0次
2024-01-20更新
|
56次组卷
|
2卷引用:安徽省桐城中学2023-2024学年高一下学期开学检测化学试题
6 . NA为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,11.2LCO2中含有原子的数目为 |
B.等体积、等物质的量浓度的NaCl和KCl溶液中,阴、阳离子数目之和均为 |
| C.71gCl2与足量的铁完全反应生成FeCl3时,反应转移的电子数为2NA |
| D.常温常压下,48gO2和O3的混合气体含有的氧原子数大于1.5NA小于3NA |
您最近一年使用:0次
2024-01-18更新
|
240次组卷
|
4卷引用:河南省信阳高级中学2023-2024学年高一下学期开学化学试题
7 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.lmolSO2与足量的O2反应,转移电子的数目为2NA |
| B.某浓硝酸中n(HNO3)=2mol,与足量的铜完全反应可生成1molNO2 |
C.常温常压下,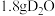 中含有质子的数目为 中含有质子的数目为 |
| D.标准状况下,2.24LSO3含氧原子约为3NA |
您最近一年使用:0次
名校
8 . 设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A. 与 与 反应每产生 反应每产生 ,转移的电子数小于 ,转移的电子数小于 |
B.含 的浓硫酸与足量的镁反应,转移的电子数大于 的浓硫酸与足量的镁反应,转移的电子数大于 |
C.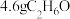 完全燃烧,可能有 完全燃烧,可能有 个 个 键断裂 键断裂 |
D. 受热熔融时电离得到的离子数目为 受热熔融时电离得到的离子数目为 |
您最近一年使用:0次
2024-01-08更新
|
258次组卷
|
3卷引用:云南省昭通市第一中学2023-2024学年高二下学期开学考试化学试题
名校
9 . NA表示阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,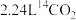 含中子数为 含中子数为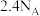 |
B.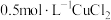 溶液中含有的Cl⁻个数为NA 溶液中含有的Cl⁻个数为NA |
| C.电解精炼铜时,阳极质量减少64g,转移电子数为2NA |
D.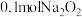 与足量水反应时转移的电子数为0.2NA 与足量水反应时转移的电子数为0.2NA |
您最近一年使用:0次
2023-12-26更新
|
206次组卷
|
2卷引用:四川省遂宁市射洪市四川省射洪中学校2023-2024学年高三下学期开学理综试题-高中化学
名校
解题方法
10 . 铋(Bi)的化合物广泛应用于电子、医药等领域。由辉铋矿(主要成分为Bi2S3,含FeS2、CuO、SiO2等杂质)制备NaBiO3的工艺流程如下:

已知:
i.Bi3易水解。NaBiO3难溶于冷水。
ii.“氧化浸取”时,铋元素转化为Bi3,硫元素转化为硫单质。
iii.Cu(OH)2(s)+4NH3(g) Cu[(NH3)4]2-(aq)+2OH-(aq) K=4.4×10-7
Cu[(NH3)4]2-(aq)+2OH-(aq) K=4.4×10-7
回答下列问题:
(1)为提高“浸取”速率,采取的措施有:升高温度、_____ (写出一条)。辉铋矿浸取率随温度的变化曲线如图,高于40℃时浸取率快速下降,其可能的原因是_____ 。

(2)“氧化浸取”时,H2O2和FeS2发生反应的物质的量之比为_____ 。
(3)“除铜”时发生反应:Cu2+(aq)+4NH3(g) Cu[(NH3)4]2-(aq) K=2×1013,则Ksp[Cu(OH)2]=
Cu[(NH3)4]2-(aq) K=2×1013,则Ksp[Cu(OH)2]=_____ 。
(4)“转化”时,生成NaBiO3的离子方程式为_____ 。
(5)已知酸性环境下,NaBiO3的可以将 氧化成
氧化成 (
(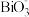 被还原成
被还原成 )
)
取NaBiO3产品wg,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用amol·L1H2C2O4标准溶液滴定生成的 ,当溶液紫红色恰好褪去时,消耗bmL标准溶液。该产品的纯度为
,当溶液紫红色恰好褪去时,消耗bmL标准溶液。该产品的纯度为_____ (用含w、a、b的代数式表示)。

已知:
i.Bi3易水解。NaBiO3难溶于冷水。
ii.“氧化浸取”时,铋元素转化为Bi3,硫元素转化为硫单质。
iii.Cu(OH)2(s)+4NH3(g)
 Cu[(NH3)4]2-(aq)+2OH-(aq) K=4.4×10-7
Cu[(NH3)4]2-(aq)+2OH-(aq) K=4.4×10-7回答下列问题:
(1)为提高“浸取”速率,采取的措施有:升高温度、

(2)“氧化浸取”时,H2O2和FeS2发生反应的物质的量之比为
(3)“除铜”时发生反应:Cu2+(aq)+4NH3(g)
 Cu[(NH3)4]2-(aq) K=2×1013,则Ksp[Cu(OH)2]=
Cu[(NH3)4]2-(aq) K=2×1013,则Ksp[Cu(OH)2]=(4)“转化”时,生成NaBiO3的离子方程式为
(5)已知酸性环境下,NaBiO3的可以将
 氧化成
氧化成 (
(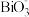 被还原成
被还原成 )
)取NaBiO3产品wg,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用amol·L1H2C2O4标准溶液滴定生成的
 ,当溶液紫红色恰好褪去时,消耗bmL标准溶液。该产品的纯度为
,当溶液紫红色恰好褪去时,消耗bmL标准溶液。该产品的纯度为
您最近一年使用:0次



