1 . 设 为阿伏加德罗常数的值。如果
为阿伏加德罗常数的值。如果 某气态双原子分子的分子数为p,则
某气态双原子分子的分子数为p,则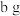 该气体在标准状况下的体积
该气体在标准状况下的体积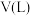 是
是
 为阿伏加德罗常数的值。如果
为阿伏加德罗常数的值。如果 某气态双原子分子的分子数为p,则
某气态双原子分子的分子数为p,则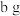 该气体在标准状况下的体积
该气体在标准状况下的体积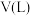 是
是A.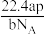 | B.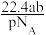 | C. | D.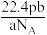 |
您最近一年使用:0次
2 . 科学家制得一种新型分子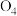 ,关于
,关于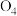 和
和 的下列说法不正确的是
的下列说法不正确的是
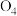 ,关于
,关于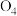 和
和 的下列说法不正确的是
的下列说法不正确的是| A.互为同素异形体 | B.等质量的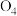 和 和 所含原子数不同 所含原子数不同 |
| C.都属于单质 | D.它们的转化属于化学变化 |
您最近一年使用:0次
名校
3 . 写出下列序号所代表的内容(假设温度为0℃,压强为101Kpa):
| 物质 | 分子数 | 质量 | 物质的量 | 摩尔质量 | 体积 |
| 氧气 | 3.01×1023 | 16g | ① | 32g/mol | ② |
| 水 | ③ | ④ | 2mol | ⑤ | 40cm3 |
您最近一年使用:0次
解题方法
4 . 下列说法正确的是
A.同温同压下,相同质量的 、 、 两种气体,密度之比为3:2 两种气体,密度之比为3:2 |
B.同温同压下,相同质量的 和 和 两种气体,其原子数目一定相等 两种气体,其原子数目一定相等 |
C.同温同压下,相同原子数目的 和 和 两种气体,其质量一定相等 两种气体,其质量一定相等 |
| D.同温同压下,相同体积的气体A和气体B,其物质的量一定相等 |
您最近一年使用:0次
5 . 按要求填空
(1)0.5mol SO2共约含有____ 个原子,它与___ 克SO3所含硫原子数相等。
(2)将质量比为14 :15的N2和NO混合,则N2和NO的物质的量之比为_____ ,混合气体中氮原子和氧原子的个数比为________ 。
(3)同温同压下,质量相同的五种气体:①CO2 ②H2 ③O2 ④CH4 ,所占的体积由大到小的顺序是(填序号)__________ 。
(4)标准状况下,有N2和CO2混合气体质量为18g,体积为11.2L,则此混合气体中N2的物质的量为_____ mol; CO2的质量是____ 克。
(1)0.5mol SO2共约含有
(2)将质量比为14 :15的N2和NO混合,则N2和NO的物质的量之比为
(3)同温同压下,质量相同的五种气体:①CO2 ②H2 ③O2 ④CH4 ,所占的体积由大到小的顺序是(填序号)
(4)标准状况下,有N2和CO2混合气体质量为18g,体积为11.2L,则此混合气体中N2的物质的量为
您最近一年使用:0次
6 . 请按要求填空。
(1)标况下等质量的O2与O3的体积之比为___________ 。
(2)1.7 g H2O2中含有O原子的物质的量为___________ ,质子数目为___________ ,已知a g H2O2中含原子数为b,则阿伏加德罗常数可表示为___________ (用含a、b的代数式表示)
(3)12.4 g Na2X中含有0.4 mol Na+,X的相对原子质量是___________ 。
(4)已知在标准状况下,某气体密度为1.25 g/L,则该气体摩尔质量为___________ 。
(1)标况下等质量的O2与O3的体积之比为
(2)1.7 g H2O2中含有O原子的物质的量为
(3)12.4 g Na2X中含有0.4 mol Na+,X的相对原子质量是
(4)已知在标准状况下,某气体密度为1.25 g/L,则该气体摩尔质量为
您最近一年使用:0次
名校
7 . 关于物质的量计算,试回答:(设NA为阿伏伽德罗常数)
(1)6.02×1022个OH-中含有___________ mol质子,___________ mol电子。
(2)1.204×1024个H2S分子中所含硫元素的质量为___________ 。
(3)常温常压下,160g的SO3气体含有的原子数为___________ 。
(4)含有3.01×1023个O原子的H2O与___________ molNH3的质量相同。
(5)SO2和O2在一定条件可下发生反应:2SO2+O2 2SO3,现有amolSO2和bmolO2充分反应后,硫原子与氧原子的个数比为
2SO3,现有amolSO2和bmolO2充分反应后,硫原子与氧原子的个数比为___________ 。
(6)在25℃、101kPa的条件下,等质量的CH4和A气体的分子数之比为15∶8,则A的摩尔质量为___________ 。
(7)1.6g某物质含有3.01×1022个分子,该物质的相对分子质量为___________ 。
(1)6.02×1022个OH-中含有
(2)1.204×1024个H2S分子中所含硫元素的质量为
(3)常温常压下,160g的SO3气体含有的原子数为
(4)含有3.01×1023个O原子的H2O与
(5)SO2和O2在一定条件可下发生反应:2SO2+O2
 2SO3,现有amolSO2和bmolO2充分反应后,硫原子与氧原子的个数比为
2SO3,现有amolSO2和bmolO2充分反应后,硫原子与氧原子的个数比为(6)在25℃、101kPa的条件下,等质量的CH4和A气体的分子数之比为15∶8,则A的摩尔质量为
(7)1.6g某物质含有3.01×1022个分子,该物质的相对分子质量为
您最近一年使用:0次
名校
8 . 根据所学知识填空
(1)1.0molH2O中,氢原子与氧原子个数之比为___________ 。
(2)1.204×1023个CO2分子的物质的量为___________ mol。
(3)1molOH-中含有___________ mol电子。
(4)在标准状况下,由CO和CO2组成的混合气体22.4L,质量是40g。此混合物中CO和CO2的物质的量比是___________ 。
(5)写出FeCl2溶液中通入Cl2的离子方程式___________ 。
(1)1.0molH2O中,氢原子与氧原子个数之比为
(2)1.204×1023个CO2分子的物质的量为
(3)1molOH-中含有
(4)在标准状况下,由CO和CO2组成的混合气体22.4L,质量是40g。此混合物中CO和CO2的物质的量比是
(5)写出FeCl2溶液中通入Cl2的离子方程式
您最近一年使用:0次
名校
9 . 物质的量是国际单位制中7个基本物理量之一、利用物质的量及其导出量可以大大简化相关的化学计算。
(1)标准状况下,与0.5molH3PO4含有相同数目氧原子的CO2气体的体积为___________ L。
(2)标准状况下,N2的密度为_______ g∙L-1;同温同体积下,相同质量的N2与O2的压强之比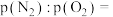
________ 。
(3)酸式(或碱式)滴定管是实验室常见的一种计量溶液体积的精确仪器。已知:从滴定管中滴出的25滴水即为1.00mL。若该实验条件下,水的密度为1 g∙cm-3,则滴定管滴出的半滴水中H2O分子数目为___________ (保留两位有效数字)。
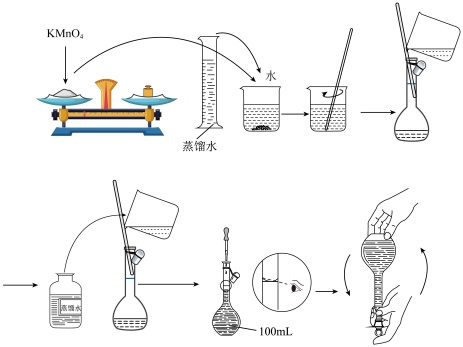
(4) KMnO4是一种重要的氧化剂,实验室若要配制100mL0.50mol∙L-1 KMnO4溶液,则需用托盘天平称取KMnO4固体质量为___________  ;其中确定100mL溶液体积的容器是
;其中确定100mL溶液体积的容器是___________ (填名称);若按照下图所示操作配制KMnO4溶液,则KMnO4溶液浓度将___________ (填“偏高、偏低或无影响”)。
(1)标准状况下,与0.5molH3PO4含有相同数目氧原子的CO2气体的体积为
(2)标准状况下,N2的密度为
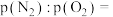
(3)酸式(或碱式)滴定管是实验室常见的一种计量溶液体积的精确仪器。已知:从滴定管中滴出的25滴水即为1.00mL。若该实验条件下,水的密度为1 g∙cm-3,则滴定管滴出的半滴水中H2O分子数目为
(4) KMnO4是一种重要的氧化剂,实验室若要配制100mL0.50mol∙L-1 KMnO4溶液,则需用托盘天平称取KMnO4固体质量为
 ;其中确定100mL溶液体积的容器是
;其中确定100mL溶液体积的容器是
您最近一年使用:0次
解题方法
10 . 回答下列问题。
(1)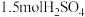 的质量是
的质量是___________ g,完全中和消耗NaOH的物质的量是___________ mol,该硫酸所含氢元素的质量与___________  中所含氢元素的质量相同。
中所含氢元素的质量相同。
(2)等质量的 和
和 ,它们的物质的量之比为
,它们的物质的量之比为___________ ,所含分子数之比为___________ 。
(3)含相同原子数目的甲烷 和氨气
和氨气 ,它们分子数之比为
,它们分子数之比为___________ 。
(4) 中含
中含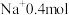 ,则
,则 的摩尔质量为
的摩尔质量为___________ g/mol,X的相对原子质量___________ 。
(1)
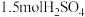 的质量是
的质量是 中所含氢元素的质量相同。
中所含氢元素的质量相同。(2)等质量的
 和
和 ,它们的物质的量之比为
,它们的物质的量之比为(3)含相同原子数目的甲烷
 和氨气
和氨气 ,它们分子数之比为
,它们分子数之比为(4)
 中含
中含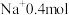 ,则
,则 的摩尔质量为
的摩尔质量为
您最近一年使用:0次



