1 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.22.4LNO2含有的原子总数为3NA |
| B.常温下,将2.7g铝片投入浓硝酸中,转移的电子总数为0.3NA |
| C.5.6g铁粉与足量稀硫酸反应,转移的电子总数为0.3NA |
| D.11.2gN2含有的原子总数为0.8NA |
您最近一年使用:0次
2 . 回答下列问题。
(1)同温同压下,同体积的氨气和硫化氢(H2S)气体的质量之比为___________ ,密度之比为___________ 。
(2)同温同压下,同质量的氨气和硫化氢气体的体积之比为___________ ,其中含有的氢原子数目之比为___________ 。
(3)同温同压下,氨气和硫化氢气体含有的氢原子数相等,则氨气和硫化氢气体的体积之比为___________ ,电子数之比为___________ 。
(1)同温同压下,同体积的氨气和硫化氢(H2S)气体的质量之比为
(2)同温同压下,同质量的氨气和硫化氢气体的体积之比为
(3)同温同压下,氨气和硫化氢气体含有的氢原子数相等,则氨气和硫化氢气体的体积之比为
您最近一年使用:0次
名校
解题方法
3 . NA为阿伏加德罗常数的值,下列有关叙述正确的是
| A.标准状况下,11.2L氖气中所含电子数为0.5NA |
B.32g环状S8( )分子中含有的 )分子中含有的 键的数目为NA 键的数目为NA |
C.常温常压下,3.6gD2O与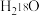 组成的体系中含有中子数2NA 组成的体系中含有中子数2NA |
D.某电池的总反应为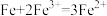 ,当有5.6gFe溶解时电路中有0.3NA电子通过 ,当有5.6gFe溶解时电路中有0.3NA电子通过 |
您最近一年使用:0次
解题方法
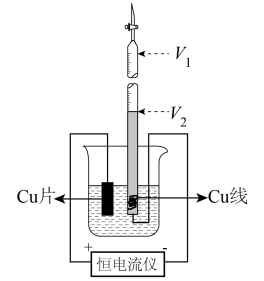
4 . Cu2O主要在玻璃、搪瓷工业中作红色颜料。阿伏加德罗常数(NA)是化学中重要的物理常数。某实验小组利用下图装置电化学合成Cu2O并采用量气法测定阿伏加德罗常数的值(夹持装置略)。
实验步骤为:
Ⅱ.用砂纸打磨Cu片表面,洗涤干净,用滤纸擦干后插入烧杯内。
Ⅲ.取一段Cu线,把Cu线一端的绝缘层剥掉并弯成螺旋状,插入量气管的倒口中。
Ⅳ.将Cu片和Cu线分别连接恒电流仪的两极,进行电解实验。
Ⅴ.电解结束后,读出量气管中液面位置V2,离心分离出烧杯中的Cu2O固体,并用适量蒸馏水洗涤。
回答下列问题:
(1)量气管不采用酸式滴定管的原因是_______ 。该小组进行了多次平行实验,在每次实验中,量气管中液面位置V1应尽可能控制在同一位置,目的是_______ 。
(2)步骤Ⅱ中,Cu片打磨前,表面黑色物质的主要成分为_______ (写化学式)。
(3)步骤Ⅲ中,Cu线裸露部分应全部放在量气管内,目的是_______ 。
(4)电解时,Cu片附近首先析出白色的CuCl,进而转化为Cu2O。该条件下CuCl转化为Cu2O的离子方程式为_______ 。
(5)某次实验,电解电流为100.0mA,电解时间为722s,测量的体积折合成H2的物质的量为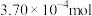 ,则NA值为
,则NA值为_______ (用科学计数法表示,保留2位小数,已知单个电子的电量约为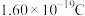 )。
)。
(6)步骤Ⅴ中,可通过检测洗出液中是否存在Cl-来判断洗涤是否完成。检测的方法是_____ 。
实验步骤为:
Ⅱ.用砂纸打磨Cu片表面,洗涤干净,用滤纸擦干后插入烧杯内。
Ⅲ.取一段Cu线,把Cu线一端的绝缘层剥掉并弯成螺旋状,插入量气管的倒口中。
Ⅳ.将Cu片和Cu线分别连接恒电流仪的两极,进行电解实验。
Ⅴ.电解结束后,读出量气管中液面位置V2,离心分离出烧杯中的Cu2O固体,并用适量蒸馏水洗涤。
回答下列问题:
(1)量气管不采用酸式滴定管的原因是
(2)步骤Ⅱ中,Cu片打磨前,表面黑色物质的主要成分为
(3)步骤Ⅲ中,Cu线裸露部分应全部放在量气管内,目的是
(4)电解时,Cu片附近首先析出白色的CuCl,进而转化为Cu2O。该条件下CuCl转化为Cu2O的离子方程式为
(5)某次实验,电解电流为100.0mA,电解时间为722s,测量的体积折合成H2的物质的量为
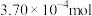 ,则NA值为
,则NA值为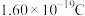 )。
)。(6)步骤Ⅴ中,可通过检测洗出液中是否存在Cl-来判断洗涤是否完成。检测的方法是
您最近一年使用:0次
5 . NA表示阿伏加德罗常数,下列说法正确的是
A.3molT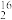 O分子中的分子总数为42NA O分子中的分子总数为42NA |
| B.氧原子总数为0.2NA的SO2和O2的混合气体,其体积为2.24L |
| C.0.1mol•L-1的Na2SO4溶液中含有Na+数目为0.2NA |
| D.7.8gNa2O2和Na2S的混合物中含有的阴离子数目为0.1NA |
您最近一年使用:0次
解题方法
6 . 回答下列问题。
(1)已知硫酸钠晶体(Na2SO4·10H2O)的物质的量为0.5 mol,则所含钠离子的物质的量是___________ ,钠离子的数目是___________ ,所含硫酸根离子的物质的量是___________ 。
(2)18克水的物质的量为___________ ,其中含有H的原子的数目约为多少___________ 。
(1)已知硫酸钠晶体(Na2SO4·10H2O)的物质的量为0.5 mol,则所含钠离子的物质的量是
(2)18克水的物质的量为
您最近一年使用:0次
名校
7 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,5.6 LH2O中,所含的氢原子总数为0.5NA |
| B.0.2 mol/LFeCl3溶液中,所含氯离子的数目为0.6NA |
| C.常温常压下,1.4 g N2和CO的混合气体中,所含的原子总数为0.1NA |
| D.等物质的量的H2和O2的混合气体中,所含的分子数为NA |
您最近一年使用:0次
8 . 回答下列问题。
(1)1 mol CO(NH2)2中含___________ mol氮原子,___________ 个氧原子,所含氧原子数跟___________ mol H2O所含氧原子数相等。
(2)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为___________ ,R的相对原子质量为___________ 。含R的质量为1.6 g的Na2R,其物质的量为___________ 。
(3)铝合金具有广泛的用途,但铝制器具不宜盛放碱性食物,其请写出该反应的离子方程式___________ ,若生成6.72L气体(标准状况),则消耗铝的质量为___________ g。
(1)1 mol CO(NH2)2中含
(2)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为
(3)铝合金具有广泛的用途,但铝制器具不宜盛放碱性食物,其请写出该反应的离子方程式
您最近一年使用:0次
9 . 在标准状况下①6.72LC2H6 ②3.01×1023个NH3分子 ③13.6gH2S ④0.6molH2O,下列对这四种气体关系从大到小的表达正确的是
| A.物质的量:③>①>④>② | B.原子数:①>②>④>③ |
| C.体积:④>②>③>① | D.质量:④>③>①>② |
您最近一年使用:0次
名校
10 . 下列物质所含分子数最多的是
A.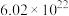 个 个 | B. | C. | D.标准状况下 |
您最近一年使用:0次



