名校
解题方法
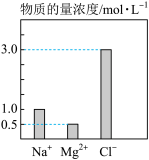
1 . 某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有 、
、 、
、 、
、 、
、 。为了进一步确认,对该溶液进行实验检测:
。为了进一步确认,对该溶液进行实验检测:
步骤一:仔细观察,该溶液呈无色、透明、均一状态:
步骤二:加入足量 溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失。
溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失。
(1)原溶液中除图中的离子外,肯定还含有的离子是_______ ,肯定不含有的离子是_______ 。
(2)步骤二中称量沉淀前的实验操作步骤有:过滤、洗涤、干燥。检验沉淀已洗干净的方法是_______ 。
(3)原溶液中 物质的量浓度为
物质的量浓度为_______ mol/L。
(4)向原溶液中加入 溶液,反应的离子方程式为
溶液,反应的离子方程式为_______ 。
(5)若向100mL原溶液中加入1mol/L的 溶液,当生成的沉淀质量刚好最大时,加入的
溶液,当生成的沉淀质量刚好最大时,加入的 溶液体积为
溶液体积为_______ L。
 、
、 、
、 、
、 、
、 。为了进一步确认,对该溶液进行实验检测:
。为了进一步确认,对该溶液进行实验检测:
步骤一:仔细观察,该溶液呈无色、透明、均一状态:
步骤二:加入足量
 溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失。
溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失。(1)原溶液中除图中的离子外,肯定还含有的离子是
(2)步骤二中称量沉淀前的实验操作步骤有:过滤、洗涤、干燥。检验沉淀已洗干净的方法是
(3)原溶液中
 物质的量浓度为
物质的量浓度为(4)向原溶液中加入
 溶液,反应的离子方程式为
溶液,反应的离子方程式为(5)若向100mL原溶液中加入1mol/L的
 溶液,当生成的沉淀质量刚好最大时,加入的
溶液,当生成的沉淀质量刚好最大时,加入的 溶液体积为
溶液体积为
您最近一年使用:0次
2022-12-28更新
|
252次组卷
|
4卷引用:河南省周口中英文学校2019届高三上学期第三次月考化学试题
河南省周口中英文学校2019届高三上学期第三次月考化学试题陕西省渭南市华阴市2021-2022学年高一上学期期末考试化学试题宁夏平罗中学2022-2023学年高二下学期期中考试化学试题(已下线)第11讲 物质的量浓度-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)
名校
2 . 按要求填空:
(1)已知17g 中含1
中含1 H,则R的摩尔质量为
H,则R的摩尔质量为_____________ 。
(2)同温同压下,等体积的 和
和 的质量之比为
的质量之比为_____________ 。
(3)若由 和
和 组成的混合气体的平均相对分子质量为20.4,则混合气中
组成的混合气体的平均相对分子质量为20.4,则混合气中 和
和 的分子数之比为
的分子数之比为_______ 。
(4)将a L标准状况下的氯化氢气体溶于100 水中(水的密度近似为1
水中(水的密度近似为1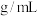 ),得到密度为ρ
),得到密度为ρ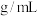 的盐酸,则该盐酸的物质的量浓度是
的盐酸,则该盐酸的物质的量浓度是_____________  。
。
(1)已知17g
 中含1
中含1 H,则R的摩尔质量为
H,则R的摩尔质量为(2)同温同压下,等体积的
 和
和 的质量之比为
的质量之比为(3)若由
 和
和 组成的混合气体的平均相对分子质量为20.4,则混合气中
组成的混合气体的平均相对分子质量为20.4,则混合气中 和
和 的分子数之比为
的分子数之比为(4)将a L标准状况下的氯化氢气体溶于100
 水中(水的密度近似为1
水中(水的密度近似为1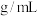 ),得到密度为ρ
),得到密度为ρ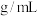 的盐酸,则该盐酸的物质的量浓度是
的盐酸,则该盐酸的物质的量浓度是 。
。
您最近一年使用:0次
名校
解题方法
3 . 回答下列问题
(1)在温度t℃时,某溶液中c(H+)= mol/L,c(OH-)=
mol/L,c(OH-)= mol/L,已知a+b=12,则t
mol/L,已知a+b=12,则t_______ 25℃(填“大于”“小于”或“等于”)。
(2)常温下,向某Ba(OH)2溶液中逐滴加入pH=x的盐酸,测得混合溶液的部分pH如下表所示:
X= _______ 。Ba(OH)2溶液的物质的量浓度为 _______ 。
(3)常温下,向100mL pH=2的硫酸与硫酸钠的混合溶液中,加入300mL上述Ba(OH)2溶液,沉淀正好达最大量,此时溶液的pH_______ 7(填“大于”“小于”或“等于”);原混合溶液中硫酸钠的物质的量浓度为 _______ 。
(1)在温度t℃时,某溶液中c(H+)=
 mol/L,c(OH-)=
mol/L,c(OH-)= mol/L,已知a+b=12,则t
mol/L,已知a+b=12,则t(2)常温下,向某Ba(OH)2溶液中逐滴加入pH=x的盐酸,测得混合溶液的部分pH如下表所示:
| 序号 | 氢氧化钡溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 12 |
| ② | 22.00 | 18.00 | 11 |
| ③ | 22.00 | 22.00 | 7 |
(3)常温下,向100mL pH=2的硫酸与硫酸钠的混合溶液中,加入300mL上述Ba(OH)2溶液,沉淀正好达最大量,此时溶液的pH
您最近一年使用:0次
4 . 将标准状况下22.4L氯化氢气体溶于水得到500mL的溶液,计算
(1)所得溶液溶质的物质的量浓度为_______ mol/L。
(2)上述溶液可与_______ mL2mol/L的氢氧化钠溶液恰好完全反应。
(1)所得溶液溶质的物质的量浓度为
(2)上述溶液可与
您最近一年使用:0次
名校
5 . 回答下列问题
(1)某硫酸钠溶液50mL中含有1.15gNa+,取出10mL稀释至20mL后所得溶液中 的物质的量浓度是
的物质的量浓度是_______ 。
(2)12.4g Na2X中含有0.4mol Na+,则该物质的化学式为_______ 。
(3)室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示。

①A室混合气体所含分子总数约为_______ 。
②实验测得A室混合气体的质量为34g,则该混合气体的密度是同温同压下氦气密度的_______ 倍。
③若将A室H2、O2的混合气体点燃引爆,恢复原温度后,最终活塞停留的位置在_______ 刻度,容器内气体压强与反应前气体压强之比为_______ 。
(1)某硫酸钠溶液50mL中含有1.15gNa+,取出10mL稀释至20mL后所得溶液中
 的物质的量浓度是
的物质的量浓度是(2)12.4g Na2X中含有0.4mol Na+,则该物质的化学式为
(3)室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示。

①A室混合气体所含分子总数约为
②实验测得A室混合气体的质量为34g,则该混合气体的密度是同温同压下氦气密度的
③若将A室H2、O2的混合气体点燃引爆,恢复原温度后,最终活塞停留的位置在
您最近一年使用:0次
名校
6 . 回答下列问题
(1)标准状况下有①0.5NA个HCl分子②25.6g SO2气体③0.2mol 氨气④2mol 氦气⑤6.02×1023个白磷分子⑥33.6L甲烷,用数字序号填写下列空白,质量最大的是_______ ,体积最小的是_______ ,所含原子个数从大到小的顺序为_______ 。
(2)现有M、N两种气态化合物,其摩尔质量之比为2:1,试回答下列问题:
①同温同压下,M、N气体的密度之比为_______ 。
②相同温度下,在两个相同体积的密闭容器中分别充入M、N,若两个容器中气体的密度相等,则两个容器中的压强之比为_______ 。
(3)20℃时,20mL NaOH溶液质量为20g,将其蒸干后得氢氧化钠4g,则20℃时,则氢氧化钠溶液的物质的量浓度为_______
(1)标准状况下有①0.5NA个HCl分子②25.6g SO2气体③0.2mol 氨气④2mol 氦气⑤6.02×1023个白磷分子⑥33.6L甲烷,用数字序号填写下列空白,质量最大的是
(2)现有M、N两种气态化合物,其摩尔质量之比为2:1,试回答下列问题:
①同温同压下,M、N气体的密度之比为
②相同温度下,在两个相同体积的密闭容器中分别充入M、N,若两个容器中气体的密度相等,则两个容器中的压强之比为
(3)20℃时,20mL NaOH溶液质量为20g,将其蒸干后得氢氧化钠4g,则20℃时,则氢氧化钠溶液的物质的量浓度为
您最近一年使用:0次
7 . 有(NH4)2CO3 和 NH4HCO3 混合物 25.4g,加入 100mL 某浓度的 Ba(OH)2 溶液,充分反应,使沉淀完全,加热悬浊液后生成 NH30.400mol。计算:
(1)(NH4)2CO3 和 NH4HCO3 的物质的量之比_______ 。
(2)Ba(OH)2 溶液的物质的量浓度_______ 。
(1)(NH4)2CO3 和 NH4HCO3 的物质的量之比
(2)Ba(OH)2 溶液的物质的量浓度
您最近一年使用:0次
8 . 25℃时,向20mL硫酸氢钠和盐酸的混合液中,逐滴加入0.05 mol∙L−1Ba(OH)2溶液时,生成BaSO4的量和溶液的pH变化如图(忽略溶液混合时溶液体积的变化),计算:

(1)原混合液中硫酸氢钠的物质的量浓度___ 。
(2)原混合液中HCl的物质的量浓度___ 。
(3)B点时溶液的pH___ 。

(1)原混合液中硫酸氢钠的物质的量浓度
(2)原混合液中HCl的物质的量浓度
(3)B点时溶液的pH
您最近一年使用:0次
9 . 实验室常用邻苯二甲酸氢钾(KHC8H4O4)来测定氢氧化钠溶液的浓度,反应如下:KHC8H4O4+NaOH=KNaC8H4O4+H2O。若氢氧化钠溶液的浓度为0.1mol·L-1,到达终点时,溶液的pH约为9.1。
(1)在测定氢氧化钠溶液浓度时,有下列操作:①向溶液中加入1-2滴指示剂②向锥形瓶中加20-30mL蒸馏水溶解③用氢氧化钠溶液滴定到终点,半分钟不褪色④重复以上操作⑤准确称取0.4-0.5g邻苯二甲酸氢钾加入250mL锥形瓶中⑥根据两次实验数据计算氢氧化钠的物质的量浓度。
以上各步中,正确的(填序号)操作顺序是___ 。
(2)该实验应选用___ 作指示剂,达到滴定终点时溶液由___ 色变为___ 色。
(3)上述操作中,将邻苯二甲酸氢钾直接放到锥形瓶中溶解,对实验是否有影响?___ ,并说明理由:___ 。
(4)滴定前,用蒸馏水洗净碱式滴定管,然后加待测定的氢氧化钠溶液滴定,此操作将造成实验结果___ (填“偏大”“偏小”或“无影响”)
(5)现准确称取KHC8H4O4(分子量204.2)晶体0.5105g,溶于水后加入指示剂,用NaOH溶液滴定至终点,消耗NaOH20.00mL,则NaOH溶液的浓度为___ (结果保留四位有效数字)。
(1)在测定氢氧化钠溶液浓度时,有下列操作:①向溶液中加入1-2滴指示剂②向锥形瓶中加20-30mL蒸馏水溶解③用氢氧化钠溶液滴定到终点,半分钟不褪色④重复以上操作⑤准确称取0.4-0.5g邻苯二甲酸氢钾加入250mL锥形瓶中⑥根据两次实验数据计算氢氧化钠的物质的量浓度。
以上各步中,正确的(填序号)操作顺序是
(2)该实验应选用
(3)上述操作中,将邻苯二甲酸氢钾直接放到锥形瓶中溶解,对实验是否有影响?
(4)滴定前,用蒸馏水洗净碱式滴定管,然后加待测定的氢氧化钠溶液滴定,此操作将造成实验结果
(5)现准确称取KHC8H4O4(分子量204.2)晶体0.5105g,溶于水后加入指示剂,用NaOH溶液滴定至终点,消耗NaOH20.00mL,则NaOH溶液的浓度为
您最近一年使用:0次
名校
10 . 回答下列问题:
(1)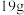 某二价金属氯化物(
某二价金属氯化物(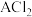 )中含有
)中含有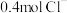 ,则
,则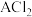 的摩尔质量是
的摩尔质量是_______ ,A的相对原子质量是_______ ,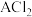 的化学式是
的化学式是_______ 。
(2)如图实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
①该浓盐酸中 的物质的量浓度为
的物质的量浓度为_______  。
。
②取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_______ 。
A.溶液中 的物质的量B.溶液的浓度
的物质的量B.溶液的浓度
C.溶液中 的数目D.溶液的密度
的数目D.溶液的密度
③学生欲用上述浓盐酸加蒸馏水稀释 得到物质的量浓度为
得到物质的量浓度为 的稀盐酸,该学生需要量取
的稀盐酸,该学生需要量取_______  上述浓盐酸进行配制。
上述浓盐酸进行配制。
④假设该同学用 的盐酸中和含
的盐酸中和含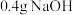 的
的 溶液,则该同学需取
溶液,则该同学需取_______  稀盐酸。
稀盐酸。
(1)
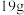 某二价金属氯化物(
某二价金属氯化物(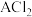 )中含有
)中含有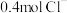 ,则
,则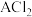 的摩尔质量是
的摩尔质量是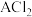 的化学式是
的化学式是(2)如图实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
盐酸 分子式: 相对分子质量:36.5 密度:   的质量分数: 的质量分数: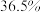 |
 的物质的量浓度为
的物质的量浓度为 。
。②取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是
A.溶液中
 的物质的量B.溶液的浓度
的物质的量B.溶液的浓度C.溶液中
 的数目D.溶液的密度
的数目D.溶液的密度③学生欲用上述浓盐酸加蒸馏水稀释
 得到物质的量浓度为
得到物质的量浓度为 的稀盐酸,该学生需要量取
的稀盐酸,该学生需要量取 上述浓盐酸进行配制。
上述浓盐酸进行配制。④假设该同学用
 的盐酸中和含
的盐酸中和含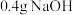 的
的 溶液,则该同学需取
溶液,则该同学需取 稀盐酸。
稀盐酸。
您最近一年使用:0次



