名校
1 . 将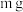 某二价金属氯化物溶于水中配成
某二价金属氯化物溶于水中配成 溶液,从中取出一半,再加水稀释到
溶液,从中取出一半,再加水稀释到 ,此时
,此时 的物质的量浓度为
的物质的量浓度为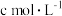 ,则此氯化物中金属原子的相对原子质量为
,则此氯化物中金属原子的相对原子质量为
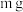 某二价金属氯化物溶于水中配成
某二价金属氯化物溶于水中配成 溶液,从中取出一半,再加水稀释到
溶液,从中取出一半,再加水稀释到 ,此时
,此时 的物质的量浓度为
的物质的量浓度为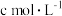 ,则此氯化物中金属原子的相对原子质量为
,则此氯化物中金属原子的相对原子质量为A.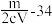 | B.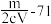 | C.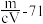 | D.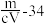 |
您最近一年使用:0次
2021-11-06更新
|
652次组卷
|
4卷引用:四川省成都市蓉城名校联盟2021-2022学年高一上学期期中联考化学试题
2 . 实验室有质量分数为98%,密度为 的浓硫酸,现需配制浓度为
的浓硫酸,现需配制浓度为 ,体积为
,体积为 的稀硫酸,则所需浓硫酸的体积为
的稀硫酸,则所需浓硫酸的体积为
 的浓硫酸,现需配制浓度为
的浓硫酸,现需配制浓度为 ,体积为
,体积为 的稀硫酸,则所需浓硫酸的体积为
的稀硫酸,则所需浓硫酸的体积为
A.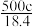 | B.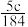 | C.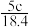 | D.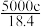 |
您最近一年使用:0次
2021-11-06更新
|
273次组卷
|
3卷引用:四川省成都市蓉城名校联盟2021-2022学年高一上学期期中联考化学试题
名校
解题方法
3 . 根据所学知识,按要求填写下列空格。
(1)约含 个氧原子的
个氧原子的 的物质的量为
的物质的量为___________  ,与上述
,与上述 中所含原子总数相同的
中所含原子总数相同的 标准状况下体积是
标准状况下体积是___________ L;
(2) 硫酸铝溶液中,
硫酸铝溶液中,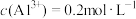 ,则
,则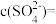
___________  ;将该溶液稀释至
;将该溶液稀释至 ,稀释后溶液中的
,稀释后溶液中的 的物质的量为
的物质的量为___________  。
。
(3) 某金属硝酸盐
某金属硝酸盐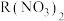 中含有
中含有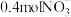 ,则
,则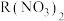 的摩尔质量为
的摩尔质量为___________ , 的相对原子质量为
的相对原子质量为___________ 。
(4)现有标准状况下 和
和 混合气体为
混合气体为 ,其质量为
,其质量为 ,则此混合气体中,
,则此混合气体中, 和
和 的物质的量之比为
的物质的量之比为___________ ,C和O原子个数比为___________ 。
(1)约含
 个氧原子的
个氧原子的 的物质的量为
的物质的量为 ,与上述
,与上述 中所含原子总数相同的
中所含原子总数相同的 标准状况下体积是
标准状况下体积是(2)
 硫酸铝溶液中,
硫酸铝溶液中,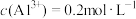 ,则
,则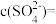
 ;将该溶液稀释至
;将该溶液稀释至 ,稀释后溶液中的
,稀释后溶液中的 的物质的量为
的物质的量为 。
。(3)
 某金属硝酸盐
某金属硝酸盐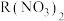 中含有
中含有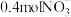 ,则
,则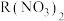 的摩尔质量为
的摩尔质量为 的相对原子质量为
的相对原子质量为(4)现有标准状况下
 和
和 混合气体为
混合气体为 ,其质量为
,其质量为 ,则此混合气体中,
,则此混合气体中, 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
名校
4 . 回答下列问题:
(1)某同学将标准状况下44.8 L的HCl气体溶于水,配成500 mL的溶液。所配成的盐酸溶液的物质的量浓度为___________ ,稀释到2 L,此时盐酸溶液物质的量浓度为___________ 。
(2)在400mL 2 的
的 溶液中,溶质的质量是
溶液中,溶质的质量是___________ ,此溶液中的 的物质的量浓度为
的物质的量浓度为___________ 。
(3)在氨水溶液中,有多种微粒, 的摩尔质量为
的摩尔质量为___________ ,1mol  含有的电子数目为
含有的电子数目为___________ ,1mol  含有的质子数目为
含有的质子数目为___________ 。
(1)某同学将标准状况下44.8 L的HCl气体溶于水,配成500 mL的溶液。所配成的盐酸溶液的物质的量浓度为
(2)在400mL 2
 的
的 溶液中,溶质的质量是
溶液中,溶质的质量是 的物质的量浓度为
的物质的量浓度为(3)在氨水溶液中,有多种微粒,
 的摩尔质量为
的摩尔质量为 含有的电子数目为
含有的电子数目为 含有的质子数目为
含有的质子数目为
您最近一年使用:0次
名校
5 . 根据所学知识填空:
(1)___________ mol H2O中含有的氧原子数与1.5 mol CO2中含有的氧原子数相等。
(2)标准状况下,4.48L NH3中N原子质量为___________ g,H原子数目为___________ 。
(3)已知a g A和b g B恰好完全反应生成0.2 mol C和d g D,则C的摩尔质量为___________ (用含a、b、d的表达式表示)。
(4)NA为阿伏加德罗常数,标准状况下,m g某气体中含有b个分子,则n g该气体在相同状态下的体积为___________ L(用含m、n、b、NA的表达式表示)
(5)将80.0 g无水硫酸铁溶于水配制成500 mL溶液,若从中取出50 mL,用水稀释到100 mL,所得溶液中Fe3+的物质的量浓度为___________ 。
(1)
(2)标准状况下,4.48L NH3中N原子质量为
(3)已知a g A和b g B恰好完全反应生成0.2 mol C和d g D,则C的摩尔质量为
(4)NA为阿伏加德罗常数,标准状况下,m g某气体中含有b个分子,则n g该气体在相同状态下的体积为
(5)将80.0 g无水硫酸铁溶于水配制成500 mL溶液,若从中取出50 mL,用水稀释到100 mL,所得溶液中Fe3+的物质的量浓度为
您最近一年使用:0次
名校
解题方法
6 . 下列说法正确的是
| A.某气体X相对氢气的密度是16,则该气体的摩尔质量为32 |
B.V L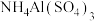 溶液中含a g 溶液中含a g  ,取此溶液 ,取此溶液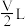 用水稀释为5V L,则稀释后溶液中 用水稀释为5V L,则稀释后溶液中 为 为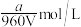 (不考虑水解) (不考虑水解) |
C.常温常压下,同质量的气体X和气体Y,体积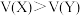 ,则摩尔质量 ,则摩尔质量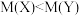 |
D.m g气体Y含分子数为b,则n g该气体在标准状况下体积为( 为阿伏加德罗常数的值) 为阿伏加德罗常数的值)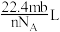 |
您最近一年使用:0次
2021-10-17更新
|
174次组卷
|
2卷引用:江西省抚州市临川区第十中学2022届高三月考化学试卷
名校
7 . 某同学用溶质质量分数为15%的稀盐酸和大理石反应来制取二氧化碳气体:
(1)用20.3g溶质质量分数为37%的浓盐酸能配制上述稀盐酸___ g(结果精确到1g)。
(2)若需收集10瓶(每瓶以125mL计算)二氧化碳气体,问至少需要多少克上述稀盐酸与足量的大理石反应才能制得___ (实验条件下二氧化碳的密度为2g/L)?(写出计算过程,结果精确到0.01g)
(1)用20.3g溶质质量分数为37%的浓盐酸能配制上述稀盐酸
(2)若需收集10瓶(每瓶以125mL计算)二氧化碳气体,问至少需要多少克上述稀盐酸与足量的大理石反应才能制得
您最近一年使用:0次
2021-09-27更新
|
75次组卷
|
2卷引用:四川省绵阳南山中学2021-2022学年高一上学期入学考试化学试题
名校
8 . 下列曲线能正确表达对应的反应或过程的是
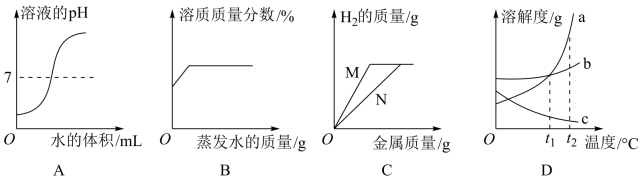

| A.向一定量的盐酸中逐滴加水稀释 |
| B.某温度下将一定量接近饱和的 KNO3 溶液恒温蒸发水分 |
| C.金属与一定量的稀硫酸反应,由图象可知,金属 N 比金属 M 活泼 |
| D.将 a、b、c 三种物质的饱和溶液分别由 t1℃升温至 t2℃时,所得溶液中溶质质量分数大小关系是:a>b>c |
您最近一年使用:0次
20-21高一上·江苏镇江·阶段练习
名校
9 . 实验室用密度为1.19 g/mL、质量分数为36.5%的浓盐酸配制500 mL 0.100 mol/L盐酸。回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为_______ 。
(2)①该实验中需要用量筒量取上述浓盐酸的体积为_______
②该配制实验中所需要的主要玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管、_______ 。
③定容时,向容量瓶中加蒸馏水至液面接近刻度线_______ 处,改用_______ 逐滴滴加蒸馏水,使溶液凹液面恰好与刻度线相切;
(3)配制过程中,下列操作中会导致结果偏高的是_______ (填序号)。
①量取浓盐酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
②容量瓶使用时有少量水
③稀释后立即移液
④移液时不小心有少量液体溅出
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
(4)已知软锰矿(主要成分是MnO2)和浓盐酸混合加热能制取氯气:MnO2+4HCl(浓) MnCl2+ Cl2↑+2H2O。现将一定量软锰矿石与200ml的浓盐酸反应(杂质不参加反应),制得标况下氯气5.6L。
MnCl2+ Cl2↑+2H2O。现将一定量软锰矿石与200ml的浓盐酸反应(杂质不参加反应),制得标况下氯气5.6L。
求①参加反应的HCl的质量_____
②反应后溶液中MnCl2的物质的量浓度_____ (反应前后溶液的体积不变)
(5)实验室为确定一瓶稀NaOH的浓度,用上述所配的盐酸溶液中和25.00mL该NaOH溶液,当酸与碱恰好完全反应时,消耗盐酸溶液22.50mL。试求该NaOH的物质的量浓度_____ 。
(1)该浓盐酸中HCl的物质的量浓度为
(2)①该实验中需要用量筒量取上述浓盐酸的体积为
②该配制实验中所需要的主要玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管、
③定容时,向容量瓶中加蒸馏水至液面接近刻度线
(3)配制过程中,下列操作中会导致结果偏高的是
①量取浓盐酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
②容量瓶使用时有少量水
③稀释后立即移液
④移液时不小心有少量液体溅出
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
(4)已知软锰矿(主要成分是MnO2)和浓盐酸混合加热能制取氯气:MnO2+4HCl(浓)
 MnCl2+ Cl2↑+2H2O。现将一定量软锰矿石与200ml的浓盐酸反应(杂质不参加反应),制得标况下氯气5.6L。
MnCl2+ Cl2↑+2H2O。现将一定量软锰矿石与200ml的浓盐酸反应(杂质不参加反应),制得标况下氯气5.6L。求①参加反应的HCl的质量
②反应后溶液中MnCl2的物质的量浓度
(5)实验室为确定一瓶稀NaOH的浓度,用上述所配的盐酸溶液中和25.00mL该NaOH溶液,当酸与碱恰好完全反应时,消耗盐酸溶液22.50mL。试求该NaOH的物质的量浓度
您最近一年使用:0次
20-21高一下·浙江·阶段练习
解题方法
10 . 某种胃药的有效成分为碳酸钙,某实验小组为测定其中碳酸钙的含量,取10粒药片(0.1 g/粒)研碎后溶解。加入25.00 mL 1.0 mol/L的稀盐酸反应,最后用1.0 mol/LNaOH溶液中和过量的盐酸,测定所消耗的NaOH的溶液体积如下:
(1)配制100 mL 1.0 mol/L的稀盐酸,需要2.5 mol/L的盐酸的体积为___________ mL。
(2)药片中碳酸钙的质量分数为___________ 。
| 测定次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| V(NaOH)/mL | 13.00 | 12.90 | 11.40 | 13.10 |
(1)配制100 mL 1.0 mol/L的稀盐酸,需要2.5 mol/L的盐酸的体积为
(2)药片中碳酸钙的质量分数为
您最近一年使用:0次



