名校
1 . 化学与科技、生活密切相关。下列叙述中正确的是
| A.中国天眼FAST用到的碳化硅是一种新型陶瓷材料 |
| B.从石墨中剥离出的石墨烯薄片能导电,因此是电解质 |
| C.宇宙飞船返回舱外表面使用的高温结构陶瓷的主要成分是硅酸盐 |
| D.光导纤维在信息技术发展中应用广泛,制造光导纤维的主要材料是单质硅 |
您最近一年使用:0次
2 . 下列热化学方程式或离子方程式中,不正确的是
A. 的电离: 的电离: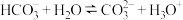 |
B.钢铁发生吸氧腐蚀时正极的电极反应式: |
C.甲烷的燃烧热为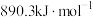 ,则甲烷燃烧的热化学方程式为 ,则甲烷燃烧的热化学方程式为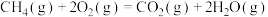 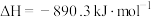 |
D.用饱和碳酸钠溶液处理水垢(CaSO4): |
您最近一年使用:0次
3 . 现有以下物质:
① 、②
、② 、③
、③ 、④
、④ 、⑤漂白粉、⑥
、⑤漂白粉、⑥ 溶液、⑦
溶液、⑦ 。
。
回答下列问题:
(1)上述物质中,属于酸性氧化物的有___________ (填序号,下同),属于电解质的有___________ 。
(2)①与水反应的离子方程式为___________ 。
(3)向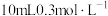 ⑦的水溶液中逐滴滴加
⑦的水溶液中逐滴滴加 ④的水溶液至中性,此时溶液中的
④的水溶液至中性,此时溶液中的
___________  (假设混合后溶液体积的变化忽略不计)。
(假设混合后溶液体积的变化忽略不计)。
(4)向⑥中通入少量①,下图所示⑥溶液的电导率变化曲线合理的是___________(填字母)。
(5)现用NaOH固体配制490mL1.00mol/LNaOH溶液。
①通过计算,需用托盘天平称量 固体的质量为
固体的质量为___________  ;配制溶液时所用的玻璃仪器为量筒、烧杯、胶头滴管、玻璃棒和
;配制溶液时所用的玻璃仪器为量筒、烧杯、胶头滴管、玻璃棒和___________ 。
②下列操作将导致所配 溶液的浓度偏大的是
溶液的浓度偏大的是___________ (填字母)。
A.将烧杯的溶液转移到容量瓶时有溶液溅出瓶外
B.转移溶液之前容量瓶中有少量蒸馏水
C.定容时俯视容量瓶刻度线
D.加水超过刻度线,用胶头滴管吸出多余液体
①
 、②
、② 、③
、③ 、④
、④ 、⑤漂白粉、⑥
、⑤漂白粉、⑥ 溶液、⑦
溶液、⑦ 。
。回答下列问题:
(1)上述物质中,属于酸性氧化物的有
(2)①与水反应的离子方程式为
(3)向
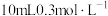 ⑦的水溶液中逐滴滴加
⑦的水溶液中逐滴滴加 ④的水溶液至中性,此时溶液中的
④的水溶液至中性,此时溶液中的
 (假设混合后溶液体积的变化忽略不计)。
(假设混合后溶液体积的变化忽略不计)。(4)向⑥中通入少量①,下图所示⑥溶液的电导率变化曲线合理的是___________(填字母)。
A.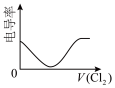 | B.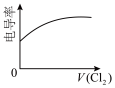 | C.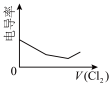 | D.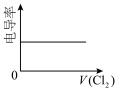 |
(5)现用NaOH固体配制490mL1.00mol/LNaOH溶液。
①通过计算,需用托盘天平称量
 固体的质量为
固体的质量为 ;配制溶液时所用的玻璃仪器为量筒、烧杯、胶头滴管、玻璃棒和
;配制溶液时所用的玻璃仪器为量筒、烧杯、胶头滴管、玻璃棒和②下列操作将导致所配
 溶液的浓度偏大的是
溶液的浓度偏大的是A.将烧杯的溶液转移到容量瓶时有溶液溅出瓶外
B.转移溶液之前容量瓶中有少量蒸馏水
C.定容时俯视容量瓶刻度线
D.加水超过刻度线,用胶头滴管吸出多余液体
您最近一年使用:0次
4 . 下列关于液氨、氨气、氨水和铵盐的叙述正确的是
| A.液氨可用作制冷剂 |
| B.液氨、氨气、氨水属于同一种物质 |
| C.氨水中只含有NH3和H2O两种分子 |
| D.氨气和铵盐在一定条件下均能导电,均属于电解质 |
您最近一年使用:0次
名校
5 . “点水成冰”实验中,用蘸有 粉末的小棒触碰液体球后(成分为饱和
粉末的小棒触碰液体球后(成分为饱和 溶液),它开始“结冰”。下列说法错误的是
溶液),它开始“结冰”。下列说法错误的是
 粉末的小棒触碰液体球后(成分为饱和
粉末的小棒触碰液体球后(成分为饱和 溶液),它开始“结冰”。下列说法错误的是
溶液),它开始“结冰”。下列说法错误的是A.液体球中分散质粒子直径小于 m m |
B. 属于离子化合物,只含离子键 属于离子化合物,只含离子键 |
C.向 溶液中加入NaOH固体,溶液导电性逐渐增强 溶液中加入NaOH固体,溶液导电性逐渐增强 |
D. 中四种元素的原子半径:Na>C>O>H 中四种元素的原子半径:Na>C>O>H |
您最近一年使用:0次
2024-03-26更新
|
68次组卷
|
3卷引用:山西省大同市2023-2024学年高一下学期3月月考化学试题
6 . NaCl溶于水的过程如图所示。下列叙述正确的是


| A.NaCl固体不导电的原因是不含导电的离子 |
| B.NaCl溶于水发生了化学变化 |
C.水分子能减弱 和 和 之间的作用力 之间的作用力 |
D. 、 、 分别与水分子形成大小相同的环 分别与水分子形成大小相同的环 |
您最近一年使用:0次
7 . 下列物质的分类正确的是
类别 选项 | 碱 | 盐 | 电解质 |
| A | 火碱 | 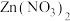 |  |
| B | 纯碱 |  | 熔融 |
| C |  |  | 饱和食盐水 |
| D | KOH |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 油条是我国传统食品,其做法是将明矾[KAl(SO4)2•12H2O]、纯碱、食盐按比例加入温水中,再加入面粉,搅拌成面团,放置,使面团产生气体,形成孔洞,放置过程发生反应:3Na2CO3+KAl(SO4)2•12H2O=3Na2SO4+K2SO4+3CO2↑+2Al(OH)3↓+21H2O。下列有关判断正确的是
| A.明矾属于混合物 |
| B.放置过程发生的反应中,反应物和生成物均为电解质 |
C.KAl(SO4)2在水溶液中的电离方程式为KAl(SO4)2=K++Al3++SO |
D.该反应说明Al3+与CO 不能大量共存 不能大量共存 |
您最近一年使用:0次
9 . 碳酸亚铁( )是生产补血剂的一种原料,实验室以铁屑为原料制备
)是生产补血剂的一种原料,实验室以铁屑为原料制备 的流程如下:
的流程如下:

回答下列问题:
(1)用电离方程式表示 在水中的变化:
在水中的变化:____________________ 。
(2)“气体1”是________ (填化学式);若“溶解”时生成的“气体1”在标准状况下的体积为2.24 L,则参加反应的铁的质量为________ g。
(3)实验室配制100 mL 2mol/L 溶液。
溶液。
①需要18 mol/L浓 的体积为
的体积为________ mL(计算结果保留两位有效数字)。
②下列仪器中,需要的有________ (填标号),还缺少的玻璃仪器为________ (填仪器名称)。

 )是生产补血剂的一种原料,实验室以铁屑为原料制备
)是生产补血剂的一种原料,实验室以铁屑为原料制备 的流程如下:
的流程如下:
回答下列问题:
(1)用电离方程式表示
 在水中的变化:
在水中的变化:(2)“气体1”是
(3)实验室配制100 mL 2mol/L
 溶液。
溶液。①需要18 mol/L浓
 的体积为
的体积为②下列仪器中,需要的有

您最近一年使用:0次
解题方法
10 . 一定温度下,向 溶液中滴加两滴酚酞溶液,然后向
溶液中滴加两滴酚酞溶液,然后向 溶液中匀速滴加
溶液中匀速滴加 溶液,测得电导率随时间变化的曲线如图所示,下列说法错误的是
溶液,测得电导率随时间变化的曲线如图所示,下列说法错误的是

 溶液中滴加两滴酚酞溶液,然后向
溶液中滴加两滴酚酞溶液,然后向 溶液中匀速滴加
溶液中匀速滴加 溶液,测得电导率随时间变化的曲线如图所示,下列说法错误的是
溶液,测得电导率随时间变化的曲线如图所示,下列说法错误的是
A. 内可观察到有白色沉淀产生,溶液红色褪去,电导率减小 内可观察到有白色沉淀产生,溶液红色褪去,电导率减小 |
B.反应至 点,加入 点,加入 溶液的体积为 溶液的体积为 |
C. 电导率降低,说明 电导率降低,说明 不是电解质 不是电解质 |
D. 电导率增大,主要是因为 电导率增大,主要是因为 电离出的离子导电 电离出的离子导电 |
您最近一年使用:0次



