解题方法
1 . 从不同的角度对物质进行分类有利于研究物质的组成与性质.现有以下5种物质:①Cu②NaCl③饱和氯化铁溶液④硝酸银溶液⑤干冰
回答下列问题:
(1)以上物质能导电的有________ (填序号).
(2)以上物质属于电解质的有________ (填序号).
(3)分别写出②、④在水中的电离方程式________ 、________ .
(4)①可溶解在③中,该反应的离子方程式为________________________ .
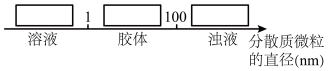
(5)将少量③分别滴加到下列物质中,得到三种分散系 、
、 、
、 .
.

试将 、
、 、
、 符号以及对应的分散质具体的化学式填入下列方框中
符号以及对应的分散质具体的化学式填入下列方框中__________ 。
回答下列问题:
(1)以上物质能导电的有
(2)以上物质属于电解质的有
(3)分别写出②、④在水中的电离方程式
(4)①可溶解在③中,该反应的离子方程式为
(5)将少量③分别滴加到下列物质中,得到三种分散系
 、
、 、
、 .
.
试将
 、
、 、
、 符号以及对应的分散质具体的化学式填入下列方框中
符号以及对应的分散质具体的化学式填入下列方框中
您最近一年使用:0次
名校
解题方法
2 . 下列物质:①NaCl晶体②液态醋酸③铜④蔗糖⑤酒精⑥熔融的KNO3 ⑦液氧⑧硫酸溶液(用编号回答)其中属于电解质的是_______ ;属于非电解质的是_______ 。
您最近一年使用:0次
解题方法
3 . 现有下列物质:①NaCl固体②HCl气体③ 固体④熔融KCl⑤铜⑥稀硫酸⑦CaO⑧
固体④熔融KCl⑤铜⑥稀硫酸⑦CaO⑧ ⑨氨水。
⑨氨水。
(1)上述物质中,属于电解质的是__________ (填序号)。
(2)写出②的水溶液和少量③反应的离子方程式:__________ .
 固体④熔融KCl⑤铜⑥稀硫酸⑦CaO⑧
固体④熔融KCl⑤铜⑥稀硫酸⑦CaO⑧ ⑨氨水。
⑨氨水。(1)上述物质中,属于电解质的是
(2)写出②的水溶液和少量③反应的离子方程式:
您最近一年使用:0次
名校
4 . 现有以下物质:①NaCl晶体;②干冰;③液态的醋酸;④铜;⑤蔗糖;⑥熔融的NaHSO4;⑦氯化氢。请回答下列问题:(填序号)
(1)以上物质能导电的是__________________ ,属于电解质的是______________ ,属于非电解质的是__________ 。
(2)NaHSO4溶于水时的电离方程式为_______________________________ 。
(3)物质⑦具有________________ (填写“氧化性”“还原性”或者“氧化性和还原性”),在反应MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O中,浓盐酸显示的性质是
MnCl2+Cl2↑+2H2O中,浓盐酸显示的性质是_____________ (填序号)。
a.只有还原性 b.还原性和酸性 c.只有氧化性 d.氧化性和酸性
(4)物质④在氧化还原反应中应该只能表现__________ (填“氧化性”或“还原性”)。
(1)以上物质能导电的是
(2)NaHSO4溶于水时的电离方程式为
(3)物质⑦具有
 MnCl2+Cl2↑+2H2O中,浓盐酸显示的性质是
MnCl2+Cl2↑+2H2O中,浓盐酸显示的性质是a.只有还原性 b.还原性和酸性 c.只有氧化性 d.氧化性和酸性
(4)物质④在氧化还原反应中应该只能表现
您最近一年使用:0次
5 . Ⅰ.现有下列物质:①固体氢氧化钡,②石墨棒,③纯醋酸,④液态氯化氢,⑤硫酸氢钾固体,⑥熔融氯化钠,⑦酒精(C2H5OH),⑧碳酸钠粉末。请用序号回答下列问题:
(1)以上物质中能导电的是_______ 。
(2)以上物质中属于电解质的是_______ 。
(3)以上物质中属于非电解质的是_______ 。
Ⅱ.高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止刻蚀液与下层(砷化镓)反应。
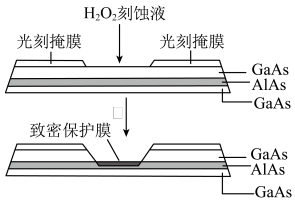
(4)已知:Ga和Al最外层电子数相同,As和N最外层电子数相同。在H2O2与上层GaAs的反应中,As元素的化合价变为+5价,则该反应的氧化剂与还原剂的物质的量之比为_______ 。
(5)配平下列化学方程式_______ 。
_______Cu+_______HNO3(稀)=_______Cu(NO3)2+_______NO↑+_______H2O
(1)以上物质中能导电的是
(2)以上物质中属于电解质的是
(3)以上物质中属于非电解质的是
Ⅱ.高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止刻蚀液与下层(砷化镓)反应。

(4)已知:Ga和Al最外层电子数相同,As和N最外层电子数相同。在H2O2与上层GaAs的反应中,As元素的化合价变为+5价,则该反应的氧化剂与还原剂的物质的量之比为
(5)配平下列化学方程式
_______Cu+_______HNO3(稀)=_______Cu(NO3)2+_______NO↑+_______H2O
您最近一年使用:0次
解题方法
6 . 下列物质中,A.KI(s) B.C2H5OH(l) C.Cl2(g) D.CH3COOH(l) E.BaSO4(s) F.NaHSO4(s) G.石墨(s) H.蔗糖(s) I.NaOH(l)
(1)属于非电解质的是___________ (填字母,下同),属于强电解质的是___________ ,属于弱电解质的是___________ 。
(2)能直接导电的是___________ ,能溶于水且水溶液能导电的是___________ 。
(1)属于非电解质的是
(2)能直接导电的是
您最近一年使用:0次
7 . 二氧化硫是形成酸雨的“罪魁祸首”,为了保护环境,应减少SO2在大气中的排放。请回答下列问题:
(1)SO2与水反应可生成亚硫酸,那么SO2是电解质还是非电解质?_____ 。
(2)工业尾气中的SO2常用NaOH溶液吸收,生成Na2SO3或NaHSO3,写出Na2SO3和NaHSO3的电离方程式。
①Na2SO3:_____ 。
②NaHSO3:_____ 。
(3)SO2在催化剂的作用下可被氧气氧化成SO3,SO3与水反应生成H2SO4。
①SO3是电解质还是非电解质?_____ 。
②O2是电解质还是非电解质?_____ 。
③SO3与NaOH溶液反应可生成NaHSO4.已知NaHSO4=Na++H++ ,则NaHSO4是酸类物质吗?
,则NaHSO4是酸类物质吗?_____ 。
(1)SO2与水反应可生成亚硫酸,那么SO2是电解质还是非电解质?
(2)工业尾气中的SO2常用NaOH溶液吸收,生成Na2SO3或NaHSO3,写出Na2SO3和NaHSO3的电离方程式。
①Na2SO3:
②NaHSO3:
(3)SO2在催化剂的作用下可被氧气氧化成SO3,SO3与水反应生成H2SO4。
①SO3是电解质还是非电解质?
②O2是电解质还是非电解质?
③SO3与NaOH溶液反应可生成NaHSO4.已知NaHSO4=Na++H++
 ,则NaHSO4是酸类物质吗?
,则NaHSO4是酸类物质吗?
您最近一年使用:0次
解题方法
8 . 某兴趣小组同学在测定溶液的导电性实验时,采用如图所示的串联装置,闭合开关时,发现灯泡不亮。
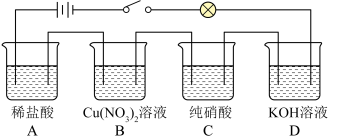
(1)上述四个烧杯中的溶质的电解质类型分别为________________________ 。
(2)上述四个烧杯中________ (填字母)烧杯中的物质发生了电离。
(3)小灯泡不亮的原因是什么______________ ?怎样才能使灯泡亮起来______________ ?
(4)若经过操作灯泡亮起来后,各烧杯等体积溶液中溶质的粒子数目相等,则哪个烧杯的溶液导电能力最强______________ ?

(1)上述四个烧杯中的溶质的电解质类型分别为
(2)上述四个烧杯中
(3)小灯泡不亮的原因是什么
(4)若经过操作灯泡亮起来后,各烧杯等体积溶液中溶质的粒子数目相等,则哪个烧杯的溶液导电能力最强
您最近一年使用:0次
2023高一上·全国·专题练习
9 . 常见的可拆分物质有:
(1)强酸:___________ 。
(2)强碱:___________ 。
(3)可溶性盐:___________ 。
(4)浓盐酸、浓硝酸在离子方程式中___________ ,浓硫酸___________ 。
(1)强酸:
(2)强碱:
(3)可溶性盐:
(4)浓盐酸、浓硝酸在离子方程式中
您最近一年使用:0次
解题方法
10 . 电解质和非电解质
(1)电解质:在水溶液中或熔融状态下能___________ 的___________ 。电解质在水溶液或熔融状态下能产生___________ 的离子。
(2)非电解质:在水溶液中和熔融状态下都___________ 的___________ 。
(1)电解质:在水溶液中或熔融状态下能
(2)非电解质:在水溶液中和熔融状态下都
您最近一年使用:0次



