解题方法
1 . A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有氧化性。下述为相关实验步骤和实验现象:

请回答下列问题:
(1)写出A、B和C的化学式:
A____________ ,B____________ ,C____________ 。
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式:____________________________________________________ 。
(3)写出将SO2气体通入K溶液中发生反应的离子方程式:___________________________________________________ 。
(4)写出由F→H的化学方程式:______________________________ 。

请回答下列问题:
(1)写出A、B和C的化学式:
A
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式:
(3)写出将SO2气体通入K溶液中发生反应的离子方程式:
(4)写出由F→H的化学方程式:
您最近一年使用:0次
名校
2 . 能正确表示下列反应的离子方程式是
| A.用过量石灰乳吸收工业尾气中的SO2: Ca2++2OH-+SO2=CaSO3 ↓+ H2O |
| B.用酸性KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4—+6H++5H2O2=2Mn2++5O2 ↑+8H2O |
C.用铜做电极电解NaCl溶液:2C1—+2H2O H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
| D.将 Fe2O3加入到 HI 溶液中:Fe2O3+ 6H+=2Fe3+ +3H2O |
您最近一年使用:0次
2016-07-04更新
|
1009次组卷
|
10卷引用:2018届高三一轮复习化学:微考点9-离子方程式的正误判断
解题方法
3 . 化学实验室产生的废液中含有大量会污染环境的物质,为了保护环境,化学实验室产生的废液必须经处理后才能排放。某化学实验室产生的酸性废液中含有Fe3+、Cu2+、Ba2+三种金属阳离子和Cl-一种阴离子,实验室设计了下述方案对废液进行处理,以回收金属并测定含量,保护环境。
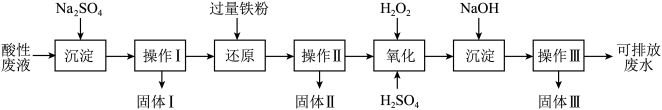
已知实验中处理的酸性废液的体积为1L,用pH计测定出其中H+物质的量浓度为0.10mol/L。
请回答下列问题:
(1)实验中操作I、Ⅱ、Ⅲ的方法相同,操作步骤依次为过滤、_________ 、干燥。
(2)“氧化”步骤所得溶液颜色为棕黄色,该反应的离子方程式为:__________ 。
(3)实验中称量固体I 的质量为4.66g,固体II 的质量为15.2g,用足量的稀硝酸溶解固体Ⅱ后产生了标准状况下的无色气体4.48L,则固体Ⅱ中金属铜的质量为________ g。
(4)实验中将固体Ⅲ进行充分灼烧,使用仪器除了酒精灯、三脚架、泥三角、玻璃棒外,还有_____ (填名称)。最后得到的红棕色固体质量为40.0g,则原溶液中氯离子的物质的量浓度为________ (写出计算过程)。

已知实验中处理的酸性废液的体积为1L,用pH计测定出其中H+物质的量浓度为0.10mol/L。
请回答下列问题:
(1)实验中操作I、Ⅱ、Ⅲ的方法相同,操作步骤依次为过滤、
(2)“氧化”步骤所得溶液颜色为棕黄色,该反应的离子方程式为:
(3)实验中称量固体I 的质量为4.66g,固体II 的质量为15.2g,用足量的稀硝酸溶解固体Ⅱ后产生了标准状况下的无色气体4.48L,则固体Ⅱ中金属铜的质量为
(4)实验中将固体Ⅲ进行充分灼烧,使用仪器除了酒精灯、三脚架、泥三角、玻璃棒外,还有
您最近一年使用:0次
4 . 下列指定反应的离子方程式正确的是
| A.向NaAlO2溶液中通入过量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| B.在酸性条件下,用H2O2将I-氧化为I2:H2O2+2I-+2H+=I2+2H2O |
| C.向FeBr2溶液中通入足量氯气:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
| D.NaHCO3溶液中加入少量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O |
您最近一年使用:0次
2016-09-19更新
|
215次组卷
|
3卷引用:2018届高三一轮复习化学:微考点9-离子方程式的正误判断



