名校
解题方法
1 .  俗称大苏打、海波,易溶于水,在中性或碱性环境中能稳定存在,食品工业用作螯合剂、抗氧化剂,医药工业用作洗涤剂、消毒剂。下列说法中根据实验目的、实验操作或现象得到的相关离子方程式正确的是
俗称大苏打、海波,易溶于水,在中性或碱性环境中能稳定存在,食品工业用作螯合剂、抗氧化剂,医药工业用作洗涤剂、消毒剂。下列说法中根据实验目的、实验操作或现象得到的相关离子方程式正确的是
 俗称大苏打、海波,易溶于水,在中性或碱性环境中能稳定存在,食品工业用作螯合剂、抗氧化剂,医药工业用作洗涤剂、消毒剂。下列说法中根据实验目的、实验操作或现象得到的相关离子方程式正确的是
俗称大苏打、海波,易溶于水,在中性或碱性环境中能稳定存在,食品工业用作螯合剂、抗氧化剂,医药工业用作洗涤剂、消毒剂。下列说法中根据实验目的、实验操作或现象得到的相关离子方程式正确的是| 选项 | 实验目的 | 实验操作或现象 | 相关离子方程式 |
| A | 制备 | 实验室用 通入 通入 和 和 的混合溶液中来制备 的混合溶液中来制备 | 4SO2+2S2-+CO =3S2O =3S2O +CO2 +CO2 |
| B | 检验硫代硫酸钠氧化变质可能混有的 | 取少量样品溶于水,先加入过量稀盐酸,再滴加 溶液,有沉淀生成 溶液,有沉淀生成 | SO +Ba2+=BaSO4↓ +Ba2+=BaSO4↓ |
| C | 探究温度对硫代硫酸钠与硫酸反应速率的影响 | 分别将两种反应溶液先混合,再水浴加热至反应要求温度,测得该温度下的反应速率 | 2S2O +2H+=S↓+SO +2H+=S↓+SO +2H2O +2H2O |
| D | 用过量硫代硫酸钠除去水中溶解的氯气 | 黄绿色褪去 | S2O +4Cl2+5H2O=2SO +4Cl2+5H2O=2SO +8Cl-+10H+ +8Cl-+10H+ |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-02-11更新
|
2385次组卷
|
7卷引用:湖南省四大名校名师团队2022-2023学年高三下学期2月模拟冲刺卷(1)化学试题
湖南省四大名校名师团队2022-2023学年高三下学期2月模拟冲刺卷(1)化学试题(已下线)素养卷09 微型原理验证方案设计-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题04 离子反应湖南省部分学校2022-2023学年高三下学期开学考试化学试题湖南省衡阳市第八中学2023-2024学年高三上学期开学(暑假检测)化学试题江苏省靖江高级中学、华罗庚中学2023-2024学年高三上学期第一次阶段考试化学试题江西省新余市第一中学2023-2024学年高三上学期开学考试化学试题
名校
2 . 下表所示装置能达到实验目的,且相应化学用语也正确的是
| 选项 | A | B | C | D |
| 实验目的 | 测定醋酸与氢氧化钠反应的反应热 | 验证铁的吸氧腐蚀 | 测定反应速率 | 制备并收集少量NO |
| 装置 | 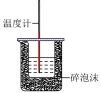 |  | 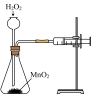 | 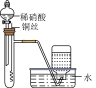 |
A.A中的离子方程式为: 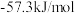 |
B.B中碳粉表面的电极反应式为: |
C.C中的化学方程式为: |
D.D中的离子方程式为: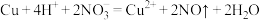 |
您最近半年使用:0次
名校
解题方法
3 . 比较乙酸、碳酸、苯酚的酸性强弱的实验如图所示,下列说法正确的是
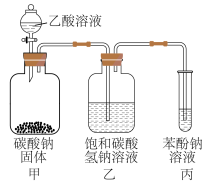

A.甲中反应:2H++CO =H2O+CO2↑ =H2O+CO2↑ |
| B.乙中的NaHCO3溶液可改为NaOH溶液 |
| C.丙中出现浑浊说明碳酸的酸性强于苯酚的 |
| D.去除乙装置仍可达到该实验目的 |
您最近半年使用:0次
2022-11-05更新
|
389次组卷
|
4卷引用:天津市河西区2022-2023学年高三上学期期中质量调查化学试题
4 . 硫酸四氨合铜晶体( )常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备
)常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备 的流程如下:
的流程如下:
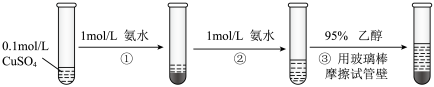
请回答:
(1)写出过程②发生反应的离子方程式_______ 。
(2)过程③加入95%乙醇的作用是_______ 。
(3)根据①→②→③的现象,给出相应微粒与 结合由弱到强的排序
结合由弱到强的排序_______ 。
(4) 具有对称的空间构型,若其中两个
具有对称的空间构型,若其中两个 被两个
被两个 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为_______ 。
(5)下列说法正确的是_______。
 )常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备
)常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备 的流程如下:
的流程如下:
请回答:
(1)写出过程②发生反应的离子方程式
(2)过程③加入95%乙醇的作用是
(3)根据①→②→③的现象,给出相应微粒与
 结合由弱到强的排序
结合由弱到强的排序(4)
 具有对称的空间构型,若其中两个
具有对称的空间构型,若其中两个 被两个
被两个 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为(5)下列说法正确的是_______。
A.③中发生反应的离子方程式为: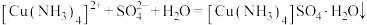 |
| B.③中用玻璃棒摩擦器壁可以促进晶体析出 |
C. 晶体中存在共价键、配位键、离子键和氢键 晶体中存在共价键、配位键、离子键和氢键 |
D.硫酸四氨合铜晶体在水中的电离方程式为: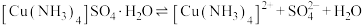 |
您最近半年使用:0次
解题方法
5 . 下列反应的现象对应的离子方程式正确的是
| A.澄清石灰水跟稀硝酸反应:Ca(OH)2+2H+=Ca2++2H2O |
| B.CaCO3与稀HCl反应制备CO2:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C.氢氧化钡溶液中加入硫酸至中性: H++OH-=H2O |
| D.向稀硫酸溶液中投入铁粉:2Fe+6H+=2Fe3++3H2↑ |
您最近半年使用:0次
名校
解题方法
6 . 宏观辨识、微观探析和符号表征是体现化学学科特征的思维方式。某化学兴趣小组设计实验,探究离子反应及氧化还原反应的本质。回答下列问题:

Ⅰ.离子反应
(1)向 溶液中滴入几滴酚酞溶液(装置如图所示),接通电源,向该溶液中滴入
溶液中滴入几滴酚酞溶液(装置如图所示),接通电源,向该溶液中滴入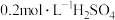 溶液。
溶液。
①接通电源前,能说明 在水中电离的实验现象为
在水中电离的实验现象为_____ 。
②随着 溶液的滴入,观察到烧杯中溶液红色逐渐褪去,产生白色沉淀,小灯泡亮度变暗,这些现象说明该反应的微观本质是
溶液的滴入,观察到烧杯中溶液红色逐渐褪去,产生白色沉淀,小灯泡亮度变暗,这些现象说明该反应的微观本质是 和
和 浓度降低,该反应的离子方程式为
浓度降低,该反应的离子方程式为_____ 。
(2)向 溶液中逐滴滴入
溶液中逐滴滴入 盐酸,测定溶液电导率的变化如图所示。
盐酸,测定溶液电导率的变化如图所示。

① 点恰好完全反应,此时溶液中存在的主要微粒有
点恰好完全反应,此时溶液中存在的主要微粒有 、
、_____ 。
②下列化学反应的离子方程式与 溶液和稀盐酸反应相同的是
溶液和稀盐酸反应相同的是_____ (填标号)。
A. 溶液和稀硫酸反应
溶液和稀硫酸反应
B.氨水和稀盐酸反应
C. 溶液和
溶液和 溶液反应
溶液反应
D.澄清石灰水和稀硝酸反应
Ⅱ.氧化还原反应
(3)部分含硫物质如图所示,其中 和
和 是大气污染物。这些物质之间的相互转化为工业生产和处理环境问题提供了理论支持。
是大气污染物。这些物质之间的相互转化为工业生产和处理环境问题提供了理论支持。
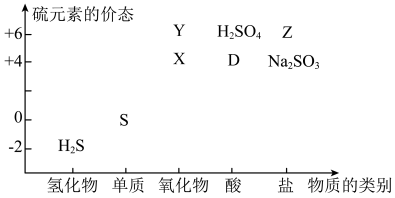
已知 可发生下列过程:
可发生下列过程: ,其中反应①的离子方程式是
,其中反应①的离子方程式是_____ ,若欲将X转化成“安全物质”Z,使其对环境的影响最小,需加入_____ (填标号)。
A.酸性物质 B.碱性物质 C.氧化剂 D.还原剂
 转化为
转化为 可以说明氧化还原反应的本质是发生了
可以说明氧化还原反应的本质是发生了_____ 。

Ⅰ.离子反应
(1)向
 溶液中滴入几滴酚酞溶液(装置如图所示),接通电源,向该溶液中滴入
溶液中滴入几滴酚酞溶液(装置如图所示),接通电源,向该溶液中滴入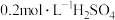 溶液。
溶液。①接通电源前,能说明
 在水中电离的实验现象为
在水中电离的实验现象为②随着
 溶液的滴入,观察到烧杯中溶液红色逐渐褪去,产生白色沉淀,小灯泡亮度变暗,这些现象说明该反应的微观本质是
溶液的滴入,观察到烧杯中溶液红色逐渐褪去,产生白色沉淀,小灯泡亮度变暗,这些现象说明该反应的微观本质是 和
和 浓度降低,该反应的离子方程式为
浓度降低,该反应的离子方程式为(2)向
 溶液中逐滴滴入
溶液中逐滴滴入 盐酸,测定溶液电导率的变化如图所示。
盐酸,测定溶液电导率的变化如图所示。
①
 点恰好完全反应,此时溶液中存在的主要微粒有
点恰好完全反应,此时溶液中存在的主要微粒有 、
、②下列化学反应的离子方程式与
 溶液和稀盐酸反应相同的是
溶液和稀盐酸反应相同的是A.
 溶液和稀硫酸反应
溶液和稀硫酸反应B.氨水和稀盐酸反应
C.
 溶液和
溶液和 溶液反应
溶液反应D.澄清石灰水和稀硝酸反应
Ⅱ.氧化还原反应
(3)部分含硫物质如图所示,其中
 和
和 是大气污染物。这些物质之间的相互转化为工业生产和处理环境问题提供了理论支持。
是大气污染物。这些物质之间的相互转化为工业生产和处理环境问题提供了理论支持。
已知
 可发生下列过程:
可发生下列过程: ,其中反应①的离子方程式是
,其中反应①的离子方程式是A.酸性物质 B.碱性物质 C.氧化剂 D.还原剂
 转化为
转化为 可以说明氧化还原反应的本质是发生了
可以说明氧化还原反应的本质是发生了
您最近半年使用:0次
2023-10-02更新
|
90次组卷
|
4卷引用:甘肃省酒泉市2023-2024学年高三上学期10月联考化学试题
名校
7 . 下列离子方程式书写正确,且能完整解释对应实验现象的是
A.氧化铁溶于氢碘酸: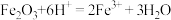 |
B.苯酚钠溶液中通入 ,出现白色浑浊:2 ,出现白色浑浊:2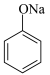 +CO2+H2O +CO2+H2O 2 2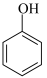 +Na2CO3 +Na2CO3 |
C.四氯化钛的浓溶液制备水合二氧化钛: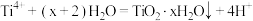 |
D.碳酸氢镁溶液与过量石灰水反应: |
您最近半年使用:0次
2023-09-02更新
|
99次组卷
|
2卷引用:重庆市七校2023-2024学年高三上学期开学考试化学试题
名校
8 . 硅酸( )是一种难溶于水的弱酸,从溶液中析出时常形成凝胶状沉淀。实验室常用
)是一种难溶于水的弱酸,从溶液中析出时常形成凝胶状沉淀。实验室常用 溶液制备硅酸。某小组同学进行了如下实验;
溶液制备硅酸。某小组同学进行了如下实验;
下列结论不正确的是
 )是一种难溶于水的弱酸,从溶液中析出时常形成凝胶状沉淀。实验室常用
)是一种难溶于水的弱酸,从溶液中析出时常形成凝胶状沉淀。实验室常用 溶液制备硅酸。某小组同学进行了如下实验;
溶液制备硅酸。某小组同学进行了如下实验;| 编号 | Ⅰ | Ⅱ |
| 实验 | 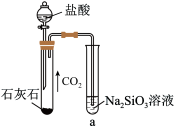 | 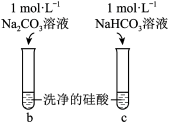 |
| 现象 | a中产生凝胶状沉淀 | b中凝胶状沉淀溶解,c中无明显变化 |
A.盐酸与石灰石反应离子反应方程式;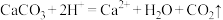 |
B.由Ⅰ不能说明酸性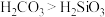 |
C.由Ⅱ可知,同浓度时 溶液的碱性强于 溶液的碱性强于 溶液 溶液 |
D.向 溶液中通入过量 溶液中通入过量 ,发生反应: ,发生反应: |
您最近半年使用:0次
解题方法
9 . 下列解释相应实验现象或事实的离子方程式中不正确的是
| A.Na加入滴有酚酞的水中溶液变红:2Na+2H2O=2Na++2OH-+H2↑ |
| B.氢氧化钠溶液可用于制备氢氧化铁:Fe3++3OH-=Fe(OH)3↓ |
C.向铁粉中加入稀硫酸可得到硫酸亚铁溶液:Fe+2H++SO =FeSO4+H2↑ =FeSO4+H2↑ |
D.铜粉与稀HNO3反应产生无色气体:3Cu+8H++2NO =3Cu2++2NO↑+4H2O =3Cu2++2NO↑+4H2O |
您最近半年使用:0次
名校
解题方法
10 . 下列离子方程式能用来解释相应实验现象的是
| 实验现象 | 离子方程式 | |
| A | 用氨水吸收烟气中少量的 | 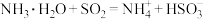 |
| B |  溶液和稍过量的 溶液和稍过量的 制备 制备 | 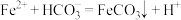 |
| C | 向 悬浊液中滴加 悬浊液中滴加 溶液,沉淀溶解 溶液,沉淀溶解 |  |
| D | FeO溶于稀硝酸 |  |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2022-12-30更新
|
273次组卷
|
3卷引用:北京市八一学校2022-2023学年高三上学期12月月考化学试题



