1 . 已知氧化性:BrO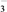 >ClO
>ClO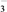 >Cl2>IO
>Cl2>IO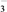 >I2。现将饱和氯水逐滴滴入KI淀粉溶液中至过量。
>I2。现将饱和氯水逐滴滴入KI淀粉溶液中至过量。
(1)可观察到的现象是
①_________________________________________________ ;
②_________________________________________________ 。
(2)写出有关反应的离子方程式:
①___________________________________________ ;
②___________________________________________ 。
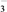 >ClO
>ClO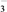 >Cl2>IO
>Cl2>IO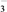 >I2。现将饱和氯水逐滴滴入KI淀粉溶液中至过量。
>I2。现将饱和氯水逐滴滴入KI淀粉溶液中至过量。(1)可观察到的现象是
①
②
(2)写出有关反应的离子方程式:
①
②
您最近一年使用:0次
2017-09-23更新
|
177次组卷
|
2卷引用:2018届高三一轮复习化学:考点12-氧化性、还原性强弱的比较
名校
2 . 向含有0.2 mol FeI2溶液中加入a mol Br2。下列叙述不正确的是
| A.a=0.1 时,发生的反应为 2I-+Br2=I2+2Br- |
| B.a=0.25 时,发生的反应为 4Fe2++6I-+5Br2=4Fe3++3I2+10Br- |
| C.溶液中的I-一半被氧化时,c(I-)∶c(Br-)=l∶l |
| D.0.2<a<0.3时(不考虑碘与水反应),溶液中各离子浓度的关系为:2c(Fe2+)+ 3c(Fe3+)+c(H+)=c(Br-)+c(OH-) |
您最近一年使用:0次
2016-10-21更新
|
659次组卷
|
17卷引用:2018届高三一轮复习化学:考点14-氧化还原反应的计算
2018届高三一轮复习化学:考点14-氧化还原反应的计算2016届辽宁省部分重点高中协作校高三下模拟理综化学试卷2015-2016学年河北省定州中学高二6月月考化学试卷2015-2016学年云南临沧一中高二下学期期末考试化学卷2017届辽宁省东北育才学校高三上学期第一次模拟化学试卷2017届福建省仙游一中高三上第一次月考化学试卷2017届辽宁省沈阳东北育才学校高三上模拟一化学试卷黑龙江省双鸭山市第一中学2016-2017学年高二下学期期末考试化学试题河北省武邑中学2018届高三上学期第一次月考化学试题河南省南阳市第一中学2018届高三上学期第二次考试化学试题河北省馆陶县第一中学2018届高三上学期第一次月考化学试题河北省邱县第一中学2018届高三上学期第一次月考化学试题山东省郓城实验中学2018届高三10月月考化学试题甘肃省兰州第一中学2018届高三上学期第二次月考(9月)化学试题湖南三湘名校教育联盟2018届高三第一次大联考化学试题湖南省茶陵县第三中学2020届高三第三次月考化学试题宁夏银川市唐徕中学2023-2024学年高三上学期期中考试化学试题
3 . 将浓盐酸滴入KMnO4溶液,产生黄绿色气体,溶液的紫红色褪去,向反应后的溶液中加入NaBiO3,溶液又变为紫红色,BiO3-反应后变为无色的Bi3+。据此判断下列说法正确的是
| A.滴加盐酸时,HCl是还原剂,Cl2是还原产物 |
| B.已知Bi为第ⅤA族元素,上述实验说明Bi具有较强的非金属性 |
| C.若有0.1 mol NaBiO3参加了反应,则整个过程转移电子0.4NA |
| D.此实验条件下,物质的氧化性:KMnO4 > NaBiO3 > Cl2 |
您最近一年使用:0次
2016-09-14更新
|
414次组卷
|
7卷引用:2018届高三一轮复习化学:考点12-氧化性、还原性强弱的比较
名校
4 . 已知酸性条件下有以下反应关系: ①KBrO3能将KI氧化成I2或KIO3,其本身被还原为Br2。②Br2能将I-氧化为I2。③KIO3能将I-氧化为I2,也能将Br-氧化为Br2,其本身被还原为I2。现向含有1 mol KI的硫酸溶液中加入含amol KBrO3的溶液,a的取值不同,所得产物也不同。下列判断正确的是:
| 编号 | a的取值范围 | 产物的化学式 |
| ① | a≤1/6 | I2、Br- |
| ② | 1/6<a<1/5 | I2、Br-、Br2 |
| ③ | 1/5<a<6/5 | I2、IO3-、Br2 |
| ④ | a≥6/5 | IO3-、Br2 |
| A.①③④ | B.②③④ | C.①②③④ | D.①④ |
您最近一年使用:0次
2015-09-28更新
|
313次组卷
|
4卷引用:2018届高三一轮复习化学:考点14-氧化还原反应的计算



