解题方法
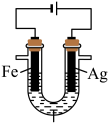
1 . 某兴趣小组探究电镀银实验。回答下列问题:
I.实验准备。
(1)用 固体配制
固体配制 溶液,不需要使用的仪器是
溶液,不需要使用的仪器是___________ (填字母)。___________ 。
Ⅱ.探究银离子对镀层的影响。
【提出猜想】
镀层外观与 浓度有关。
浓度有关。
【查阅资料】
络合反应: ,
, 。
。
【设计实验】
【问题讨论】
(3)实验a中,溶液变红色的可能原因是 和
和___________ (用离子方程式表示,已知氧化性: )。
)。
(4)①实验a、b的阴极都伴随有气泡,其原因是___________ (写电极反应式)。
②实验b比实验a产生的镀层光亮、致密,其原理是___________ 。
③一段时间后,实验b中 平衡不移动,其原因是
平衡不移动,其原因是___________ 。
【实验结论】
其他条件不变, 浓度很小时,银镀层光亮、致密。
浓度很小时,银镀层光亮、致密。
Ⅲ.探究温度、含量对镀层的影响。
表1:其他条件不变,与
 溶液等体积混合的溶液中含量对镀层外观的影响。
溶液等体积混合的溶液中含量对镀层外观的影响。
表2:其他条件不变,温度对镀层外观的影响。
(5)表1中 含量为
含量为 时,镀层模糊、无光泽的原因是
时,镀层模糊、无光泽的原因是___________ ;
表2中温度为 时镀层光亮不均匀的主要原因是
时镀层光亮不均匀的主要原因是___________ 。
Ⅳ.探究新配方电镀银。
由于电镀液使用氰化钾,在电镀过程中会产生有毒气体,以及废液含剧毒的氰化物,不符合环境要求。由 溶液和
溶液和 溶液组成电镀液也可以得到光亮、致密的镀层。
溶液组成电镀液也可以得到光亮、致密的镀层。
(6)使用新配方可以达到同样的目的,其原理是___________ 。已知: 。
。
I.实验准备。
(1)用
 固体配制
固体配制 溶液,不需要使用的仪器是
溶液,不需要使用的仪器是A. B.
B.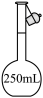 C.
C. D.
D.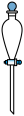 E.
E.
Ⅱ.探究银离子对镀层的影响。
【提出猜想】
镀层外观与
 浓度有关。
浓度有关。【查阅资料】
络合反应:
 ,
, 。
。【设计实验】
| 实验 | 装置 | 现象 |
| a |
 的 的 溶液(含少量 溶液(含少量 ) ) | 阴极表面有疏松的黑色物质生成并伴随有无色气泡,一段时间后,取阴极区电解质溶液于试管,滴加 溶液,溶液变为红色。 溶液,溶液变为红色。 |
| b |
 的 的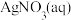 与过量 与过量 混合(含少量 混合(含少量 ) ) | 阴极表面有光亮、致密的银白色物质生成,仍然有少量无色气泡。一段时间后,取少量阴极区溶液于试管,滴加 溶液,溶液不变红。 溶液,溶液不变红。 |
(3)实验a中,溶液变红色的可能原因是
 和
和 )。
)。(4)①实验a、b的阴极都伴随有气泡,其原因是
②实验b比实验a产生的镀层光亮、致密,其原理是
③一段时间后,实验b中
 平衡不移动,其原因是
平衡不移动,其原因是【实验结论】
其他条件不变,
 浓度很小时,银镀层光亮、致密。
浓度很小时,银镀层光亮、致密。Ⅲ.探究温度、含量对镀层的影响。
表1:其他条件不变,与

 溶液等体积混合的溶液中含量对镀层外观的影响。
溶液等体积混合的溶液中含量对镀层外观的影响。 含量( 含量( ) ) | 镀层外观表象 |
| 10 | 镀层模糊,无光泽 |
| 25 | 镀层呈雾状,光泽不足 |
| 50 | 镀层光亮、致密 |
温度/ | 镀层外观表象 |
| 25 | 光亮 |
| 35 | 光亮 |
| 40 | 光亮 |
| 55 | 光亮不均匀 |
(5)表1中
 含量为
含量为 时,镀层模糊、无光泽的原因是
时,镀层模糊、无光泽的原因是表2中温度为
 时镀层光亮不均匀的主要原因是
时镀层光亮不均匀的主要原因是Ⅳ.探究新配方电镀银。
由于电镀液使用氰化钾,在电镀过程中会产生有毒气体,以及废液含剧毒的氰化物,不符合环境要求。由
 溶液和
溶液和 溶液组成电镀液也可以得到光亮、致密的镀层。
溶液组成电镀液也可以得到光亮、致密的镀层。(6)使用新配方可以达到同样的目的,其原理是
 。
。
您最近一年使用:0次
2024-04-16更新
|
329次组卷
|
5卷引用:2024届青海省西宁市大通县高三下学期第二次模拟考试理科综合试题-高中化学
2024届青海省西宁市大通县高三下学期第二次模拟考试理科综合试题-高中化学2024届青海省玉树州高三下学期第四次联考理综试题-高中化学2024届陕西省商洛市高三下学期第三次尖子生学情诊断考试理综试题-高中化学2024届河南省TOP二十名校联考高三下学期5月猜题(一)理科综合试卷-高中化学(已下线)压轴题12?化学实验综合题(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
2 . 治理氮氧化物(NOx)的污染是化学研究的重要课题之一。NO能被灼烧的铁粉还原为N2,同时生成同时生成FeO,利用下列装置模拟该反应。

已知:①浓硝酸可氧化NO;②NaOH溶液能与NO2反应,不与NO反应。
(1)上述装置接口的连接顺序为a→__________ (按气流方向,用小写字母表示)。
(2)装置D的作用是___________________ 。
(3)装置E中反应的化学方程式为___________________ 。
(4)打开分液漏斗活塞,烧瓶中观察到的实验现象有_____________________ 。
(5)实验室常用NaOH溶液吸收多余的氮氧化物(NOx):NO+NO2+2NaOH=2NaNO2+H2O。设计实验验证产物NaNO2既有氧化性又有还原性。
限选试剂:稀硫酸、KI-淀粉溶液、双氧水、酸性高锰酸钾溶液
(6)最终得到的亚硝酸钠(NaNO2)外观与食盐非常相似,毒性较强。
已知①Ksp(AgNO2) =2.0×10-8,Ksp(AgCl) =1.8×10-10;
② Ka(HNO2) =5.1×10-4。
若鉴别NaNO2和NaCl两种固体,实验方法是__________________________ (试剂自选)。

已知:①浓硝酸可氧化NO;②NaOH溶液能与NO2反应,不与NO反应。
(1)上述装置接口的连接顺序为a→
(2)装置D的作用是
(3)装置E中反应的化学方程式为
(4)打开分液漏斗活塞,烧瓶中观察到的实验现象有
(5)实验室常用NaOH溶液吸收多余的氮氧化物(NOx):NO+NO2+2NaOH=2NaNO2+H2O。设计实验验证产物NaNO2既有氧化性又有还原性。
限选试剂:稀硫酸、KI-淀粉溶液、双氧水、酸性高锰酸钾溶液
实验步骤 | 实验操作 | 现象 | 实验结论 |
1 | NaNO2具有氧化性 | ||
2 | NaNO2具有还原性 |
已知①Ksp(AgNO2) =2.0×10-8,Ksp(AgCl) =1.8×10-10;
② Ka(HNO2) =5.1×10-4。
若鉴别NaNO2和NaCl两种固体,实验方法是
您最近一年使用:0次
名校
解题方法
3 . 肼(N2H4)的熔点2.0℃、沸点113.5℃,极易溶于水,在碱性介质中具有还原性。在强碱性介质中,用次氯酸钠氧化尿素[CO(NH2)2]可得粗肼,再经蒸馏得到肼溶液。回答下列问题:
I.制备NaClO强碱性溶液
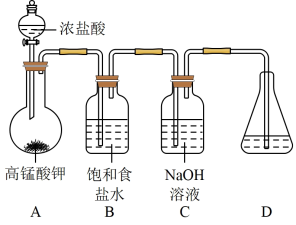
(1)在加入实验药品之前必须进行的操作是_______ 。
(2)A为氯气发生装置,A中反应的化学方程式是_______ 。
(3)次氯酸钠高于35℃容易分解。制备NaClO 强碱性溶液时需要注意的两个关键问题是_______ 。
II.制备N2H4

(4)仪器F的名称是_______ 。
(5)通入N2目的是_______ 。
(6)次氯酸钠氧化尿素的温度一般控制在105~108℃。E中制得肼的离子方程式为_______ .。
(7)向三颈烧瓶中加入NaClO强碱性溶液应当_______ . (填“一次大量”或“分批少量”)加入,充分反应后制得粗肼。蒸馏提纯时应调节控温槽的温度略高于_______ ℃,得到肼溶液。
I.制备NaClO强碱性溶液

(1)在加入实验药品之前必须进行的操作是
(2)A为氯气发生装置,A中反应的化学方程式是
(3)次氯酸钠高于35℃容易分解。制备NaClO 强碱性溶液时需要注意的两个关键问题是
II.制备N2H4

(4)仪器F的名称是
(5)通入N2目的是
(6)次氯酸钠氧化尿素的温度一般控制在105~108℃。E中制得肼的离子方程式为
(7)向三颈烧瓶中加入NaClO强碱性溶液应当
您最近一年使用:0次
2021-03-05更新
|
585次组卷
|
3卷引用:青海省西宁市2021届高三复习检测一(一模)理科综合化学试题