23-24高一下·全国·课前预习
1 . 氨可在加热条件下和氧化铜反应生成铜和氮气,反应的化学方程式为____ 。
您最近一年使用:0次
2 . 浓硝酸可以氧化非金属单质,如加热条件下可将C氧化为CO2,同时生成红棕色气体,反应的化学方程式为________________________ ,体现浓硝酸的________ 性。
您最近一年使用:0次
解题方法
3 . 利用绿矾(FeSO4·7H2O)对某工厂废水(含有强氧化性离子Cr2O )进行处理。
)进行处理。
(1)工业上还可用空气、水、黄铁矿(主要成分为FeS2)来制取FeSO4。已知该反应除生成硫酸亚铁外,还生成一种中学化学常见的强酸,试写出该反应的化学方程式:_______________________ 。
(2)请配平下列离子方程式:______ 。
Fe2++ Cr2O +
+  = Fe3++ Cr3++ H2O
= Fe3++ Cr3++ H2O
 )进行处理。
)进行处理。(1)工业上还可用空气、水、黄铁矿(主要成分为FeS2)来制取FeSO4。已知该反应除生成硫酸亚铁外,还生成一种中学化学常见的强酸,试写出该反应的化学方程式:
(2)请配平下列离子方程式:
Fe2++ Cr2O
 +
+  = Fe3++ Cr3++ H2O
= Fe3++ Cr3++ H2O
您最近一年使用:0次
4 . 配平下列离子方程式。
① Fe3++ SO2+ H2O= Fe2++ SO + H+
+ H+_____ 。
② C2O + MnO
+ MnO + H+= CO2↑+ Mn2++ H2O
+ H+= CO2↑+ Mn2++ H2O_____ 。
① Fe3++ SO2+ H2O= Fe2++ SO
 + H+
+ H+② C2O
 + MnO
+ MnO + H+= CO2↑+ Mn2++ H2O
+ H+= CO2↑+ Mn2++ H2O
您最近一年使用:0次
5 . NO是大气污染物之一、目前有一种治理方法是在400℃左右、有催化剂存在的条件下,使 与NO反应生成无污染的
与NO反应生成无污染的 和
和 。请写出该反应的化学方程式。
。请写出该反应的化学方程式。___________
 与NO反应生成无污染的
与NO反应生成无污染的 和
和 。请写出该反应的化学方程式。
。请写出该反应的化学方程式。
您最近一年使用:0次
名校
解题方法
6 . 某离子反应中涉及H2O、ClO-、NH 、H+、N2、Cl-六种微粒。其中N2的分子数随时间变化的曲线如图所示。下列判断正确的是( )
、H+、N2、Cl-六种微粒。其中N2的分子数随时间变化的曲线如图所示。下列判断正确的是( )

 、H+、N2、Cl-六种微粒。其中N2的分子数随时间变化的曲线如图所示。下列判断正确的是( )
、H+、N2、Cl-六种微粒。其中N2的分子数随时间变化的曲线如图所示。下列判断正确的是( )
| A.该反应的还原剂是Cl- |
| B.每生成1个N2分子,转移3个电子 |
| C.参与反应的氧化剂与还原剂的个数比为2:3 |
| D.反应后溶液的酸性明显增强 |
您最近一年使用:0次
2020-10-25更新
|
793次组卷
|
5卷引用:专题强化练3 氧化还原反应方程式的书写与配平
解题方法
7 . 下列有关过氧化氢跟酸性高锰酸钾溶液反应的化学方程式正确的是
A. |
B.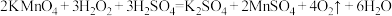 |
C.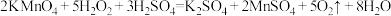 |
D.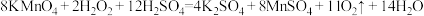 |
您最近一年使用:0次
8 . (1)工业上利用 和
和 反应来制取单质
反应来制取单质 。
。
①配平化学方程式:________ 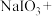
____________  =
=_______ 
________ 
________ 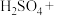
_______ 
②该反应中还原剂是________ (填化学式),_____ (填元素名称)元素被还原,生成1mol氧化产物转移的电子数目为________  (设
(设 为阿伏加 德罗常数的值)。
为阿伏加 德罗常数的值)。
(2)已知: 、
、 、
、 、
、 和一些未知物组成的氧化还原反应中
和一些未知物组成的氧化还原反应中 是氧化产物。该反应中还原性:
是氧化产物。该反应中还原性:
________ (填“>”或“<”) ,写出配平后的离子方程式:
,写出配平后的离子方程式:___________ 。
 和
和 反应来制取单质
反应来制取单质 。
。①配平化学方程式:
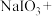
 =
=

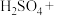

②该反应中还原剂是
 (设
(设 为阿伏加 德罗常数的值)。
为阿伏加 德罗常数的值)。(2)已知:
 、
、 、
、 、
、 和一些未知物组成的氧化还原反应中
和一些未知物组成的氧化还原反应中 是氧化产物。该反应中还原性:
是氧化产物。该反应中还原性:
 ,写出配平后的离子方程式:
,写出配平后的离子方程式:
您最近一年使用:0次
20-21高一·全国·课时练习
9 . 在工业上次磷酸(H3PO2)常用于化学镀银,发生的反应如下:Ag++H3PO2+H2O→Ag↓+H3PO4+H+,请回答下列问题:
(1)H3PO2中,P元素的化合价为_____ ;该反应中,H3PO2被_______ (填“氧化”或“还原”)。
(2)配平该离子方程式:______________ 。
(3)H3PO2是一元弱酸,写出其与足量NaOH溶液反应的离子方程式:___________ 。
(1)H3PO2中,P元素的化合价为
(2)配平该离子方程式:
(3)H3PO2是一元弱酸,写出其与足量NaOH溶液反应的离子方程式:
您最近一年使用:0次
20-21高一·全国·课时练习
解题方法
10 . +6价铬的化合物毒性较大,常用NaHSO3将酸性废液中的 还原成Cr3+,该反应的离子方程式为
还原成Cr3+,该反应的离子方程式为___________ 。
 还原成Cr3+,该反应的离子方程式为
还原成Cr3+,该反应的离子方程式为
您最近一年使用:0次



