名校
解题方法
1 . 下列反应的离子方程式正确的是
A.酸性 溶液与 溶液与 反应: 反应: |
B. 溶液与 溶液与 溶液反应: 溶液反应: |
C. 溶液与NaOH溶液混合: 溶液与NaOH溶液混合: |
D.向水中通入 : : |
您最近一年使用:0次
2022-11-14更新
|
106次组卷
|
2卷引用:福建省三明第一中学2023-2024学年高一上学期期中考试化学试题
解题方法
2 . 为验证木炭与浓硫酸反应生成的气体M含有CO2和SO2,可按下图进行实验。各装置中可供选择的试剂是:①澄清石灰水,②品红溶液,③酸性高锰酸钾溶液。判断各装置所盛试剂后,请回答:
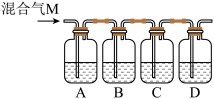
(1)A中所盛放的试剂是_______ (填写试剂序号)。
(2)B中的实验现象_______ ,B装置的作用是_______ 。
(3)C中所盛试剂是_______ (填写试剂序号),C装置的作用是_______ 。
(4)D中所盛试剂应是_______ (填写试剂序号),作用是_______ 。
(5)配平下列方程式
①_______
________Cu2S+_______HNO3=_______Cu(NO3)2+_______H2SO4+_______NO↑+_______H2O
②_______
_______MnO +_______H2O2+_______H+=_______Mn2++_______O2↑+_______H2O
+_______H2O2+_______H+=_______Mn2++_______O2↑+_______H2O
(6)油画所用的颜料含有某种白色铅化合物,置于空气中,天长日久就会生成黑色PbS,从而使油画色彩变暗,若用H2O2来擦拭,则可将PbS转化为白色的PbSO4而使油画恢复光彩。问:这一过程的化学方程式:_______ 。

(1)A中所盛放的试剂是
(2)B中的实验现象
(3)C中所盛试剂是
(4)D中所盛试剂应是
(5)配平下列方程式
①
________Cu2S+_______HNO3=_______Cu(NO3)2+_______H2SO4+_______NO↑+_______H2O
②
_______MnO
 +_______H2O2+_______H+=_______Mn2++_______O2↑+_______H2O
+_______H2O2+_______H+=_______Mn2++_______O2↑+_______H2O(6)油画所用的颜料含有某种白色铅化合物,置于空气中,天长日久就会生成黑色PbS,从而使油画色彩变暗,若用H2O2来擦拭,则可将PbS转化为白色的PbSO4而使油画恢复光彩。问:这一过程的化学方程式:
您最近一年使用:0次
名校
3 . 㵘同学根据Mg与 反应的原理推测Na也能在
反应的原理推测Na也能在 中燃烧,为了确定其产物,在春老师的指导下他设计了如图所示装置进行实验。已知
中燃烧,为了确定其产物,在春老师的指导下他设计了如图所示装置进行实验。已知 能被CO还原得到黑色的金属Pd。请回答下列问题:
能被CO还原得到黑色的金属Pd。请回答下列问题:
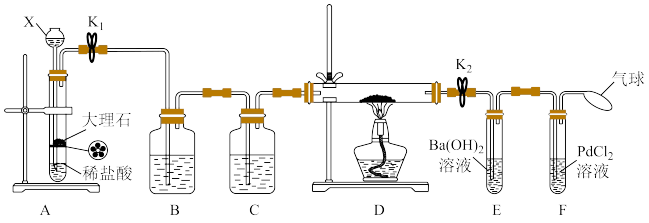
(1)仪器X的名称是___________ 。
(2)装置B中的试剂是___________ ,作用是___________ 。
(3)先称量硬质玻璃管的质量为 ,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是
,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是 。再按如下顺序进行实验操作。
。再按如下顺序进行实验操作。
①打开 和
和 ,通入
,通入 待E中出现
待E中出现___________ 时,再点燃酒,此操作的目的是___________ ;②熄灭酒精灯;③冷却到室温;④关闭 和
和 ;⑤称量硬质玻璃管。重复上述操作步骤,直至硬质玻璃管恒重,称得质量为
;⑤称量硬质玻璃管。重复上述操作步骤,直至硬质玻璃管恒重,称得质量为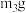 。
。
(4)加热D装置中硬质玻璃管一段时间,观察到以下现象:
①钠块表面变黑,熔融成金属小球;
②继续加热,钠燃烧产生黄色火焰,硬质玻璃管中有大量黑色和白色固体产生。
③F中试管内壁有黑色沉淀产生。
产生上述现象②中黑色固体的原因是___________ 。
(5)探究硬质玻璃管中固体产物中钠元素的存在形式:
假设一:白色固体是 ;假设二:白色固体是
;假设二:白色固体是 ;假设三:白色固体是
;假设三:白色固体是 和
和 的混合物。请完成下列实验设计,验证上述假设:
的混合物。请完成下列实验设计,验证上述假设:
步骤1:将硬质玻璃管中的固体产物溶于水后,过滤;
步骤2:往步骤1所得滤液中加入足量的___________ 溶液产生白色沉淀,过滤;
步骤3:往步骤2所得滤液中滴加几滴酚酞试液,滤液不变红色。
结论:假设一成立。
(6)根据上述实验现象及表格中的实验数据,写出Na与 反应的总化学方程式:
反应的总化学方程式:___________ 。
 反应的原理推测Na也能在
反应的原理推测Na也能在 中燃烧,为了确定其产物,在春老师的指导下他设计了如图所示装置进行实验。已知
中燃烧,为了确定其产物,在春老师的指导下他设计了如图所示装置进行实验。已知 能被CO还原得到黑色的金属Pd。请回答下列问题:
能被CO还原得到黑色的金属Pd。请回答下列问题:
(1)仪器X的名称是
(2)装置B中的试剂是
(3)先称量硬质玻璃管的质量为
 ,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是
,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是 。再按如下顺序进行实验操作。
。再按如下顺序进行实验操作。①打开
 和
和 ,通入
,通入 待E中出现
待E中出现 和
和 ;⑤称量硬质玻璃管。重复上述操作步骤,直至硬质玻璃管恒重,称得质量为
;⑤称量硬质玻璃管。重复上述操作步骤,直至硬质玻璃管恒重,称得质量为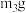 。
。(4)加热D装置中硬质玻璃管一段时间,观察到以下现象:
①钠块表面变黑,熔融成金属小球;
②继续加热,钠燃烧产生黄色火焰,硬质玻璃管中有大量黑色和白色固体产生。
③F中试管内壁有黑色沉淀产生。
产生上述现象②中黑色固体的原因是
(5)探究硬质玻璃管中固体产物中钠元素的存在形式:
假设一:白色固体是
 ;假设二:白色固体是
;假设二:白色固体是 ;假设三:白色固体是
;假设三:白色固体是 和
和 的混合物。请完成下列实验设计,验证上述假设:
的混合物。请完成下列实验设计,验证上述假设:步骤1:将硬质玻璃管中的固体产物溶于水后,过滤;
步骤2:往步骤1所得滤液中加入足量的
步骤3:往步骤2所得滤液中滴加几滴酚酞试液,滤液不变红色。
结论:假设一成立。
(6)根据上述实验现象及表格中的实验数据,写出Na与
 反应的总化学方程式:
反应的总化学方程式: |  |  |
| 66.70g | 69.00g | 72.15g |
您最近一年使用:0次
解题方法
4 . 下列含氮物质中,氮元素化合价最低的是
| A.NO | B.NH3 | C.NO2 | D.HNO3 |
您最近一年使用:0次
2021-04-23更新
|
256次组卷
|
4卷引用:福建省永安市第三中学高中校2021-2022学年高一上学期10月月考化学试题
5 . 利用氧化还原反应法配平:
Cu + HNO3(稀) — Cu( NO3 )2+ NO↑ + H2O
配平后方程式为______________ ,当1mol Cu完全反应时电子转移_______ mol, 被还原的HNO3为 ________ mol。
Cu + HNO3(稀) — Cu( NO3 )2+ NO↑ + H2O
配平后方程式为
您最近一年使用:0次
名校
6 . 媒体报道某工厂排放的废水中含有三氯合镉酸钠NaCdCl3,造成了水体重金属镉污染,三氯合镉酸钠中镉Cd的化合价是( )
| A.+2 | B.+1 | C.﹣4 | D.+4 |
您最近一年使用:0次
2020-11-12更新
|
126次组卷
|
2卷引用:福建省莆田第七中学2021-2022学年高一下学期期中考试化学试题
7 . 磷化铝(AlP)和磷化氢(PH3)都是粮食储备常用的高效熏蒸杀虫剂。
(1)磷元素在元素周期表中的位置:_____ 。AlP遇水蒸气会发生反应放出PH3气体,该反应的另一种产物的化学式为_____ 。
(2)工业制备PH3的流程如图所示。

①次磷酸属于_____ 元酸。
②次磷酸分解反应Ⅲ的化学方程式为:_____ 。
③若起始时有1molP4参加反应,则整个工业流程中共生成_____ molPH3。(不考虑产物的损失)
(1)磷元素在元素周期表中的位置:
(2)工业制备PH3的流程如图所示。

①次磷酸属于
②次磷酸分解反应Ⅲ的化学方程式为:
③若起始时有1molP4参加反应,则整个工业流程中共生成
您最近一年使用:0次



