1 . 高锰酸钾是一种典型的强氧化剂。完成下列填空:
I.在稀硫酸中, 和H2O2能发生氧化还原反应:
和H2O2能发生氧化还原反应:
氧化反应:H2O2-2e- == 2H++O2↑
还原反应: +5e-+8H+ == Mn2++4H2O
+5e-+8H+ == Mn2++4H2O
(1)反应中若有0.5 mol H2O2参加此反应,转移电子的个数为______ 。由上述反应得出的物质氧化性强弱的结论是____ >_____ (填写化学式)。
(2)已知:2KMnO4+7H2O2+3H2SO4 == K2SO4+2MnSO4+6O2↑+10H2O,则被1molKMnO4氧化的H2O2是______ mol。
II.将SO2气体通入酸性高锰酸钾溶液,溶液褪色, 被还原成Mn2+。
被还原成Mn2+。
(3)请写出上述过程的离子方程式______ 。
III.在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
① + CuS + H+→ Cu2+ + SO2↑ + Mn2+ + H2O(未配平)
+ CuS + H+→ Cu2+ + SO2↑ + Mn2+ + H2O(未配平)
② + Cu2S + H+ → Cu2++ SO2↑ + Mn2++ H2O(未配平)
+ Cu2S + H+ → Cu2++ SO2↑ + Mn2++ H2O(未配平)
(4)配平反应①:________ 。
(5)下列关于反应②的说法中错误的是__________ (选填编号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8:5
c.还原性的强弱关系是: Mn2+<Cu2S
d.若生成2.24 L(标况下) SO2,则反应中转移电子的物质的量是0.6mol
I.在稀硫酸中,
 和H2O2能发生氧化还原反应:
和H2O2能发生氧化还原反应:氧化反应:H2O2-2e- == 2H++O2↑
还原反应:
 +5e-+8H+ == Mn2++4H2O
+5e-+8H+ == Mn2++4H2O(1)反应中若有0.5 mol H2O2参加此反应,转移电子的个数为
(2)已知:2KMnO4+7H2O2+3H2SO4 == K2SO4+2MnSO4+6O2↑+10H2O,则被1molKMnO4氧化的H2O2是
II.将SO2气体通入酸性高锰酸钾溶液,溶液褪色,
 被还原成Mn2+。
被还原成Mn2+。(3)请写出上述过程的离子方程式
III.在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
①
 + CuS + H+→ Cu2+ + SO2↑ + Mn2+ + H2O(未配平)
+ CuS + H+→ Cu2+ + SO2↑ + Mn2+ + H2O(未配平)②
 + Cu2S + H+ → Cu2++ SO2↑ + Mn2++ H2O(未配平)
+ Cu2S + H+ → Cu2++ SO2↑ + Mn2++ H2O(未配平) (4)配平反应①:
(5)下列关于反应②的说法中错误的是
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8:5
c.还原性的强弱关系是: Mn2+<Cu2S
d.若生成2.24 L(标况下) SO2,则反应中转移电子的物质的量是0.6mol
您最近一年使用:0次
2020-10-25更新
|
842次组卷
|
5卷引用:福建省福州市第四中学2021届高三上学期9月月考化学试题
福建省福州市第四中学2021届高三上学期9月月考化学试题福建省三明市泰宁一中学2021届高三上学期第二阶段考试化学试题(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)专题05 氧化还原反应-2022年高考化学二轮复习重点专题常考点突破练
名校
解题方法
2 . 下列化学反应对应的离子方程式表示正确的是
A.KAl(SO4)2中滴加Ba(OH)2使 恰好完全沉淀:2Al3++3 恰好完全沉淀:2Al3++3 +3Ba2++6OH-=2Al(OH)3↓ +3BaSO4↓ +3Ba2++6OH-=2Al(OH)3↓ +3BaSO4↓ |
B.NH4HCO3溶于过量的NaOH溶液中: |
| C.向Ca(ClO)2溶液中通入少量SO2 : Ca2++ClO-+H2O+SO2=Cl-+CaSO4↓+2H+ |
D. 溶液与等物质的量的 溶液与等物质的量的 反应: 反应: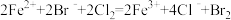 |
您最近一年使用:0次
2020-10-21更新
|
861次组卷
|
2卷引用:安徽省安庆市怀宁县怀宁中学2021届高三年级第一次质量检测化学试题
3 . 已知NH4CuSO3与足量的10 mol/L硫酸混合微热,产生下列现象:①有红色金属生成;②产生刺激性气味的气体;③溶液呈现蓝色。据此判断下列说法正确的是( )
| A.反应中硫酸作氧化剂 | B.NH4CuSO3中氮元素被氧化 |
| C.刺激性气味的气体是SO2 | D.1 mol NH4CuSO3完全反应转移1 mol电子 |
您最近一年使用:0次
2020-10-20更新
|
462次组卷
|
6卷引用:安徽省六安市第一中学2021届高三上学期第二次月考化学试题
安徽省六安市第一中学2021届高三上学期第二次月考化学试题湖北省六校(恩施高中 郧阳中学 沙市中学 十堰一中 随州二中 襄阳三中)2021届高三11月联考化学试题(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)山东省新泰市新泰中学2022届高三第一次阶段性考试化学试题山东省泰安市新泰第一中学东校2021-2022学年高三上学期期中考试化学试题
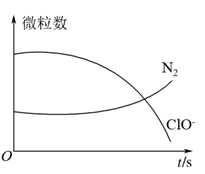
4 . 某离子反应涉及H2O、ClO-、 、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
 、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
| A.该反应中Cl-为氧化产物 |
| B.消耗1个还原剂微粒,转移6e- |
C. 被ClO-氧化成N2 被ClO-氧化成N2 |
| D.反应后溶液的酸性减弱 |
您最近一年使用:0次
2020-10-02更新
|
1134次组卷
|
8卷引用:山东省济南外国语学校2018届高三12月考试化学试题
5 . 在一个氧化还原反应体系中,反应物、生成物共有六种微粒:Fe3+、 、Fe2+、
、Fe2+、 、H+、H2O。已知氧化性
、H+、H2O。已知氧化性 (H+)>Fe3+。下列叙述不正确的是( )
(H+)>Fe3+。下列叙述不正确的是( )
 、Fe2+、
、Fe2+、 、H+、H2O。已知氧化性
、H+、H2O。已知氧化性 (H+)>Fe3+。下列叙述不正确的是( )
(H+)>Fe3+。下列叙述不正确的是( )| A.该反应说明Fe(NO3)2溶液不宜加酸酸化 |
| B.该反应中氧化剂与还原剂的个数之比为8:1 |
C.若有1个 发生还原反应,则转移8e- 发生还原反应,则转移8e- |
D.该反应中Fe2+是还原剂, 是还原产物 是还原产物 |
您最近一年使用:0次
2020-10-02更新
|
1145次组卷
|
3卷引用:人教版(2019)高一必修第一册 第一章 物质及其变化 第三节 氧化还原反应 方法帮
6 . 写出下列反应的离子方程式(已知还原性: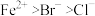 ):
):
(1)向 溶液中通入少量
溶液中通入少量 (
( 与
与 的微粒数的比值
的微粒数的比值 ):
):_________ ;
(2)向 溶液中通入足量
溶液中通入足量 :
:______ ;
(3)向 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为
的化学计量数之比为 :
:______ 。
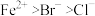 ):
):(1)向
 溶液中通入少量
溶液中通入少量 (
( 与
与 的微粒数的比值
的微粒数的比值 ):
):(2)向
 溶液中通入足量
溶液中通入足量 :
:(3)向
 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为
的化学计量数之比为 :
:
您最近一年使用:0次
2020-10-01更新
|
1461次组卷
|
3卷引用:人教版(2019)高一必修第一册 第一章 物质及其变化 章末总结
7 . 汽车剧烈碰撞时,安全气囊中发生反应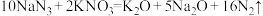 。若氧化产物比还原产物的物质的量多1.75 mol,则下列判断正确的是
。若氧化产物比还原产物的物质的量多1.75 mol,则下列判断正确的是
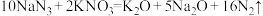 。若氧化产物比还原产物的物质的量多1.75 mol,则下列判断正确的是
。若氧化产物比还原产物的物质的量多1.75 mol,则下列判断正确的是| A.生成40.0 L(标准状况) N2 | B.有0.25 mol KNO3被氧化 |
| C.转移电子的物质的量为1.5 mol | D.被氧化的N的物质的量为3.75 mol |
您最近一年使用:0次
8 . A、B、C分别是元素甲、乙、丙的单质,它们都是常见的金属或非金属,D、E、F是常见的三种氧化物,且有如图所示转化关系,则下列说法不正确的是( )
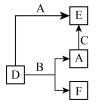

| A.E中一定都含有甲元素 |
| B.单质B肯定是氧化剂 |
| C.A、B、C中一定有一种是氧元素的单质 |
| D.若A是非金属,则B一定为金属 |
您最近一年使用:0次
2019高三·全国·专题练习
名校
解题方法
9 . 已知:还原性 ,氧化性
,氧化性 ,在含
,在含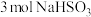 的溶液中逐滴加入
的溶液中逐滴加入 溶液,加入
溶液,加入 和析出上
和析出上 的物质的量的关系曲线如图所示。下列说法不正确的是( )
的物质的量的关系曲线如图所示。下列说法不正确的是( )
 ,氧化性
,氧化性 ,在含
,在含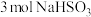 的溶液中逐滴加入
的溶液中逐滴加入 溶液,加入
溶液,加入 和析出上
和析出上 的物质的量的关系曲线如图所示。下列说法不正确的是( )
的物质的量的关系曲线如图所示。下列说法不正确的是( )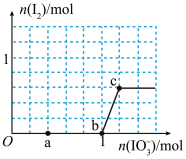
A.0~a间发生反应: |
B.a~b共消耗 的物质的量为 的物质的量为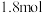 |
C.b~c间发生的反应中 仅是氧化产物 仅是氧化产物 |
D.当溶液中 与 与 的物质的量之比为 的物质的量之比为 时,加入的 时,加入的 为 为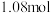 |
您最近一年使用:0次
2020-09-10更新
|
164次组卷
|
4卷引用:2019高考备考一轮复习精品资料 第二章 化学物质及其变化第3讲 氧化还原反应【押题专练】
(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化第3讲 氧化还原反应【押题专练】辽宁省实验中学东戴河分校2020届高三上学期期初摸底考试化学试题黑龙江省哈尔滨市三中2020届高三第二次月考化学试题2024届攀枝花市第十五中学校高三上学期第2次统一考试理科综合试卷-高中化学
名校
解题方法
10 . 已知氧化性: Br2> Fe3+,向含溶质a mol FeBr2的溶液中通入b mol Cl2,充分反应。下列说法不正确的是
| A.离子的还原性强弱:Fe2+>Br- >Cl- |
| B.当a=2b时,发生的离子反应:2Fe2++Cl2=2Fe3++2Cl- |
| C.当a=b时,反应后的离子浓度: c(Fe2+):c(Br-):c(Cl-)=1:2:2 |
| D.当3a=2b时,发生的离子反应:2Fe2++4Br-+3Cl2 =2Fe3++2Br2+ 6Cl- |
您最近一年使用:0次



