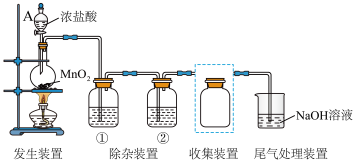
(1)仪器A的名称为
(2)发生装置中制取Cl2的化学方程式是
(3)除杂装置①中的试剂是
(4)将虚线框中的收集装置补充完整
(5)尾气处理装置中发生反应的离子方程式是
(6)将制得的Cl2溶于水得到氯水。在探究新制氯水成分及性质的实验中,请根据下列现将结论补充完整。
| 操作 | 现象 | 结论 | |
| a | 观察氯水颜色 | 氯水呈黄绿色 | 氯水中含有的微粒是 |
| b | 向氯水中滴入Na2CO3溶液 | 有无色气体产生 | 氯水中含有的微粒是 |
| c | 向红色纸条上滴加氯水 | 红色纸条褪色 | 氯水中含有的微粒是 |
(7)久置的氯水会失去漂白性,溶液由黄绿色变为无色。为探究氯水失效的原因,进行实验:用强光照射盛氯水的密闭广口瓶,并用传感器测定广口瓶中数据,得到如下曲线。
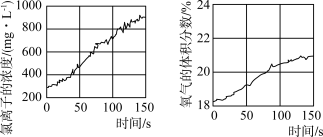
上两图中曲线变化的原因是
2 . 用如图所示装置制取氯气和“84”消毒液并进行相关探究。
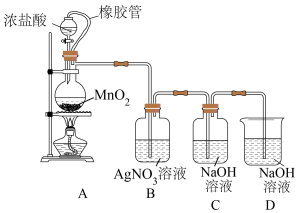
回答下列问题:
(1)装置
 中制取
中制取 的化学方程式为
的化学方程式为(2)装置
 中溶液出现浑浊,能否说明
中溶液出现浑浊,能否说明 与
与 溶液发生反应?
溶液发生反应?(3)为探究
 溶液的性质,某兴趣小组进行以下实验:
溶液的性质,某兴趣小组进行以下实验:ⅰ.取装置 (另外检验到装置
(另外检验到装置 中已无
中已无 剩余,也无溶解的
剩余,也无溶解的 )中溶液于试管中,滴入几滴紫色石蕊试液,溶液变蓝。
)中溶液于试管中,滴入几滴紫色石蕊试液,溶液变蓝。
ⅱ.将步骤ⅰ中蓝色溶液滴入浓盐酸中,蓝色迅速褪去变为无色,同时产生少量黄绿色气体。
ⅲ.取装置 中溶液于试管中,滴入稀
中溶液于试管中,滴入稀 溶液,光照,产生无色气泡。
溶液,光照,产生无色气泡。
ⅳ.取装置 中溶液于试管中,滴入几滴淀粉
中溶液于试管中,滴入几滴淀粉 溶液,溶液变蓝(已知淀粉遇
溶液,溶液变蓝(已知淀粉遇 变蓝色)。
变蓝色)。
①步骤ⅱ中蓝色迅速褪去的原因是
②步骤ⅲ中光照产生无色气泡的原因是
③步骤ⅳ说明 具有
具有
| A | B | C | D |
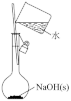 |  | 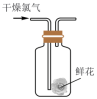 | 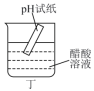 |
配制一定物质的量浓度的 溶液 溶液 | 比较NaHCO3和Na2CO3的热稳定性 | 检验干燥 是否具有漂白性 是否具有漂白性 | 测定醋酸溶液的 |
| A.A | B.B | C.C | D.D |
4 . 化学试剂根据其性质不同,需用不同方法保存。下列有关试剂保存的说法中错误的是
| A.漂白粉应避光保存在阴凉干燥的地方 | B.金属钠保存在煤油或石蜡油中 |
| C.新制氯水保存在棕色试剂瓶中 | D.配制的 溶液保存在容量瓶中 溶液保存在容量瓶中 |
5 . 下列实验操作与现象以及得出相关结论都正确的是
选项 | 操作与现象 | 结论 |
A | 取实验室存放的KI溶液少量于试管中,滴加淀粉溶液,变蓝 | KI已变质 |
B | 向某溶液中滴加 | 原溶液有 |
C | 向甲乙两支盛有硫代硫酸钠溶液的试管中分别滴加浓度均为3  溶液和 溶液和 溶液,甲未见浑浊,乙变浑浊 溶液,甲未见浑浊,乙变浑浊 | 增大 |
D | 向新制氯水中滴加紫色石蕊试液,溶液变红色 | HClO是弱酸 |
| A.A | B.B | C.C | D.D |
A. 通入品红溶液中,品红褪色 通入品红溶液中,品红褪色 |
| B.新制的氯水长期放置,溶液由黄绿色变为无色 |
C.将稀硫酸加入 溶液中,溶液由黄色变为橙色 溶液中,溶液由黄色变为橙色 |
D.将盛满 的密闭烧瓶浸入冰水中,气体红棕色变浅 的密闭烧瓶浸入冰水中,气体红棕色变浅 |
7 . 下列操作可行的是
| A.将未用完的小钠块直接扔入垃圾桶 | B.金属镁着火时用泡沫灭火器灭火 |
C.用 试纸测定氯水的 试纸测定氯水的 | D.在烧杯中做钠与水反应的实验 |
8 . 下列实验设计、现象和结论都正确的是
选项 | 实验 | 现象 | 结论 |
A | 将CO2通入BaCl2溶液中 | 有白色沉淀生成 | 白色沉淀是BaCO3 |
B | 向两支试管中各加入1 mL 1 mol/L的酸性KMnO4溶液,再向两支试管分别加入2 mL 1 mol/L的H2C2O4溶液和2mL0.5mol/L的H2C2O4溶液,记录高锰酸钾溶液褪色所需时间 | 1 mol/L的H2C2O4溶液中高锰酸钾溶液褪色快 | 浓度越大,反应速率越快 |
C | 向含AgCl和AgBr的饱和溶液中加入足量浓AgNO3溶液 | 产生两种颜色沉淀,但以白色为主 |
|
D | 向滴有酚酞的氨水中滴加氯水 | 溶液的红色褪去 | 氯水具有漂白性 |
| A.A | B.B | C.C | D.D |
| A.溶液的酸性和导电性均增强 |
| B.溶液的漂白性增强 |
| C.水、亚硫酸钠、氯水均为电解质 |
| D.向反应后的溶液中加入硝酸银溶液,产生白色沉淀,证明该溶液中存在氯离子 |

| A.氯水具有漂白性,能用作棉、麻和纸张的漂白剂 |
B.往氯水中滴加 溶液,会有白色沉淀生成 溶液,会有白色沉淀生成 |
| C.光照时,容器内氧气的体积分数会持续减小 |
| D.光照后的氯水的酸性强于新制氯水 |

 溶液,产生黑色沉淀
溶液,产生黑色沉淀 ,无
,无
 能加快反应
能加快反应


