名校
1 . 按下图装置进行实验,探究氯气的性质,下列说法正确的是
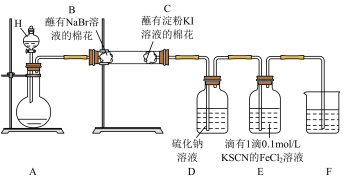

| A.仪器H的名称为分液漏斗,可用长颈漏斗替换 |
| B.C中棉花变蓝,说明氯气置换出碘,则非金属性:Cl>I, |
| C.E中溶液先变红后褪色,说明Cl2有漂白性 |
| D.F中溶液为NaOH溶液,进行尾气处理 |
您最近一年使用:0次
2023-08-08更新
|
307次组卷
|
2卷引用:四川省仁寿第一中学校南校区2023-2024学年高三上学期开学考试化学试题
名校
2 . 已知KMnO4在常温下与浓盐酸迅速反应生成Cl2,某兴趣小组设计下图装置用NaOH溶液吸收Cl2制得漂白液并探究NaClO的性质。
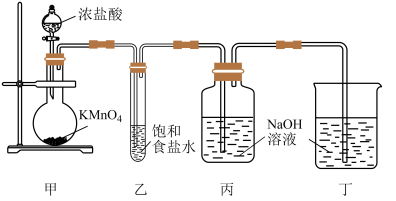
(1)甲装置中发生反应的离子方程式为_______ 。
(2)乙装置的作用为_______ 。
(3)丙装置中发生反应的离子方程式为_______ 。
(4)为探究NaClO溶液的性质,某兴趣小组进行以下实验:
i.取丙中溶液于试管中,滴入几滴紫色石蕊试液,溶液变蓝。
ii.将步骤i中蓝色溶液滴入浓盐酸中,蓝色迅速褪去,同时产生少量黄绿色气体。
iii.取丙中溶液于试管中,滴入稀H2SO4溶液,光照,产生无色气泡。
iv.取丙中溶液于试管中,滴入几滴淀粉KI溶液,溶液变蓝。
①步骤ii中蓝色迅速褪去的原因是_______ ;产生黄绿色气体的离子方程式为_______ 。
②步骤iii 中光照产生无色气泡的原因是_______ (用化学方程式表示)。
③步骤iv说明NaClO具有_______ 性。

(1)甲装置中发生反应的离子方程式为
(2)乙装置的作用为
(3)丙装置中发生反应的离子方程式为
(4)为探究NaClO溶液的性质,某兴趣小组进行以下实验:
i.取丙中溶液于试管中,滴入几滴紫色石蕊试液,溶液变蓝。
ii.将步骤i中蓝色溶液滴入浓盐酸中,蓝色迅速褪去,同时产生少量黄绿色气体。
iii.取丙中溶液于试管中,滴入稀H2SO4溶液,光照,产生无色气泡。
iv.取丙中溶液于试管中,滴入几滴淀粉KI溶液,溶液变蓝。
①步骤ii中蓝色迅速褪去的原因是
②步骤iii 中光照产生无色气泡的原因是
③步骤iv说明NaClO具有
您最近一年使用:0次
2023-02-09更新
|
130次组卷
|
5卷引用:四川省泸州市泸县第四中学2023-2024学年高一下学期开学化学试题
四川省泸州市泸县第四中学2023-2024学年高一下学期开学化学试题河南省安阳市重点高中2022-2023学年一下学期开学考试化学试题河南省安阳市第一中学2022-2023学年高一下学期开学考试化学试题河南郑州市2022-2023学年高一下学期开学考试化学试题(已下线)期中测试卷二【测试范围:第一、二章】-2023-2024学年高一化学上学期期中考点大串讲(人教版2019必修第一册)
名校
解题方法
3 . 某学习小组的同学用MnO2和浓盐酸反应来制备纯净的氯气并验证其有无漂白性,设计装置如图:

(1)A装置中反应的化学方程式:____________________________ ;D装置中现象:___________________ ;该套装置存在的缺陷:_________________________________ 。
(2)取少量E装置中溶液与洁厕灵(含盐酸)混合产生有毒气体,原因是_______________________ (用离子方程式表示)。
(3)若将Cl2通入热的烧碱溶液中,可以发生如下两个反应:
Cl2+2NaOH=NaCl+NaClO+H2O和3Cl2+6NaOH=5NaCl+NaClO3+3H2O。
从氧化还原角度分析Cl2表现了_______________ 。当混合液中Cl-和ClO 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为__________________ 。
(4)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,其反应物是___________ ,CuO的作用是_____________ ,写出总反应的化学方程式,并用单线桥法标出该反应的电子转移情况______________________________ 。


(1)A装置中反应的化学方程式:
(2)取少量E装置中溶液与洁厕灵(含盐酸)混合产生有毒气体,原因是
(3)若将Cl2通入热的烧碱溶液中,可以发生如下两个反应:
Cl2+2NaOH=NaCl+NaClO+H2O和3Cl2+6NaOH=5NaCl+NaClO3+3H2O。
从氧化还原角度分析Cl2表现了
 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为(4)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,其反应物是

您最近一年使用:0次
2022-12-14更新
|
395次组卷
|
3卷引用:四川省泸州市泸县2022-2023学年高一下学期开学考试化学试题
名校
解题方法
4 . 实验室用如图装置(夹持装置略)制备高效水处理剂高铁酸钾(K2FeO4)。
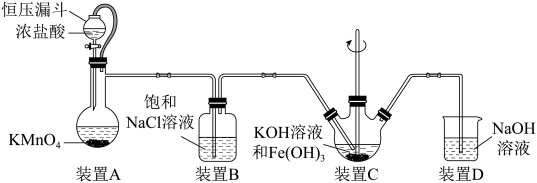
已知:K2FeO4具有强氧化性,可溶于水,微溶于浓KOH溶液,在0℃~5℃、强碱性溶液中比较稳定。
(1)装置A用于制取氯气,盛装KMnO4的仪器为______ ,A中发生反应的离子方程式为________ ,其中恒压漏斗的作用是_________ 。
(2)装置B中饱和NaCl溶液的作用为___________ 。
(3)装置C中生成K2FeO4反应的离子方程式为___________ ,为使C中K2FeO4稳定存在,可以采取的措施有___________ (任答一点)
(4)高铁酸钾作为水处理剂发挥的作用是___________ (答两点)

已知:K2FeO4具有强氧化性,可溶于水,微溶于浓KOH溶液,在0℃~5℃、强碱性溶液中比较稳定。
(1)装置A用于制取氯气,盛装KMnO4的仪器为
(2)装置B中饱和NaCl溶液的作用为
(3)装置C中生成K2FeO4反应的离子方程式为
(4)高铁酸钾作为水处理剂发挥的作用是
您最近一年使用:0次



