名校
1 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
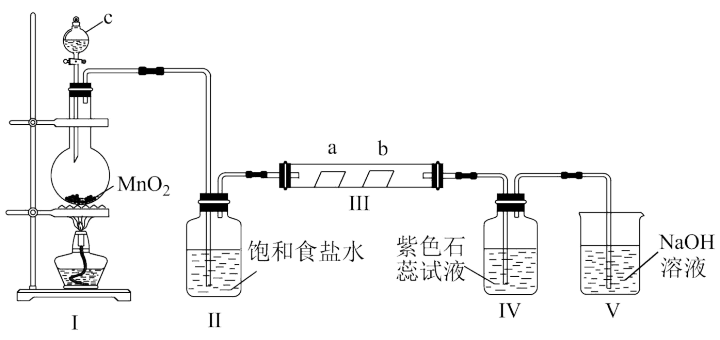
(1)装置Ⅰ中仪器c的名称是___________ ,实验室以二氧化锰和浓盐酸制备氯气的化学方程式为___________ 。
(2)装置Ⅱ的作用是___________ 。
(3)若产生的Cl2足量,实验过程中装置Ⅳ中的实验现象是___________ 。
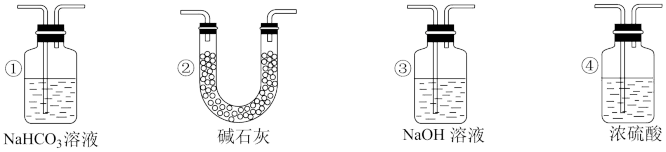
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___________ 装置(填序号)。
(5)除了Cl2能够对自来水杀菌消毒外,工业中还常用高铁酸钾(K2FeO4)作为高效、多功能的自来水处理剂,高铁酸钾与水反应时,能生成Fe(OH)3胶体吸附杂质净水,同时还产生一种气体,写出该原理的离子方程式___________ ,每生成1mol该气体,K2FeO4转移的电子数目为___________ NA。

(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)若产生的Cl2足量,实验过程中装置Ⅳ中的实验现象是
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

(5)除了Cl2能够对自来水杀菌消毒外,工业中还常用高铁酸钾(K2FeO4)作为高效、多功能的自来水处理剂,高铁酸钾与水反应时,能生成Fe(OH)3胶体吸附杂质净水,同时还产生一种气体,写出该原理的离子方程式
您最近一年使用:0次
2021-12-18更新
|
293次组卷
|
2卷引用:贵州省黔南州都匀市都匀第一中学2021-2022学年高一上学期期中化学试题
2 . 进行实验探究是研究物质性质、掌握变化原理的重要手段。某化学兴趣小组进行如下一系列化学实验探究,请根据实验信息回答相关问题。
I.探究Fe(OH)3胶体的制备
①写出探究实验I中制备Fe(OH)3胶体的化学方程式_______ ;
②实验(1)中滴入前3滴未观察到光路,可能的原因是_______ ,实验(2)中滴入第1滴时观察到很淡的光路可能的原因是_______ 。
③该兴趣小组同学通过以上探究对Fe(OH)3胶体的形成有以下认识,其中正确的有_______ 。
A.胶体区别于浊液的本质特征是分散质粒子直径大小
B.胶体是最不稳定的分散系
C.一定条件下胶体与浊液可以相互转化
D.Fe(OH)3胶体粒子是若干个Fe(OH)3聚集而成的
II.探究过氧化钠的性质。请根据实验现象分析实验结论。
④综合以上探究结果,请写出过氧化钠与水反应的化学方程式_______ 。
III.某学习小组设计以下四个实验探究氯水的成分,请回答相关问题。
(1)根据实验①得出的结论是_______ 。
(2)实验②中“实验方法”的具体操作过程是_______ 。
(3)写出实验③和实验④中的“实验现象”:③_______ ;④_______ 。
(4)通过实验③的“实验现象”,同学们得出两个不同的结论。这两个结论可能是:a._______ ;b._______ 。请设计一个简单的实验证明哪一个是正确的?_______
I.探究Fe(OH)3胶体的制备
| 实验编号 | 装置 | 试剂 | 实验操作 | 现象 |
| (1) |  | a:沸水 b:饱和FeCl3溶液 | 在a中逐滴滴入b试剂,同时用一束光照射溶液,观察现象。 | 前3滴未观察到光路,从第4滴开始观察到淡淡的光路,第8滴观察到明显光路;停止滴入,持续加热30min出现红褐色沉淀。 |
| (2) | a:NaOH稀溶液 b:饱和FeCl3溶液 | 滴入1滴出现红褐色沉淀,观察到很淡的光路,第2滴生成更多沉淀,光路消失。 |
②实验(1)中滴入前3滴未观察到光路,可能的原因是
③该兴趣小组同学通过以上探究对Fe(OH)3胶体的形成有以下认识,其中正确的有
A.胶体区别于浊液的本质特征是分散质粒子直径大小
B.胶体是最不稳定的分散系
C.一定条件下胶体与浊液可以相互转化
D.Fe(OH)3胶体粒子是若干个Fe(OH)3聚集而成的
II.探究过氧化钠的性质。请根据实验现象分析实验结论。
| 编号 | 操作 | 实验现象 | 实验结论 |
| (1) |  | 试管外壁发热 | ① |
| 产生大量能使带火星木条复燃的气体 | ② | ||
| (2) |  | 溶液变红 | ③ |
| 变红的溶液很快褪色 | 过氧化钠具有漂白性 |
III.某学习小组设计以下四个实验探究氯水的成分,请回答相关问题。
| 编号 | 实验方法 | 实验现象 | 结论 |
| ① | 将足量的氯水滴加到AgNO3溶液中 | 生成白色沉淀 | |
| ② | 淀粉-KI试纸变蓝色 | 氯水中含有C12 | |
| ③ | 将足量的氯水滴加到含有酚酞的NaOH溶液中 | ||
| ④ | 将足量的氯水滴加到Na2CO3溶液中 | 氯水中含有H+ |
(2)实验②中“实验方法”的具体操作过程是
(3)写出实验③和实验④中的“实验现象”:③
(4)通过实验③的“实验现象”,同学们得出两个不同的结论。这两个结论可能是:a.
您最近一年使用:0次
解题方法
3 . 下列实验设计能达到实验目的的是
| 选项 | 实验目的 | 实验设计 |
| A | 制备NO | 将铜丝插入浓硝酸中 |
| B | 鉴别NaBr和KI溶液 | 分别加新制氯水后再用CCl4萃取 |
| C | 证明碳的非金属性比硅的强 | 将盐酸与石灰石反应产生的气体直接通入硅酸钠溶液中 |
| D | 检验某盐中是否含 | 向盛某盐溶液的试管中滴入氢氧化钠溶液后,观察试管口处湿润的蓝色石蕊试纸是否变红 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-22更新
|
1040次组卷
|
2卷引用:贵州省贵阳市2022届高三一模理综化学试卷
解题方法
4 . 氯气是现代工业和生活中常用的杀菌消毒剂。回答下列问题:
(1)实验室常用 固体和浓盐酸在加热条件下制取
固体和浓盐酸在加热条件下制取 ,反应的离子方程式为
,反应的离子方程式为___________ 。实验室还可用 固体和浓盐酸在室温条件下制取少量氯气(同时生成
固体和浓盐酸在室温条件下制取少量氯气(同时生成 和
和 ),可选用图中的
),可选用图中的___________ (选填“A”或“B”)作为发生装置,反应的离子方程式为___________ 。图所示装置中玻璃弯管的作用是___________ 。
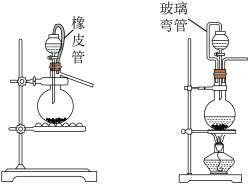
(2)某实验小组同学将上面制得的氯气通入蒸馏水中获得了氯气的水溶液——氯水,并利用如下装置探究氯水的成分及性质:
(说明:试管中溶液均为 ,均滴入氯水5滴;淀粉遇
,均滴入氯水5滴;淀粉遇 变蓝)
变蓝)
①实验I中反应方程式为___________ ,由此推断氧化性:
___________  (填“
(填“ ”或“
”或“ ”)。
”)。
②实验Ⅱ中溶液变红是由于溶液中含有___________ (填微粒符号,下同);使溶液褪色的微粒是___________ 。
(1)实验室常用
 固体和浓盐酸在加热条件下制取
固体和浓盐酸在加热条件下制取 ,反应的离子方程式为
,反应的离子方程式为 固体和浓盐酸在室温条件下制取少量氯气(同时生成
固体和浓盐酸在室温条件下制取少量氯气(同时生成 和
和 ),可选用图中的
),可选用图中的
(2)某实验小组同学将上面制得的氯气通入蒸馏水中获得了氯气的水溶液——氯水,并利用如下装置探究氯水的成分及性质:
| 实验Ⅰ | 实验Ⅱ | |
| 实验操作 | 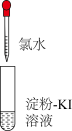 |  |
| 实验现象 | 溶液变蓝 | 石蕊溶液先变红,后褪色 |
 ,均滴入氯水5滴;淀粉遇
,均滴入氯水5滴;淀粉遇 变蓝)
变蓝)①实验I中反应方程式为

 (填“
(填“ ”或“
”或“ ”)。
”)。②实验Ⅱ中溶液变红是由于溶液中含有
您最近一年使用:0次



