1 . 进行实验探究是研究物质性质、掌握变化原理的重要手段。某化学兴趣小组进行如下一系列化学实验探究,请根据实验信息回答相关问题。
I.探究Fe(OH)3胶体的制备
①写出探究实验I中制备Fe(OH)3胶体的化学方程式_______ ;
②实验(1)中滴入前3滴未观察到光路,可能的原因是_______ ,实验(2)中滴入第1滴时观察到很淡的光路可能的原因是_______ 。
③该兴趣小组同学通过以上探究对Fe(OH)3胶体的形成有以下认识,其中正确的有_______ 。
A.胶体区别于浊液的本质特征是分散质粒子直径大小
B.胶体是最不稳定的分散系
C.一定条件下胶体与浊液可以相互转化
D.Fe(OH)3胶体粒子是若干个Fe(OH)3聚集而成的
II.探究过氧化钠的性质。请根据实验现象分析实验结论。
④综合以上探究结果,请写出过氧化钠与水反应的化学方程式_______ 。
III.某学习小组设计以下四个实验探究氯水的成分,请回答相关问题。
(1)根据实验①得出的结论是_______ 。
(2)实验②中“实验方法”的具体操作过程是_______ 。
(3)写出实验③和实验④中的“实验现象”:③_______ ;④_______ 。
(4)通过实验③的“实验现象”,同学们得出两个不同的结论。这两个结论可能是:a._______ ;b._______ 。请设计一个简单的实验证明哪一个是正确的?_______
I.探究Fe(OH)3胶体的制备
| 实验编号 | 装置 | 试剂 | 实验操作 | 现象 |
| (1) |  | a:沸水 b:饱和FeCl3溶液 | 在a中逐滴滴入b试剂,同时用一束光照射溶液,观察现象。 | 前3滴未观察到光路,从第4滴开始观察到淡淡的光路,第8滴观察到明显光路;停止滴入,持续加热30min出现红褐色沉淀。 |
| (2) | a:NaOH稀溶液 b:饱和FeCl3溶液 | 滴入1滴出现红褐色沉淀,观察到很淡的光路,第2滴生成更多沉淀,光路消失。 |
②实验(1)中滴入前3滴未观察到光路,可能的原因是
③该兴趣小组同学通过以上探究对Fe(OH)3胶体的形成有以下认识,其中正确的有
A.胶体区别于浊液的本质特征是分散质粒子直径大小
B.胶体是最不稳定的分散系
C.一定条件下胶体与浊液可以相互转化
D.Fe(OH)3胶体粒子是若干个Fe(OH)3聚集而成的
II.探究过氧化钠的性质。请根据实验现象分析实验结论。
| 编号 | 操作 | 实验现象 | 实验结论 |
| (1) |  | 试管外壁发热 | ① |
| 产生大量能使带火星木条复燃的气体 | ② | ||
| (2) |  | 溶液变红 | ③ |
| 变红的溶液很快褪色 | 过氧化钠具有漂白性 |
III.某学习小组设计以下四个实验探究氯水的成分,请回答相关问题。
| 编号 | 实验方法 | 实验现象 | 结论 |
| ① | 将足量的氯水滴加到AgNO3溶液中 | 生成白色沉淀 | |
| ② | 淀粉-KI试纸变蓝色 | 氯水中含有C12 | |
| ③ | 将足量的氯水滴加到含有酚酞的NaOH溶液中 | ||
| ④ | 将足量的氯水滴加到Na2CO3溶液中 | 氯水中含有H+ |
(2)实验②中“实验方法”的具体操作过程是
(3)写出实验③和实验④中的“实验现象”:③
(4)通过实验③的“实验现象”,同学们得出两个不同的结论。这两个结论可能是:a.
您最近一年使用:0次
名校
解题方法
2 . 含氯物质在生产、生活中有重要作用。舍勒在研究软锰矿(主要成分是MnO2,其摩尔质量为87 g/mol)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。
(1)写出浓盐酸与MnO2反应生成黄绿色气体的化学方程式为_________ ,用8.7 gMnO2与足量浓盐酸充分反应,生成Cl2的体积(标准状况下)为_________ L。
(2)实验室制取并收集干燥、纯净的该气体时,所需装置的接口连接顺序为:e接_________ (按气流方向,用小写字母表示)。所用仪器如下图所示:

(3)实验室中也可以用高锰酸钾与浓盐酸在常温下反应制取氯气。从下列仪器中选择制取氯气的装置是_________ (填字母),仪器P的名称为_________ 。
A. B.
B.  C.
C.
(4)在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
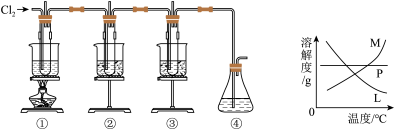
图中:①的试管里盛有15 mL 30%KOH溶液,置于热水浴中;
②的试管里盛有15 mL 8%NaOH溶液,置于冰水浴中;
③的试管里加有紫色石蕊试液;
④为尾气吸收装置。
写出②中制取次氯酸钠的离子方程式_________ 。为什么②装置要放在冰水浴中制取次氯酸钠_________ 。反应完毕经冷却后,①的试管中有大量晶体析出。图中符合该晶体溶解度曲线的是_________ (填写编号字母)。试管③紫色石蕊试液的颜色怎样变化?_________ 。
(1)写出浓盐酸与MnO2反应生成黄绿色气体的化学方程式为
(2)实验室制取并收集干燥、纯净的该气体时,所需装置的接口连接顺序为:e接

(3)实验室中也可以用高锰酸钾与浓盐酸在常温下反应制取氯气。从下列仪器中选择制取氯气的装置是
A.
 B.
B.  C.
C.
(4)在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。

图中:①的试管里盛有15 mL 30%KOH溶液,置于热水浴中;
②的试管里盛有15 mL 8%NaOH溶液,置于冰水浴中;
③的试管里加有紫色石蕊试液;
④为尾气吸收装置。
写出②中制取次氯酸钠的离子方程式
您最近一年使用:0次
名校
3 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
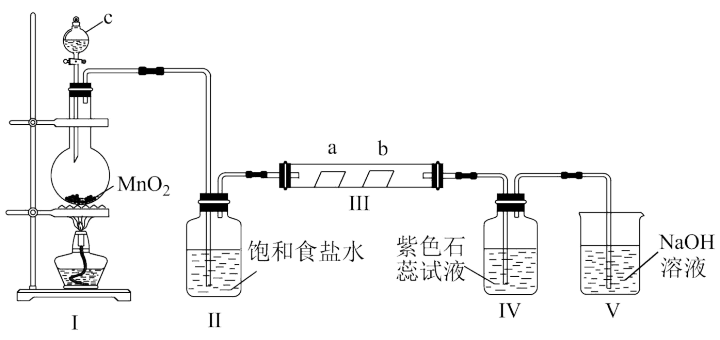
(1)装置Ⅰ中仪器c的名称是___________ ,实验室以二氧化锰和浓盐酸制备氯气的化学方程式为___________ 。
(2)装置Ⅱ的作用是___________ 。
(3)若产生的Cl2足量,实验过程中装置Ⅳ中的实验现象是___________ 。
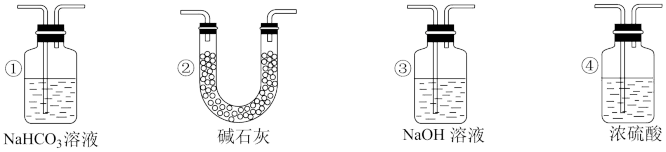
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___________ 装置(填序号)。
(5)除了Cl2能够对自来水杀菌消毒外,工业中还常用高铁酸钾(K2FeO4)作为高效、多功能的自来水处理剂,高铁酸钾与水反应时,能生成Fe(OH)3胶体吸附杂质净水,同时还产生一种气体,写出该原理的离子方程式___________ ,每生成1mol该气体,K2FeO4转移的电子数目为___________ NA。

(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)若产生的Cl2足量,实验过程中装置Ⅳ中的实验现象是
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

(5)除了Cl2能够对自来水杀菌消毒外,工业中还常用高铁酸钾(K2FeO4)作为高效、多功能的自来水处理剂,高铁酸钾与水反应时,能生成Fe(OH)3胶体吸附杂质净水,同时还产生一种气体,写出该原理的离子方程式
您最近一年使用:0次
2021-12-18更新
|
293次组卷
|
2卷引用:贵州省黔南州都匀市都匀第一中学2021-2022学年高一上学期期中化学试题



