解题方法
1 . 细菌可以促使铁、氮两种元素来进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如下图所示。___________ (填字母序号)。
A. 转化为氨态氮 B.硝化过程 C.反硝化过程
转化为氨态氮 B.硝化过程 C.反硝化过程
(2)氮气是生产氮肥的主要原料,工业合成氮的化学方程为___________ 。
(3)饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,配平下列方程式,并用单线桥标出电子转移的数目和方向。
,配平下列方程式,并用单线桥标出电子转移的数目和方向。___________ 。
___________ ___________
___________ ___________
___________ ___________
___________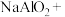 ___________
___________ ___________
___________
(4)硝酸工业生产中的尾气(主要成分为 和
和 )可用纯碱溶液吸收,相关的化学反应如下:
)可用纯碱溶液吸收,相关的化学反应如下:
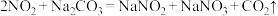
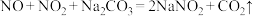
现有上述纯碱吸收液,吸收硝酸工业尾气,每产生 (标准状况)
(标准状况) 时,吸收液质量增加了
时,吸收液质量增加了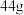 。计算吸收液中
。计算吸收液中 和
和 的物质的量之比
的物质的量之比___________ 。

A.
 转化为氨态氮 B.硝化过程 C.反硝化过程
转化为氨态氮 B.硝化过程 C.反硝化过程(2)氮气是生产氮肥的主要原料,工业合成氮的化学方程为
(3)饮用水中的
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,配平下列方程式,并用单线桥标出电子转移的数目和方向。
,配平下列方程式,并用单线桥标出电子转移的数目和方向。___________
 ___________
___________ ___________
___________ ___________
___________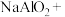 ___________
___________ ___________
___________
(4)硝酸工业生产中的尾气(主要成分为
 和
和 )可用纯碱溶液吸收,相关的化学反应如下:
)可用纯碱溶液吸收,相关的化学反应如下: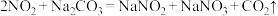
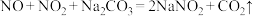
现有上述纯碱吸收液,吸收硝酸工业尾气,每产生
 (标准状况)
(标准状况) 时,吸收液质量增加了
时,吸收液质量增加了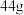 。计算吸收液中
。计算吸收液中 和
和 的物质的量之比
的物质的量之比
您最近一年使用:0次
解题方法
2 . 将空气中游离态的氮转化成含氧化合物叫做氮的固定,包括自然固氮和人工圈氮。以N2、H2为原料,在高温、高压和铁催化条件下合成氨的人工固氮技术是20世纪人类最伟大的成就之一、1921年,我国化工先驱侯德榜创造了将制碱与制氨结合的“联合制碱法”,为纯碱和氨肥工业技术的发展作出了杰出贡献。下列关于氮的转化过程,属于人工固氮的是
| A.用N2和H2合成氨 | B.闪电时空气中N2转化为NO |
| C.用NH3和CO2合成尿素 | D.豆科植物的根瘤售固氮 |
您最近一年使用:0次
名校
3 . 氮、磷元素的单质和它们的化合物用途广泛,与生产、生活有密切关系。请回答下列问题。
(1)下列属于氮的固定的是________ 。
a. 工业上N2和H2合成NH3 b. NH3催化氧化生成NO
c. N2和O2放电条件下生成NO d. NH3与灼热的氧化铜反应生成N2
(2)N2H4(联氨)可用作喷气式发动机推进剂、火箭燃料,可由次氯酸钠与氨反应制取,其化学反应方程式为_____________ 。
(3)三氟化氮( )是一种无色、无味的气体,是微电子工业技术的关键原料之一,
)是一种无色、无味的气体,是微电子工业技术的关键原料之一, 在潮湿的空气中与水蒸气能发生氧化还原反应,该反应的产物有:HF、NO和
在潮湿的空气中与水蒸气能发生氧化还原反应,该反应的产物有:HF、NO和 。
。
①写出该反应的化学方程式:___________ ,反应中生成0.2 mol  ,转移的电子数目为
,转移的电子数目为___________ ( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
② 无色、无臭,可一旦在空气中泄漏,却易于发现,判断该气体泄漏的现象是
无色、无臭,可一旦在空气中泄漏,却易于发现,判断该气体泄漏的现象是___________ 。
(4)Si3N4是一种性能优异的无机非金属材料,它的熔点高硬度大,电绝缘性好,化学性质稳定,但生产成本较高。根据以上描述推测Si3N4可能有哪些用途______ 。
a. 制作坩埚 b. 用作建筑陶瓷 c. 制作耐高温轴承 d. 制作切削刀具
(5)磷元素可以形成多种含氧酸。
①已知4.0g NaOH最多可中和100 mL 1mol·L−1 H3PO2溶液,则NaH2PO2是_________________ (填“正盐”或“酸式盐”)。
②已知常温下酸性:H3PO3 > CH3COOH > H2PO3-,则H3PO3与足量CH3COONa溶液混合的离子反应方程式为_____________ 。
(1)下列属于氮的固定的是
a. 工业上N2和H2合成NH3 b. NH3催化氧化生成NO
c. N2和O2放电条件下生成NO d. NH3与灼热的氧化铜反应生成N2
(2)N2H4(联氨)可用作喷气式发动机推进剂、火箭燃料,可由次氯酸钠与氨反应制取,其化学反应方程式为
(3)三氟化氮(
 )是一种无色、无味的气体,是微电子工业技术的关键原料之一,
)是一种无色、无味的气体,是微电子工业技术的关键原料之一, 在潮湿的空气中与水蒸气能发生氧化还原反应,该反应的产物有:HF、NO和
在潮湿的空气中与水蒸气能发生氧化还原反应,该反应的产物有:HF、NO和 。
。①写出该反应的化学方程式:
 ,转移的电子数目为
,转移的电子数目为 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。②
 无色、无臭,可一旦在空气中泄漏,却易于发现,判断该气体泄漏的现象是
无色、无臭,可一旦在空气中泄漏,却易于发现,判断该气体泄漏的现象是(4)Si3N4是一种性能优异的无机非金属材料,它的熔点高硬度大,电绝缘性好,化学性质稳定,但生产成本较高。根据以上描述推测Si3N4可能有哪些用途
a. 制作坩埚 b. 用作建筑陶瓷 c. 制作耐高温轴承 d. 制作切削刀具
(5)磷元素可以形成多种含氧酸。
①已知4.0g NaOH最多可中和100 mL 1mol·L−1 H3PO2溶液,则NaH2PO2是
②已知常温下酸性:H3PO3 > CH3COOH > H2PO3-,则H3PO3与足量CH3COONa溶液混合的离子反应方程式为
您最近一年使用:0次
名校
4 . 氮肥的使用极大提高了粮食作物的产量,对解决世界粮食危机起到了不可或缺的作用,下面是几种通过氮的固定制备氮肥的方法。
(1)自然固氮:一种途径是通过雷电将空气中少量的氮气转化为含氮化合物(氮肥),主要转化途径如下(转化所需试剂及条件已略去):
 硝酸盐[如
硝酸盐[如 ]
]
①写出在空气中 转化为NO的化学方程式
转化为NO的化学方程式_______ 。
②将 转化为
转化为 ,列举两种不同类别的化合物M
,列举两种不同类别的化合物M_______ (写化学式)。
③若M是Cu单质,与稀硝酸反应也能生成硝酸盐,写出铜粉与稀硝酸反应的离子方程式_______ 。
(2)人工固氮:
①工业上以氮气和氢气为原料,在高温、高压和催化剂的条件下合成氨。该反应的化学方程式为_______ 。
②利用氨气与氧气在催化剂作用下生成NO,是工业制备硝酸的重要环节,该反应中NO是_______ (填“氧化产物”“还原产物”或“氧化产物和还原产物”)。
③利用氨气与二氧化碳在催化剂作用下合成重要氮肥尿素 ,尿素中N元素的化合价是
,尿素中N元素的化合价是_______ 。合成尿素的化学方程式_______ 。尿素在土壤中与水结合生成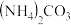 ,被植物吸收,有利于作物的生长。
,被植物吸收,有利于作物的生长。
(3)在微生物作用下实现 的转化,称为硝化过程。在一定条件下,
的转化,称为硝化过程。在一定条件下, 被
被 氧化成
氧化成 ,参加反应的
,参加反应的 和
和 的物质的量之比为
的物质的量之比为_______ 。由于 有毒,因此过量使用氮肥也会引起农作物大量减产,所以一定要合理科学使用。
有毒,因此过量使用氮肥也会引起农作物大量减产,所以一定要合理科学使用。
(4)有同学猜测,在 被细菌分解过程中,
被细菌分解过程中, 最终分解为
最终分解为 ,同时有
,同时有 生成。从化合价变化的角度分析有
生成。从化合价变化的角度分析有 生成的合理性
生成的合理性_______ 。
(1)自然固氮:一种途径是通过雷电将空气中少量的氮气转化为含氮化合物(氮肥),主要转化途径如下(转化所需试剂及条件已略去):
 硝酸盐[如
硝酸盐[如 ]
]①写出在空气中
 转化为NO的化学方程式
转化为NO的化学方程式②将
 转化为
转化为 ,列举两种不同类别的化合物M
,列举两种不同类别的化合物M③若M是Cu单质,与稀硝酸反应也能生成硝酸盐,写出铜粉与稀硝酸反应的离子方程式
(2)人工固氮:
①工业上以氮气和氢气为原料,在高温、高压和催化剂的条件下合成氨。该反应的化学方程式为
②利用氨气与氧气在催化剂作用下生成NO,是工业制备硝酸的重要环节,该反应中NO是
③利用氨气与二氧化碳在催化剂作用下合成重要氮肥尿素
 ,尿素中N元素的化合价是
,尿素中N元素的化合价是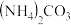 ,被植物吸收,有利于作物的生长。
,被植物吸收,有利于作物的生长。(3)在微生物作用下实现
 的转化,称为硝化过程。在一定条件下,
的转化,称为硝化过程。在一定条件下, 被
被 氧化成
氧化成 ,参加反应的
,参加反应的 和
和 的物质的量之比为
的物质的量之比为 有毒,因此过量使用氮肥也会引起农作物大量减产,所以一定要合理科学使用。
有毒,因此过量使用氮肥也会引起农作物大量减产,所以一定要合理科学使用。(4)有同学猜测,在
 被细菌分解过程中,
被细菌分解过程中, 最终分解为
最终分解为 ,同时有
,同时有 生成。从化合价变化的角度分析有
生成。从化合价变化的角度分析有 生成的合理性
生成的合理性
您最近一年使用:0次
名校
5 . 下列对化学基本概念的叙述或说法中正确的是
| A.CO2和NO2均能和水反应生成酸,所以都是酸性氧化物 |
| B.NH3和SO2的水溶液都能导电,所以都是电解质 |
| C.12C和14C互为同位素,两者之间的转化属于物理变化 |
| D.可用氨气为原料合成尿素[化学式为CO(NH2)2],从而实现氮的固定 |
您最近一年使用:0次
2022-04-24更新
|
161次组卷
|
2卷引用:辽宁省凌源市实验中学2021-2022学年高一下学期 4月月考化学试题



