氮、磷元素的单质和它们的化合物用途广泛,与生产、生活有密切关系。请回答下列问题。
(1)下列属于氮的固定的是________ 。
a. 工业上N2和H2合成NH3 b. NH3催化氧化生成NO
c. N2和O2放电条件下生成NO d. NH3与灼热的氧化铜反应生成N2
(2)N2H4(联氨)可用作喷气式发动机推进剂、火箭燃料,可由次氯酸钠与氨反应制取,其化学反应方程式为_____________ 。
(3)三氟化氮( )是一种无色、无味的气体,是微电子工业技术的关键原料之一,
)是一种无色、无味的气体,是微电子工业技术的关键原料之一, 在潮湿的空气中与水蒸气能发生氧化还原反应,该反应的产物有:HF、NO和
在潮湿的空气中与水蒸气能发生氧化还原反应,该反应的产物有:HF、NO和 。
。
①写出该反应的化学方程式:___________ ,反应中生成0.2 mol  ,转移的电子数目为
,转移的电子数目为___________ ( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
② 无色、无臭,可一旦在空气中泄漏,却易于发现,判断该气体泄漏的现象是
无色、无臭,可一旦在空气中泄漏,却易于发现,判断该气体泄漏的现象是___________ 。
(4)Si3N4是一种性能优异的无机非金属材料,它的熔点高硬度大,电绝缘性好,化学性质稳定,但生产成本较高。根据以上描述推测Si3N4可能有哪些用途______ 。
a. 制作坩埚 b. 用作建筑陶瓷 c. 制作耐高温轴承 d. 制作切削刀具
(5)磷元素可以形成多种含氧酸。
①已知4.0g NaOH最多可中和100 mL 1mol·L−1 H3PO2溶液,则NaH2PO2是_________________ (填“正盐”或“酸式盐”)。
②已知常温下酸性:H3PO3 > CH3COOH > H2PO3-,则H3PO3与足量CH3COONa溶液混合的离子反应方程式为_____________ 。
(1)下列属于氮的固定的是
a. 工业上N2和H2合成NH3 b. NH3催化氧化生成NO
c. N2和O2放电条件下生成NO d. NH3与灼热的氧化铜反应生成N2
(2)N2H4(联氨)可用作喷气式发动机推进剂、火箭燃料,可由次氯酸钠与氨反应制取,其化学反应方程式为
(3)三氟化氮(
 )是一种无色、无味的气体,是微电子工业技术的关键原料之一,
)是一种无色、无味的气体,是微电子工业技术的关键原料之一, 在潮湿的空气中与水蒸气能发生氧化还原反应,该反应的产物有:HF、NO和
在潮湿的空气中与水蒸气能发生氧化还原反应,该反应的产物有:HF、NO和 。
。①写出该反应的化学方程式:
 ,转移的电子数目为
,转移的电子数目为 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。②
 无色、无臭,可一旦在空气中泄漏,却易于发现,判断该气体泄漏的现象是
无色、无臭,可一旦在空气中泄漏,却易于发现,判断该气体泄漏的现象是(4)Si3N4是一种性能优异的无机非金属材料,它的熔点高硬度大,电绝缘性好,化学性质稳定,但生产成本较高。根据以上描述推测Si3N4可能有哪些用途
a. 制作坩埚 b. 用作建筑陶瓷 c. 制作耐高温轴承 d. 制作切削刀具
(5)磷元素可以形成多种含氧酸。
①已知4.0g NaOH最多可中和100 mL 1mol·L−1 H3PO2溶液,则NaH2PO2是
②已知常温下酸性:H3PO3 > CH3COOH > H2PO3-,则H3PO3与足量CH3COONa溶液混合的离子反应方程式为
更新时间:2024-01-10 10:23:24
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】①在酸性条件下,向含铬废水中加入FeSO4,可将 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为__________________________
②在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,离子方程式为___________________________ 。
③在碘和淀粉形成的蓝色溶液中,滴加亚硫酸钠碱性溶液,发现蓝色逐渐消失,离子方程式是_______________ 。
④对比②和③实验所得的结果,将I2、ClO-、 按氧化性由强到弱的顺序排列为
按氧化性由强到弱的顺序排列为___________ 。
 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为②在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,离子方程式为
③在碘和淀粉形成的蓝色溶液中,滴加亚硫酸钠碱性溶液,发现蓝色逐渐消失,离子方程式是
④对比②和③实验所得的结果,将I2、ClO-、
 按氧化性由强到弱的顺序排列为
按氧化性由强到弱的顺序排列为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是________ 。
a.单质的熔点降低
b.原子半径和简单离子半径均减小
c.元素的金属性减弱,非金属性增强
(2)氧化性最弱的简单阳离子是________ (填离子符号);热稳定性:
_____  (填>、<、=)。
(填>、<、=)。
(3)写出 的电子式:
的电子式:______________ 。
(4)已知化合物 由第三周期的两种相邻元素按原子个数比1:1组成,不稳定,遇水反应生成淡黄色沉淀
由第三周期的两种相邻元素按原子个数比1:1组成,不稳定,遇水反应生成淡黄色沉淀 和两种无色有刺激性气味气体
和两种无色有刺激性气味气体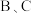 ,相应物质的转化关系如图:
,相应物质的转化关系如图:

①已知 的摩尔质量为
的摩尔质量为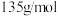 ,写出
,写出 的化学式
的化学式_______ 。
②任选一种合适的氧化剂 ,写出
,写出 的浓溶液与
的浓溶液与 反应生成
反应生成 的离子反应方程式
的离子反应方程式________ 。
③ 中的一种元素可形成化合物
中的一种元素可形成化合物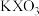 ,可用于实验室制
,可用于实验室制 。若不加催化剂,400℃时
。若不加催化剂,400℃时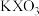 分解只生成两只盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1。写出该反应的化学方程式:
分解只生成两只盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1。写出该反应的化学方程式:_________ 。
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是
a.单质的熔点降低
b.原子半径和简单离子半径均减小
c.元素的金属性减弱,非金属性增强
(2)氧化性最弱的简单阳离子是

 (填>、<、=)。
(填>、<、=)。(3)写出
 的电子式:
的电子式:(4)已知化合物
 由第三周期的两种相邻元素按原子个数比1:1组成,不稳定,遇水反应生成淡黄色沉淀
由第三周期的两种相邻元素按原子个数比1:1组成,不稳定,遇水反应生成淡黄色沉淀 和两种无色有刺激性气味气体
和两种无色有刺激性气味气体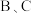 ,相应物质的转化关系如图:
,相应物质的转化关系如图:
①已知
 的摩尔质量为
的摩尔质量为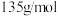 ,写出
,写出 的化学式
的化学式②任选一种合适的氧化剂
 ,写出
,写出 的浓溶液与
的浓溶液与 反应生成
反应生成 的离子反应方程式
的离子反应方程式③
 中的一种元素可形成化合物
中的一种元素可形成化合物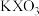 ,可用于实验室制
,可用于实验室制 。若不加催化剂,400℃时
。若不加催化剂,400℃时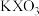 分解只生成两只盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1。写出该反应的化学方程式:
分解只生成两只盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1。写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】二氧化硒(Se)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。完成下列填空:
(1)Se和浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1:1。写出Se和浓HNO3的反应方程式_______________________________________ 。
(2)已知:Se+2H2SO4(浓) 2SO2↑+SeO2+2H2O
2SO2↑+SeO2+2H2O
2SO2+SeO2+2H2O Se+2SO42-+4H+
Se+2SO42-+4H+
SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是_________________________ 。
(3)回收得到的SeO2的含量,可以通过下面的方法测定:
①SeO2+KI+HNO3 Se+I2+KNO3+H2O(未配平) ②I2+2Na2S2O3
Se+I2+KNO3+H2O(未配平) ②I2+2Na2S2O3 Na2S4O6+2NaI
Na2S4O6+2NaI
实验中,准确称量SeO2样品0.1500g,消耗0.2000 mol·L-1的Na2S2O3溶液25.00 mL,所测定的样品中SeO2的质量分数为__________ 。
(1)Se和浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1:1。写出Se和浓HNO3的反应方程式
(2)已知:Se+2H2SO4(浓)
 2SO2↑+SeO2+2H2O
2SO2↑+SeO2+2H2O2SO2+SeO2+2H2O
 Se+2SO42-+4H+
Se+2SO42-+4H+SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是
(3)回收得到的SeO2的含量,可以通过下面的方法测定:
①SeO2+KI+HNO3
 Se+I2+KNO3+H2O(未配平) ②I2+2Na2S2O3
Se+I2+KNO3+H2O(未配平) ②I2+2Na2S2O3 Na2S4O6+2NaI
Na2S4O6+2NaI实验中,准确称量SeO2样品0.1500g,消耗0.2000 mol·L-1的Na2S2O3溶液25.00 mL,所测定的样品中SeO2的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如图所示。
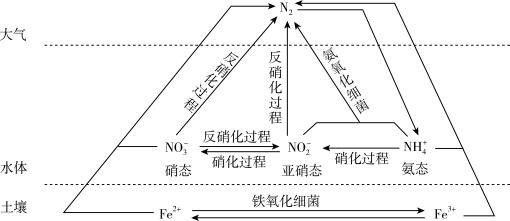
(1)图中所示氮循环中,不属于氮的固定的有___________ (填字母序号)。
a. N2 转化为氨态氮 b. 硝化过程c.反硝化过程 d.N2转化为硝态氮
(2)氮肥是水体中氨态氮的主要来源之一。
①氨气是生产氮肥的主要原料,实验室制取氨气的化学方程式为___________ 。
②检验氨态氮肥中NH 的实验方案是
的实验方案是___________ 。
(3)反硝化过程中,含氮物质发生___________ (填“氧化”或“还原”)反应。
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生 0.03 mol 氮气时,转移的电子的物质的量为___________ mol。
(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素转化为气体从水体中除去),用离子方程式分别说明利用土壤中(酸性)的铁循环脱除水体中硝态氮和氨态氮的原理:___________ 、___________ 。
(6)NOx是汽车尾气中的主要污染物之一,NOx能形成酸雨,用柴油的汽车加装尿素箱可使尾气达标,其原理为 CO(NH2)2+X=CO2+2NH3则X的化学式为___________ 。氨气和NOx可以转化为无害气体,写出NO2和 NH3催化加热条件下的化学反应方程式___________

(1)图中所示氮循环中,不属于氮的固定的有
a. N2 转化为氨态氮 b. 硝化过程c.反硝化过程 d.N2转化为硝态氮
(2)氮肥是水体中氨态氮的主要来源之一。
①氨气是生产氮肥的主要原料,实验室制取氨气的化学方程式为
②检验氨态氮肥中NH
 的实验方案是
的实验方案是(3)反硝化过程中,含氮物质发生
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生 0.03 mol 氮气时,转移的电子的物质的量为
(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素转化为气体从水体中除去),用离子方程式分别说明利用土壤中(酸性)的铁循环脱除水体中硝态氮和氨态氮的原理:
(6)NOx是汽车尾气中的主要污染物之一,NOx能形成酸雨,用柴油的汽车加装尿素箱可使尾气达标,其原理为 CO(NH2)2+X=CO2+2NH3则X的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用下图表示。
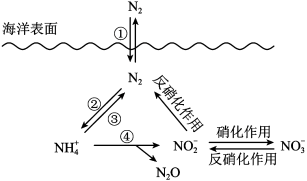
(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是___________ (填图中数字序号)。
(2)下列关于海洋氮循环的说法正确的是___________ (填字母序号)。
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含 的废水会影响海洋中
的废水会影响海洋中 的含量
的含量
(3)有氧时,在硝化细菌作用下, 可实现过程④的转化,将过程④的离子方程式补充完整:
可实现过程④的转化,将过程④的离子方程式补充完整:_____
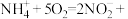 ___________
___________ ___________+___________。
___________+___________。
(4))有人研究了温度对海洋硝化细菌去除氨氮效果的影响,表为对10 L人工海水样本的监测数据:
硝化细菌去除氨氮的最佳反应温度是___________ ,在最佳反应温度时,48 h内去除氨氮反应的平均速率是___________ mg⋅L-1⋅h-1。
(5)为避免含氮废水对海洋氮循环系统的影响,需经处理后排放。下图是间接氧化工业废水中氨氮( )示意图。
)示意图。

①结合电极反应式简述间接氧化法去除氨氮的原理:___________ 。
②若生成 和
和 的物质的量之比为3∶1,则处理后废水的pH将
的物质的量之比为3∶1,则处理后废水的pH将___________ (填“增大”“不变”或“减小”)。

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是
(2)下列关于海洋氮循环的说法正确的是
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含
 的废水会影响海洋中
的废水会影响海洋中 的含量
的含量(3)有氧时,在硝化细菌作用下,
 可实现过程④的转化,将过程④的离子方程式补充完整:
可实现过程④的转化,将过程④的离子方程式补充完整: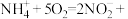 ___________
___________ ___________+___________。
___________+___________。(4))有人研究了温度对海洋硝化细菌去除氨氮效果的影响,表为对10 L人工海水样本的监测数据:
| 温度/℃ | 样本氨氮含量/mg | 处理24 h | 处理48 h |
| 氨氮含量/mg | 氨氮含量/mg | ||
| 20 | 1008 | 838 | 788 |
| 25 | 1008 | 757 | 468 |
| 30 | 1008 | 798 | 600 |
| 40 | 1008 | 977 | 910 |
(5)为避免含氮废水对海洋氮循环系统的影响,需经处理后排放。下图是间接氧化工业废水中氨氮(
 )示意图。
)示意图。
①结合电极反应式简述间接氧化法去除氨氮的原理:
②若生成
 和
和 的物质的量之比为3∶1,则处理后废水的pH将
的物质的量之比为3∶1,则处理后废水的pH将
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如下图所示。

(1)上图所示氮循环中,属于氮的固定的有___________ (填字母序号)。
a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一,氨气是生产氮肥的主要原料,工业合成氨的化学方程式为___________ 。
(3)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移的电子的物质的量为___________ mol。
(4)土壤中的铁循环可用于水体脱氮:脱氮是指将氮元素从水体中除去 ,
①用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理:___________ ,
②用离子方程式说明利用土壤中的铁循环脱除水体中硝态氮的原理:___________ 。
(5)NO是大气污染气体,测定某气体样品中NO含量操作如下:
将vL气样通入适量酸化的H2O2溶液中,使NO完全被氧化为 。向上述反应后溶液中加入v1mLc1mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为
。向上述反应后溶液中加入v1mLc1mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为 的离子方程式是
的离子方程式是_______ 。上述过程中发生下列反应:3Fe2++ +4H+=NO↑+3Fe3++2H2O;
+4H+=NO↑+3Fe3++2H2O; +6Fe2++14H+=2Cr3++6Fe3++7H2O,则气样中NO的含量为
+6Fe2++14H+=2Cr3++6Fe3++7H2O,则气样中NO的含量为_________ g/L。

(1)上图所示氮循环中,属于氮的固定的有
a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一,氨气是生产氮肥的主要原料,工业合成氨的化学方程式为
(3)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移的电子的物质的量为
(4)土壤中的铁循环可用于水体脱氮:
①用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理:
②用离子方程式说明利用土壤中的铁循环脱除水体中硝态氮的原理:
(5)NO是大气污染气体,测定某气体样品中NO含量操作如下:
将vL气样通入适量酸化的H2O2溶液中,使NO完全被氧化为
 。向上述反应后溶液中加入v1mLc1mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为
。向上述反应后溶液中加入v1mLc1mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为 的离子方程式是
的离子方程式是 +4H+=NO↑+3Fe3++2H2O;
+4H+=NO↑+3Fe3++2H2O; +6Fe2++14H+=2Cr3++6Fe3++7H2O,则气样中NO的含量为
+6Fe2++14H+=2Cr3++6Fe3++7H2O,则气样中NO的含量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.已知25℃时,醋酸、氢硫酸、氢氰酸的电离平衡常数如下表:(单位省略)
(1)体积相同、c(H+)相同的三种酸溶液a.CH3COOH;b.HCN;c.H2SO4分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的排列顺序是(填字母)_______ 。
(2)25℃时,等浓度的三种溶液①NaCN 溶液、②Na2S溶液、③CH3COONa溶液,pH由大到小的顺序为_______ (填序号)。
(3)25℃时,浓度均为0.01mol/L的①NaCN、②CH3COONa、③NaCl 溶液中,阴离子总浓度由大到小的顺序为_______ (填序号)。
(4)将浓度为0.02mol/L的HCN 与0.01mol/L NaOH 溶液等体积混合,测得混合溶液中c(Na+)>c(CN-),下列关系正确的是_______ 。
a.c(H+)<c(OH-) b.c(H+)+c(HCN)=c(OH-)+c(CN-) c.c(HCN)+c(CN-)=0.01mol/L
(5)25℃时,向NaCN溶液中通入少量H2S,反应的离子方程式为_______ 。
Ⅱ.NaCN是一种重要的基本化工原料,同时也是一种剧毒物质,严重危害人类健康。
含氰废水中的氰化物常以[Fe(CN)6]3-和CN-的形式存在,工业上有多种废水处理方法。其中电解处理法如图:用如图所示装置处理含CN-废水时,控制溶液pH为9~10并加入一定量的NaCl,一定条件下电解,阳极产生的ClO-将CN-氧化为无害物质而除去。铁电极为_______ (填“阴极”或“阳极”),阳极产生的ClO-的电极反应为_______ ,阳极产生的ClO-将CN-氧化为无害物质而除去的离子方程式为_______ 。
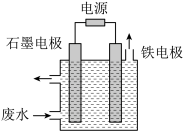
| 醋酸 | 氢硫酸 | 氢氰酸 |
| Ka=1.8×10-5 | Ka1=9.1×10-8 Ka2=1.1×10-12 | Ka=4.9×10-10 |
(2)25℃时,等浓度的三种溶液①NaCN 溶液、②Na2S溶液、③CH3COONa溶液,pH由大到小的顺序为
(3)25℃时,浓度均为0.01mol/L的①NaCN、②CH3COONa、③NaCl 溶液中,阴离子总浓度由大到小的顺序为
(4)将浓度为0.02mol/L的HCN 与0.01mol/L NaOH 溶液等体积混合,测得混合溶液中c(Na+)>c(CN-),下列关系正确的是
a.c(H+)<c(OH-) b.c(H+)+c(HCN)=c(OH-)+c(CN-) c.c(HCN)+c(CN-)=0.01mol/L
(5)25℃时,向NaCN溶液中通入少量H2S,反应的离子方程式为
Ⅱ.NaCN是一种重要的基本化工原料,同时也是一种剧毒物质,严重危害人类健康。
含氰废水中的氰化物常以[Fe(CN)6]3-和CN-的形式存在,工业上有多种废水处理方法。其中电解处理法如图:用如图所示装置处理含CN-废水时,控制溶液pH为9~10并加入一定量的NaCl,一定条件下电解,阳极产生的ClO-将CN-氧化为无害物质而除去。铁电极为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知:乙二酸(HOOC-COOH,可简写为H2C2O4),俗称草酸,已知:25℃ H2C2O4 K1 = 5.4×10-2,K2 = 5.4×10-5;
(1)已知:25℃ Ka(HF)=3.53×10-4,请写出少量草酸(H2C2O4)与NaF溶液反应的化学方程式:______ 。
(2)常温下,向某浓度的草酸溶液中逐滴加入一定物质的量浓度的KOH溶液,所得溶液中H2C2O4、HC2O 、C2O
、C2O 三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,回答下列问题:
三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,回答下列问题:
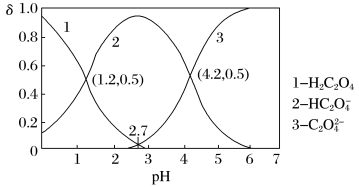
①如果所得溶液溶质为KHC2O4,则该溶液显_______ (填“酸性”、“碱性”或“中性”);
②如果所得溶液溶质为K2C2O4,则该溶液中各离子浓度由大到小顺序为_______ ;
③当所得溶液pH=2.7时,溶液中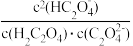 =
=_____________ ;
(3)已知25℃ 草酸钙的Ksp=4.0×10-8,碳酸钙的Ksp=2.5×10-9。回答下列问题:
25℃时向20 mL碳酸钙的饱和溶液中逐滴加入1.0×10-3mol/L的草酸钾溶液20 mL,通过计算说明能否产生草酸钙沉淀?_______________
(1)已知:25℃ Ka(HF)=3.53×10-4,请写出少量草酸(H2C2O4)与NaF溶液反应的化学方程式:
(2)常温下,向某浓度的草酸溶液中逐滴加入一定物质的量浓度的KOH溶液,所得溶液中H2C2O4、HC2O
 、C2O
、C2O 三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,回答下列问题:
三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,回答下列问题:
①如果所得溶液溶质为KHC2O4,则该溶液显
②如果所得溶液溶质为K2C2O4,则该溶液中各离子浓度由大到小顺序为
③当所得溶液pH=2.7时,溶液中
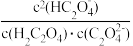 =
=(3)已知25℃ 草酸钙的Ksp=4.0×10-8,碳酸钙的Ksp=2.5×10-9。回答下列问题:
25℃时向20 mL碳酸钙的饱和溶液中逐滴加入1.0×10-3mol/L的草酸钾溶液20 mL,通过计算说明能否产生草酸钙沉淀?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】SO2是大气的主要污染物,工业上利用钠碱循环法可除去二氧化硫。回答下列问题:
(1)钠碱循环法中,吸收液为Na2SO3溶液,其水溶液在常温下pH__ 7(大于、小于、或者、等于)。
(2)可用Na2SO3溶液吸收SO2制备NaHSO3。该反应的离子方程式是___ 。
(3)已知H2SO3的电离常数为K1=1.54×10-2,K2=1.024×10-7;H2CO3的电离常数为K1=4.30×10-7,K2=5.60×10-11,则下列各组微粒可以大量共存的是__ (填字母)。
A.CO 和HSO
和HSO B.HCO
B.HCO 和HSO
和HSO C.SO
C.SO 和HCO
和HCO D.H2SO3和HCO
D.H2SO3和HCO
(4)吸收液吸收SO2的过程中,水溶液中H2SO3、HSO 、SO
、SO 随pH的分布如图:
随pH的分布如图:
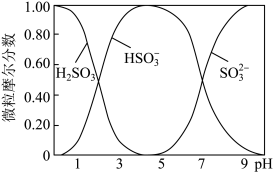
①在0.1mol/LNaHSO3溶液中离子浓度关系不正确的是____ (填字母)。
A.c(Na+)=2c(SO )+c(HSO
)+c(HSO )+c(H2SO3)
)+c(H2SO3)
B.c(H+)-c(OH-)=c(SO )-c(H2SO3)
)-c(H2SO3)
C.c(Na+)>c(HSO )>c(SO
)>c(SO )>c(OH-)
)>c(OH-)
D.c(Na+)+c(H+)=2c(SO )+c(HSO
)+c(HSO )+c(OH-)
)+c(OH-)
②室温下,向一定量的漂白液(主要成分NaClO)中滴加适量的NaHSO3溶液,该过程中溶液pH的变化是___ 。写出该反应的离子方程式___ 。
(5)泡沫灭火器内外桶中各盛有一定浓度的NaHCO3、Al2(SO4)3溶液。使用时须将该灭火器反转并拔掉插销,让上述溶液混合并由喷嘴喷射出一定量的气流和难溶物,覆盖在可燃物的表面起到灭火效果。
①写出该反应的离子方程式___ 。
②泡沫灭火器可适合于扑灭下列哪种物品的初期着火___ 。(填序号)
A.植物油 B.金属镁粉 C.家用电器 D.棉纱纸张
(1)钠碱循环法中,吸收液为Na2SO3溶液,其水溶液在常温下pH
(2)可用Na2SO3溶液吸收SO2制备NaHSO3。该反应的离子方程式是
(3)已知H2SO3的电离常数为K1=1.54×10-2,K2=1.024×10-7;H2CO3的电离常数为K1=4.30×10-7,K2=5.60×10-11,则下列各组微粒可以大量共存的是
A.CO
 和HSO
和HSO B.HCO
B.HCO 和HSO
和HSO C.SO
C.SO 和HCO
和HCO D.H2SO3和HCO
D.H2SO3和HCO
(4)吸收液吸收SO2的过程中,水溶液中H2SO3、HSO
 、SO
、SO 随pH的分布如图:
随pH的分布如图:
①在0.1mol/LNaHSO3溶液中离子浓度关系不正确的是
A.c(Na+)=2c(SO
 )+c(HSO
)+c(HSO )+c(H2SO3)
)+c(H2SO3)B.c(H+)-c(OH-)=c(SO
 )-c(H2SO3)
)-c(H2SO3)C.c(Na+)>c(HSO
 )>c(SO
)>c(SO )>c(OH-)
)>c(OH-)D.c(Na+)+c(H+)=2c(SO
 )+c(HSO
)+c(HSO )+c(OH-)
)+c(OH-)②室温下,向一定量的漂白液(主要成分NaClO)中滴加适量的NaHSO3溶液,该过程中溶液pH的变化是
(5)泡沫灭火器内外桶中各盛有一定浓度的NaHCO3、Al2(SO4)3溶液。使用时须将该灭火器反转并拔掉插销,让上述溶液混合并由喷嘴喷射出一定量的气流和难溶物,覆盖在可燃物的表面起到灭火效果。
①写出该反应的离子方程式
②泡沫灭火器可适合于扑灭下列哪种物品的初期着火
A.植物油 B.金属镁粉 C.家用电器 D.棉纱纸张
您最近一年使用:0次



