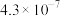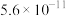Ⅰ.已知25℃时,醋酸、氢硫酸、氢氰酸的电离平衡常数如下表:(单位省略)
(1)体积相同、c(H+)相同的三种酸溶液a.CH3COOH;b.HCN;c.H2SO4分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的排列顺序是(填字母)_______ 。
(2)25℃时,等浓度的三种溶液①NaCN 溶液、②Na2S溶液、③CH3COONa溶液,pH由大到小的顺序为_______ (填序号)。
(3)25℃时,浓度均为0.01mol/L的①NaCN、②CH3COONa、③NaCl 溶液中,阴离子总浓度由大到小的顺序为_______ (填序号)。
(4)将浓度为0.02mol/L的HCN 与0.01mol/L NaOH 溶液等体积混合,测得混合溶液中c(Na+)>c(CN-),下列关系正确的是_______ 。
a.c(H+)<c(OH-) b.c(H+)+c(HCN)=c(OH-)+c(CN-) c.c(HCN)+c(CN-)=0.01mol/L
(5)25℃时,向NaCN溶液中通入少量H2S,反应的离子方程式为_______ 。
Ⅱ.NaCN是一种重要的基本化工原料,同时也是一种剧毒物质,严重危害人类健康。
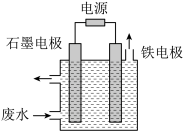
含氰废水中的氰化物常以[Fe(CN)6]3-和CN-的形式存在,工业上有多种废水处理方法。其中电解处理法如图:用如图所示装置处理含CN-废水时,控制溶液pH为9~10并加入一定量的NaCl,一定条件下电解,阳极产生的ClO-将CN-氧化为无害物质而除去。铁电极为_______ (填“阴极”或“阳极”),阳极产生的ClO-的电极反应为_______ ,阳极产生的ClO-将CN-氧化为无害物质而除去的离子方程式为_______ 。
| 醋酸 | 氢硫酸 | 氢氰酸 |
| Ka=1.8×10-5 | Ka1=9.1×10-8 Ka2=1.1×10-12 | Ka=4.9×10-10 |
(2)25℃时,等浓度的三种溶液①NaCN 溶液、②Na2S溶液、③CH3COONa溶液,pH由大到小的顺序为
(3)25℃时,浓度均为0.01mol/L的①NaCN、②CH3COONa、③NaCl 溶液中,阴离子总浓度由大到小的顺序为
(4)将浓度为0.02mol/L的HCN 与0.01mol/L NaOH 溶液等体积混合,测得混合溶液中c(Na+)>c(CN-),下列关系正确的是
a.c(H+)<c(OH-) b.c(H+)+c(HCN)=c(OH-)+c(CN-) c.c(HCN)+c(CN-)=0.01mol/L
(5)25℃时,向NaCN溶液中通入少量H2S,反应的离子方程式为
Ⅱ.NaCN是一种重要的基本化工原料,同时也是一种剧毒物质,严重危害人类健康。
含氰废水中的氰化物常以[Fe(CN)6]3-和CN-的形式存在,工业上有多种废水处理方法。其中电解处理法如图:用如图所示装置处理含CN-废水时,控制溶液pH为9~10并加入一定量的NaCl,一定条件下电解,阳极产生的ClO-将CN-氧化为无害物质而除去。铁电极为

更新时间:2021-02-04 16:54:43
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】25℃时,草酸( )的
)的 ,
,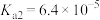 ;
; 的
的 ,
, 。回答下列问题:
。回答下列问题:
(1)写出 的第二步电离方程式
的第二步电离方程式___________ 。
(2)相同浓度的 、
、 、
、 、
、 四种溶液中碱性最弱的物质是
四种溶液中碱性最弱的物质是________ 溶液。用 的NaOH溶液滴定
的NaOH溶液滴定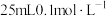 草酸溶液的滴定曲线如图所示。
草酸溶液的滴定曲线如图所示。
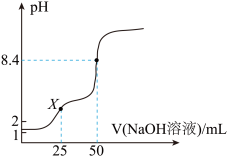
①X点溶液显___________ (填“酸性”“中性”或“碱性”),若向该溶液中滴加少量 ,反应的离子方程式为
,反应的离子方程式为___________ , 值
值___________ (填“增大”或“减小”)。
②滴定过程中所得混合溶液中 时,
时,
___________ 。
(3)反应 的平衡常数K的数量级为
的平衡常数K的数量级为___________ 。
 )的
)的 ,
,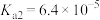 ;
; 的
的 ,
, 。回答下列问题:
。回答下列问题:(1)写出
 的第二步电离方程式
的第二步电离方程式(2)相同浓度的
 、
、 、
、 、
、 四种溶液中碱性最弱的物质是
四种溶液中碱性最弱的物质是 的NaOH溶液滴定
的NaOH溶液滴定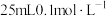 草酸溶液的滴定曲线如图所示。
草酸溶液的滴定曲线如图所示。
①X点溶液显
 ,反应的离子方程式为
,反应的离子方程式为 值
值②滴定过程中所得混合溶液中
 时,
时,
(3)反应
 的平衡常数K的数量级为
的平衡常数K的数量级为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在一元强碱MOH溶液中加入一元酸HA溶液,充分反应后,溶液呈中性。甲同学认为溶液中c(A-)==c(M+),而乙同学认为c(A-)与 c(M+)是否相等,要看一元酸HA是强酸还是弱酸。你认为_____ 同学的说法正确,理由是_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知:
(1)在相同浓度的H2CO3和HF的溶液中,用“>”“<”或“=”填空。c(H+):H2CO3_______ HF;c(F-)_______ c(CO )。
)。
(2)HCO 、CO
、CO 、F-、CN-结合质子能力:
、F-、CN-结合质子能力:_______ 。
(3)H2CO3、HCO 、HF、HCN酸性由强到弱的顺序为:
、HF、HCN酸性由强到弱的顺序为:_______ 。
(4)将足量的二氧化碳通入到NaCN溶液中的离子方程式为_______ 。
| H2CO3 | HF | HCN | |
| K或Ka1 | 4.3×10-7 | 7.2×10-4 | 4.9×10-10 |
| Ka2 | 5.6×10-11 |
(1)在相同浓度的H2CO3和HF的溶液中,用“>”“<”或“=”填空。c(H+):H2CO3
 )。
)。(2)HCO
 、CO
、CO 、F-、CN-结合质子能力:
、F-、CN-结合质子能力:(3)H2CO3、HCO
 、HF、HCN酸性由强到弱的顺序为:
、HF、HCN酸性由强到弱的顺序为:(4)将足量的二氧化碳通入到NaCN溶液中的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】水是生命的源泉,水溶液中的离子平衡与我们的生产生活密切相关。
(1)25℃时,向水的电离平衡体系中加入少量醋酸钠固体,得到pH为11的溶液,由水电离出的c(OH-)=_____ mol•L-1。
(2)25℃时,已知Ka(CH3COOH)=1.8×10-5,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=_____ mol•L-1(填精确值), =
=_____ 。
(3)某温度时水的离子积常数Kw=10-13,若将此温度下pH=11的 溶液aL与0.10mol•L-1的稀硫酸bL混合,所得混合液pH=2,则a:b=
溶液aL与0.10mol•L-1的稀硫酸bL混合,所得混合液pH=2,则a:b=______ 。
(4)25℃时,向20mL0.1mol•L-1的NH3·H2O溶液滴加amL0.1mol•L-1的H2SO4溶液时,混合溶液的pH恰好为7。则NH3·H2O的电离平衡常数Kb=_____ (用含有a的式子表示)。
(1)25℃时,向水的电离平衡体系中加入少量醋酸钠固体,得到pH为11的溶液,由水电离出的c(OH-)=
(2)25℃时,已知Ka(CH3COOH)=1.8×10-5,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=
 =
=(3)某温度时水的离子积常数Kw=10-13,若将此温度下pH=11的
 溶液aL与0.10mol•L-1的稀硫酸bL混合,所得混合液pH=2,则a:b=
溶液aL与0.10mol•L-1的稀硫酸bL混合,所得混合液pH=2,则a:b=(4)25℃时,向20mL0.1mol•L-1的NH3·H2O溶液滴加amL0.1mol•L-1的H2SO4溶液时,混合溶液的pH恰好为7。则NH3·H2O的电离平衡常数Kb=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】填写下来空白:
(1)在0.1 mol/L的NH4Cl溶液中,各离子浓度由大到小的顺序是______________ 。
(2)电解质溶液中存在着多种平衡,现有室温下0.1 mol/L的NaHCO3溶液,pH=8,回答问题:
①写出溶液中存在的多种平衡(用离子方程式表示)_____________ 。
②下面关系式正确的是________ 。
A.c(Na+)+c(H+)=c( )+c(
)+c( )+c(OH-)
)+c(OH-)
B.c(Na+)>c( )>c(OH-)>c(H2CO3)>c(H+)
)>c(OH-)>c(H2CO3)>c(H+)
C.c(OH-)=c(H+)+c(H2CO3)-c( )
)
D.c(Na+)=c( )+c(H2CO3)
)+c(H2CO3)
(1)在0.1 mol/L的NH4Cl溶液中,各离子浓度由大到小的顺序是
(2)电解质溶液中存在着多种平衡,现有室温下0.1 mol/L的NaHCO3溶液,pH=8,回答问题:
①写出溶液中存在的多种平衡(用离子方程式表示)
②下面关系式正确的是
A.c(Na+)+c(H+)=c(
 )+c(
)+c( )+c(OH-)
)+c(OH-)B.c(Na+)>c(
 )>c(OH-)>c(H2CO3)>c(H+)
)>c(OH-)>c(H2CO3)>c(H+)C.c(OH-)=c(H+)+c(H2CO3)-c(
 )
)D.c(Na+)=c(
 )+c(H2CO3)
)+c(H2CO3)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】利用所学化学反应原理,解决以下问题:
(1)一定温度下,将一定质量 的冰醋酸加水稀释过程中,溶液的导电能力变化如右图所示,请回答下列问题:

①写出冰醋酸电离方程式____________
②加水过程中,其水溶液导电能力变化的原因是:_______________________________________
③a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:__________ (填“相同”、“a点大”、“b点大”、“c点大”)
(2)常温下,将0.2 mol·L-1的CH3COOH和0.1 mol·L-1的NaOH溶液等体积混合,所得溶液的pH=5(溶液体积变化忽略不计),则该溶液中:
c(CH3COO−) + c(CH3COOH)=_______ mol/L
c(H+) - c(CH3COO−)+ c(Na+) =_______ mol/L
(3)KAl(SO4)2·12H2O可做净水剂,其原理是____________________________________ (用离子方程式表示)
(4)在0.10 mol·L-1 Na2SO3溶液中,离子浓度由大到小的顺序为___________________________________ 。
(1)一定温度下,将

①写出冰醋酸电离方程式
②加水过程中,其水溶液导电能力变化的原因是:
③a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:
(2)常温下,将0.2 mol·L-1的CH3COOH和0.1 mol·L-1的NaOH溶液等体积混合,所得溶液的pH=5(溶液体积变化忽略不计),则该溶液中:
c(CH3COO−) + c(CH3COOH)=
c(H+) - c(CH3COO−)+ c(Na+) =
(3)KAl(SO4)2·12H2O可做净水剂,其原理是
(4)在0.10 mol·L-1 Na2SO3溶液中,离子浓度由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题
(1)实验室在配制 的溶液时,为了抑制
的溶液时,为了抑制 的水解可加入少量的
的水解可加入少量的_______ (填写物质的名称).把 溶液蒸干、灼烧,最后得到的主要固体产物是
溶液蒸干、灼烧,最后得到的主要固体产物是________ (填化学式).
(2)已知 水溶液呈碱性,其原因是
水溶液呈碱性,其原因是_________ (用离子方程式和相应的文字解释).
(3)高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.
高铁电池的总反应为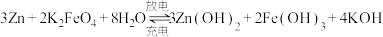 .充电时,阳极反应式为
.充电时,阳极反应式为______________ .
(1)实验室在配制
 的溶液时,为了抑制
的溶液时,为了抑制 的水解可加入少量的
的水解可加入少量的 溶液蒸干、灼烧,最后得到的主要固体产物是
溶液蒸干、灼烧,最后得到的主要固体产物是(2)已知
 水溶液呈碱性,其原因是
水溶液呈碱性,其原因是(3)高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.
高铁电池的总反应为
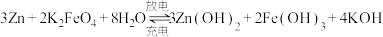 .充电时,阳极反应式为
.充电时,阳极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铁、铜及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2,其中S为-1价)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2 6SO2+Fe3O4,氧化产物为
6SO2+Fe3O4,氧化产物为______ ,若有3 mol FeS2参加反应,转移电子的物质的量为_____ 。
(2)①钢铁的电化学腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向______ 。

②写出修改前的钢铁吸氧腐蚀时石墨电极的电极反应式:___________ 。
(3)高铁酸钾(K2FeO4)可作净水剂,也可用于制造高铁电池。高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,该电池放电时正极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH,该电池放电时正极反应式为___________ 。用该电池电解100 mL 1 mol·L-1的AgNO3溶液,当电路中通过0.1 mol电子时,被电解溶液的pH为___________ (溶液体积变化忽略不计)。
(1)黄铁矿(FeS2,其中S为-1价)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2
 6SO2+Fe3O4,氧化产物为
6SO2+Fe3O4,氧化产物为(2)①钢铁的电化学腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向

②写出修改前的钢铁吸氧腐蚀时石墨电极的电极反应式:
(3)高铁酸钾(K2FeO4)可作净水剂,也可用于制造高铁电池。高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH,该电池放电时正极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH,该电池放电时正极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
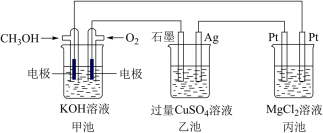
【推荐3】如图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,完成下列问题:___________ 。
(2)写出乙池石墨电极的名称为___________ (填“正极”“负极”或“阴极”“阳极”)。写出乙池中电解总反应的化学方程式:___________ 。
(3)甲池中消耗224 mL(标准状况下)O2,此时丙池中理论上最多产生___________ g沉淀,此时乙池中溶液的体积为400 mL,该溶液的pH=___________ 。
(4)若丙中电极不变,将其溶液换成NaOH溶液,开关闭合一段时间后,甲中溶液的pH将___________ (填“增大”“减小”或“不变”,下同),丙中溶液的pH将___________ 。
(5)某同学利用甲醇燃料电池设计电解法制取漂白液或Fe(OH)2的实验装置(如图)。若用于制漂白液,a为电池的___________ 极,电解质溶液最好用___________ 。若用于制Fe(OH)2,使用硫酸钠溶液作电解质溶液,阳极选用___________ 作电极。阳极反应的电极方程式为___________ 。
(2)写出乙池石墨电极的名称为
(3)甲池中消耗224 mL(标准状况下)O2,此时丙池中理论上最多产生
(4)若丙中电极不变,将其溶液换成NaOH溶液,开关闭合一段时间后,甲中溶液的pH将
(5)某同学利用甲醇燃料电池设计电解法制取漂白液或Fe(OH)2的实验装置(如图)。若用于制漂白液,a为电池的

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】常温下,叠氮酸( )是一元弱酸,高锰酸(
)是一元弱酸,高锰酸(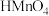 )是一元强酸,0.1
)是一元强酸,0.1 的高铼酸(
的高铼酸(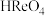 )、0.1
)、0.1 的高锰酸(
的高锰酸(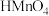 )溶液分别与0.1
)溶液分别与0.1 的NaOH溶液等体积混合,所得溶液均呈中性。请回答下列问题:
的NaOH溶液等体积混合,所得溶液均呈中性。请回答下列问题:
(1)高铼酸属于______ (填“强”或“弱”)酸,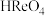 中Re的化合价为
中Re的化合价为______ 。
(2) 的电离方程式为
的电离方程式为______ ,常温下,已知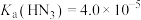 ,则0.1
,则0.1 的
的 溶液中
溶液中
______  。
。
(3)体积相同的高锰酸和醋酸溶液的pH均为2,若将两溶液稀释100倍,则pH变化较大的是_____________ ,向稀释后的溶液中分别加入0.1mol·L-1的NaOH溶液,则消耗NaOH体积较多的是_____________ 。
(4)已知25℃时,三种酸的电离常数如下:
写出下列在溶液中发生反应的离子方程式:
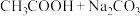 (少量):
(少量):______ ;
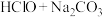 (少量):
(少量):______ 。
 )是一元弱酸,高锰酸(
)是一元弱酸,高锰酸(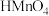 )是一元强酸,0.1
)是一元强酸,0.1 的高铼酸(
的高铼酸(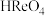 )、0.1
)、0.1 的高锰酸(
的高锰酸(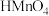 )溶液分别与0.1
)溶液分别与0.1 的NaOH溶液等体积混合,所得溶液均呈中性。请回答下列问题:
的NaOH溶液等体积混合,所得溶液均呈中性。请回答下列问题:(1)高铼酸属于
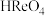 中Re的化合价为
中Re的化合价为(2)
 的电离方程式为
的电离方程式为 ,则0.1
,则0.1 的
的 溶液中
溶液中
 。
。(3)体积相同的高锰酸和醋酸溶液的pH均为2,若将两溶液稀释100倍,则pH变化较大的是
(4)已知25℃时,三种酸的电离常数如下:
化学式 |
|
| HClO |
|
|
|
|
| — |
| — |
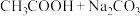 (少量):
(少量):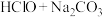 (少量):
(少量):
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】利用电化学方法可以将 有效地转化为
有效地转化为 (其中C元素的化合价为+2),装置如图1所示。
(其中C元素的化合价为+2),装置如图1所示。

(1)在该装置中,左侧Pt电极为___________ (填“阴极”或“阳极”)。
(2)装置工作时,阴极除有 生成外,还可能生成副产物降低电解效率。已知:电解效率=
生成外,还可能生成副产物降低电解效率。已知:电解效率=  。
。
①副产物可能是___________ (写出一种即可)。
②标准状况下,当阳极生成氧气的体积为224mL时,测得整个阴极区内的 ,电解效率为
,电解效率为___________ (忽略电解前后溶液的体积变化)。
(3)研究表明,溶液 会影响
会影响 转化为
转化为 的效率。如图2是常温下
的效率。如图2是常温下 (以
(以 计)在水溶液中各种存在形式的物质的量分数(
计)在水溶液中各种存在形式的物质的量分数( )随
)随 变化的情况。
变化的情况。
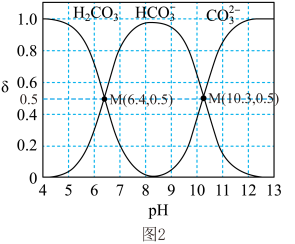
①常温下, 的
的 =
=___________ 。
② 时,
时, 几乎未转化为
几乎未转化为 ,此时
,此时 在溶液中的主要存在形式为
在溶液中的主要存在形式为___________ 。
③ 时,
时, 的转化效率较高,溶液中相应的电极反应式为
的转化效率较高,溶液中相应的电极反应式为___________ 。
 有效地转化为
有效地转化为 (其中C元素的化合价为+2),装置如图1所示。
(其中C元素的化合价为+2),装置如图1所示。
(1)在该装置中,左侧Pt电极为
(2)装置工作时,阴极除有
 生成外,还可能生成副产物降低电解效率。已知:电解效率=
生成外,还可能生成副产物降低电解效率。已知:电解效率=  。
。①副产物可能是
②标准状况下,当阳极生成氧气的体积为224mL时,测得整个阴极区内的
 ,电解效率为
,电解效率为(3)研究表明,溶液
 会影响
会影响 转化为
转化为 的效率。如图2是常温下
的效率。如图2是常温下 (以
(以 计)在水溶液中各种存在形式的物质的量分数(
计)在水溶液中各种存在形式的物质的量分数( )随
)随 变化的情况。
变化的情况。
①常温下,
 的
的 =
=②
 时,
时, 几乎未转化为
几乎未转化为 ,此时
,此时 在溶液中的主要存在形式为
在溶液中的主要存在形式为③
 时,
时, 的转化效率较高,溶液中相应的电极反应式为
的转化效率较高,溶液中相应的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】研究弱电解质的电离,有重要的实际意义。
Ⅰ.醋酸是一种常见的有机酸
(1)醋酸的电离方程式为___________ 。
(2)保持温度不变,向醋酸溶液中通入一定量的氨气,下列量将变小的是___________(填字母)。
(3)将 溶液中加水稀释,
溶液中加水稀释, 的比值将
的比值将___________ (填“变大”、“不变”或“变小”)。
(4)下列事实不能 说明 是弱电解质的是___________(填字母)。
是弱电解质的是___________(填字母)。
Ⅱ.对比酸性的相对强弱
(5)某些弱酸在 时的电离常数(
时的电离常数( )如下:
)如下:
下列反应可以发生的是___________(填字母)。
Ⅰ.醋酸是一种常见的有机酸
(1)醋酸的电离方程式为
(2)保持温度不变,向醋酸溶液中通入一定量的氨气,下列量将变小的是___________(填字母)。
A. | B. | C. | D. 电离平衡常数 电离平衡常数 |
 溶液中加水稀释,
溶液中加水稀释, 的比值将
的比值将(4)下列事实
 是弱电解质的是___________(填字母)。
是弱电解质的是___________(填字母)。A.相同温度下,浓度均为 的盐酸和醋酸的导电性对比:盐酸>醋酸 的盐酸和醋酸的导电性对比:盐酸>醋酸 |
B. 溶液能使紫色石蕊试液变蓝 溶液能使紫色石蕊试液变蓝 |
C. 时, 时, 溶液的 溶液的 约为2 约为2 |
D. 的 的 溶液恰好与 溶液恰好与 溶液完全反应 溶液完全反应 |
Ⅱ.对比酸性的相对强弱
(5)某些弱酸在
 时的电离常数(
时的电离常数( )如下:
)如下:| 化学式 |  |  |  |  |
电离常数( ) ) |  |  |  | 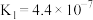  |
A. |
B. |
C. |
D.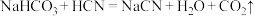 |
您最近一年使用:0次