SO2是大气的主要污染物,工业上利用钠碱循环法可除去二氧化硫。回答下列问题:
(1)钠碱循环法中,吸收液为Na2SO3溶液,其水溶液在常温下pH__ 7(大于、小于、或者、等于)。
(2)可用Na2SO3溶液吸收SO2制备NaHSO3。该反应的离子方程式是___ 。
(3)已知H2SO3的电离常数为K1=1.54×10-2,K2=1.024×10-7;H2CO3的电离常数为K1=4.30×10-7,K2=5.60×10-11,则下列各组微粒可以大量共存的是__ (填字母)。
A.CO 和HSO
和HSO B.HCO
B.HCO 和HSO
和HSO C.SO
C.SO 和HCO
和HCO D.H2SO3和HCO
D.H2SO3和HCO
(4)吸收液吸收SO2的过程中,水溶液中H2SO3、HSO 、SO
、SO 随pH的分布如图:
随pH的分布如图:
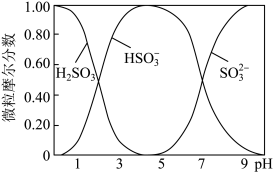
①在0.1mol/LNaHSO3溶液中离子浓度关系不正确的是____ (填字母)。
A.c(Na+)=2c(SO )+c(HSO
)+c(HSO )+c(H2SO3)
)+c(H2SO3)
B.c(H+)-c(OH-)=c(SO )-c(H2SO3)
)-c(H2SO3)
C.c(Na+)>c(HSO )>c(SO
)>c(SO )>c(OH-)
)>c(OH-)
D.c(Na+)+c(H+)=2c(SO )+c(HSO
)+c(HSO )+c(OH-)
)+c(OH-)
②室温下,向一定量的漂白液(主要成分NaClO)中滴加适量的NaHSO3溶液,该过程中溶液pH的变化是___ 。写出该反应的离子方程式___ 。
(5)泡沫灭火器内外桶中各盛有一定浓度的NaHCO3、Al2(SO4)3溶液。使用时须将该灭火器反转并拔掉插销,让上述溶液混合并由喷嘴喷射出一定量的气流和难溶物,覆盖在可燃物的表面起到灭火效果。
①写出该反应的离子方程式___ 。
②泡沫灭火器可适合于扑灭下列哪种物品的初期着火___ 。(填序号)
A.植物油 B.金属镁粉 C.家用电器 D.棉纱纸张
(1)钠碱循环法中,吸收液为Na2SO3溶液,其水溶液在常温下pH
(2)可用Na2SO3溶液吸收SO2制备NaHSO3。该反应的离子方程式是
(3)已知H2SO3的电离常数为K1=1.54×10-2,K2=1.024×10-7;H2CO3的电离常数为K1=4.30×10-7,K2=5.60×10-11,则下列各组微粒可以大量共存的是
A.CO
 和HSO
和HSO B.HCO
B.HCO 和HSO
和HSO C.SO
C.SO 和HCO
和HCO D.H2SO3和HCO
D.H2SO3和HCO
(4)吸收液吸收SO2的过程中,水溶液中H2SO3、HSO
 、SO
、SO 随pH的分布如图:
随pH的分布如图:
①在0.1mol/LNaHSO3溶液中离子浓度关系不正确的是
A.c(Na+)=2c(SO
 )+c(HSO
)+c(HSO )+c(H2SO3)
)+c(H2SO3)B.c(H+)-c(OH-)=c(SO
 )-c(H2SO3)
)-c(H2SO3)C.c(Na+)>c(HSO
 )>c(SO
)>c(SO )>c(OH-)
)>c(OH-)D.c(Na+)+c(H+)=2c(SO
 )+c(HSO
)+c(HSO )+c(OH-)
)+c(OH-)②室温下,向一定量的漂白液(主要成分NaClO)中滴加适量的NaHSO3溶液,该过程中溶液pH的变化是
(5)泡沫灭火器内外桶中各盛有一定浓度的NaHCO3、Al2(SO4)3溶液。使用时须将该灭火器反转并拔掉插销,让上述溶液混合并由喷嘴喷射出一定量的气流和难溶物,覆盖在可燃物的表面起到灭火效果。
①写出该反应的离子方程式
②泡沫灭火器可适合于扑灭下列哪种物品的初期着火
A.植物油 B.金属镁粉 C.家用电器 D.棉纱纸张
更新时间:2021-04-21 08:32:08
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】写出下列盐溶液水解的离子方程式
(1)次氯酸钾(KClO)溶液__________________________________________________ ;
(2)磷酸钠(Na3PO4)溶液___________________________________________________ ;
(3)明矾净水水解原理____________________________________________ ;
(4)硫酸铁溶液__________________________________________
(5)泡沫灭火器的原理__________________________________________
(1)次氯酸钾(KClO)溶液
(2)磷酸钠(Na3PO4)溶液
(3)明矾净水水解原理
(4)硫酸铁溶液
(5)泡沫灭火器的原理
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.NaClO和KAl(SO4)2都是重要的化工产品,均可应用于造纸业。
(1)NaClO溶液的pH>7,用离子方程式表示原因___ 。
(2)某小组同学把饱和的NaClO溶液和饱和的KAl(SO4)2溶液混合反应,发现产生大量的白色胶状沉淀,同时生成一种有漂白、杀菌作用的物质。反应的离子方程式是___ 。
(3)已知在常温下测得浓度均为0.1mol•L-1的下列5种溶液的pH:
则下列离子CH3COO-,HCO ,CO
,CO ,ClO-,CN-结合质子(H+)的能力最强的是
,ClO-,CN-结合质子(H+)的能力最强的是___ 。
Ⅱ.请回答下列问题(注意:溶液混合时,均忽略溶液体积变化):
(4)25℃时,pH=2的盐酸溶液与pH=4的H2SO4溶液等体积混合,求混合后的pH=__ 。
(5)25℃时,将pH=3的H2SO4溶液和pH=12的NaOH溶液混合,充分混合后所得溶液的pH=10,则H2SO4溶液与NaOH溶液的体积比为__ 。
(6)室温下pH=9的NaOH溶液和pH=9的CH3COONa溶液,设由水电离产生的OH-的物质的量浓度分别为A和B,则 等于
等于__ 。
Ⅲ.25℃时,现有浓度均为0.1mol.L-1的下列溶液:①盐酸,②醋酸,③硫酸。请回答下列问题:
(7)等浓度,等体积的①、②、③三种溶液,用等物质的量浓度的NaOH溶液恰好完全中和时,消耗NaOH溶液的体积由大到小顺序为__ 。
(8)等体积,等pH①、②、③三种溶液,分别加入形状大小相同的镁片,开始产生气泡的速率由快到慢的关系为__ 。
(1)NaClO溶液的pH>7,用离子方程式表示原因
(2)某小组同学把饱和的NaClO溶液和饱和的KAl(SO4)2溶液混合反应,发现产生大量的白色胶状沉淀,同时生成一种有漂白、杀菌作用的物质。反应的离子方程式是
(3)已知在常温下测得浓度均为0.1mol•L-1的下列5种溶液的pH:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
则下列离子CH3COO-,HCO
 ,CO
,CO ,ClO-,CN-结合质子(H+)的能力最强的是
,ClO-,CN-结合质子(H+)的能力最强的是Ⅱ.请回答下列问题(注意:溶液混合时,均忽略溶液体积变化):
(4)25℃时,pH=2的盐酸溶液与pH=4的H2SO4溶液等体积混合,求混合后的pH=
(5)25℃时,将pH=3的H2SO4溶液和pH=12的NaOH溶液混合,充分混合后所得溶液的pH=10,则H2SO4溶液与NaOH溶液的体积比为
(6)室温下pH=9的NaOH溶液和pH=9的CH3COONa溶液,设由水电离产生的OH-的物质的量浓度分别为A和B,则
 等于
等于Ⅲ.25℃时,现有浓度均为0.1mol.L-1的下列溶液:①盐酸,②醋酸,③硫酸。请回答下列问题:
(7)等浓度,等体积的①、②、③三种溶液,用等物质的量浓度的NaOH溶液恰好完全中和时,消耗NaOH溶液的体积由大到小顺序为
(8)等体积,等pH①、②、③三种溶液,分别加入形状大小相同的镁片,开始产生气泡的速率由快到慢的关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某二元酸(H2A)在水中的电离方程式:H2A=H++HA-;HA- H++A2-。回答下列问题:
H++A2-。回答下列问题:
(1)Na2A溶液显碱性理由是:__ (用离子方程式表示)。
(2)在0.1mol/L的Na2A溶液中,下列微粒浓度关系式正确的是__ 。
A.c(A2-)+c(HA-)+c(H2A)=0.1mol/L B.c(OH-)=c(H+)+c(HA-)
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-) D.c(Na+)=2c(A2-)+2c(HA-)
(3)水的电离平衡曲线如图所示。下列说法正确的是___ 。
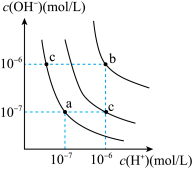
A.图中对应点的温度关系为:a>b>c
B.纯水仅升高温度,可从a点变到c点
C.水的电离常数Kw数值大小关系为:b>c>d
D.在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性
 H++A2-。回答下列问题:
H++A2-。回答下列问题:(1)Na2A溶液显碱性理由是:
(2)在0.1mol/L的Na2A溶液中,下列微粒浓度关系式正确的是
A.c(A2-)+c(HA-)+c(H2A)=0.1mol/L B.c(OH-)=c(H+)+c(HA-)
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-) D.c(Na+)=2c(A2-)+2c(HA-)
(3)水的电离平衡曲线如图所示。下列说法正确的是

A.图中对应点的温度关系为:a>b>c
B.纯水仅升高温度,可从a点变到c点
C.水的电离常数Kw数值大小关系为:b>c>d
D.在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)向0.1mol·L-1的氨水中加入少量的明矾,溶液中的 的浓度
的浓度___________ 。
(2)25℃,在0.10 H2S溶液中,通入HCI气体或加入
H2S溶液中,通入HCI气体或加入 固体以调节溶液pH,溶液pH与c(S2)关系如图(忽略溶液体积的变化、H2S的挥发)。
固体以调节溶液pH,溶液pH与c(S2)关系如图(忽略溶液体积的变化、H2S的挥发)。
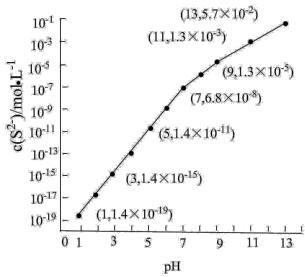
①pH=13时,溶液中的c(H2S)+c(HS-)=___________  。
。
②某溶液含0.020 Mn2+、0.10
Mn2+、0.10 H2S,当溶液pH=
H2S,当溶液pH=___________ 时,Mn2+开始沉淀。[已知: =2.8×10-13]
=2.8×10-13]
(3)25℃,两种酸的电离平衡常数如下表。
①0.10 NaHSO3溶液中粒子浓度由大到小的顺序为
NaHSO3溶液中粒子浓度由大到小的顺序为___________ 。
②向NaHCO3溶液中通入少量二氧化硫时反应的离子方程式___________ 。
(1)向0.1mol·L-1的氨水中加入少量的明矾,溶液中的
 的浓度
的浓度(2)25℃,在0.10
 H2S溶液中,通入HCI气体或加入
H2S溶液中,通入HCI气体或加入 固体以调节溶液pH,溶液pH与c(S2)关系如图(忽略溶液体积的变化、H2S的挥发)。
固体以调节溶液pH,溶液pH与c(S2)关系如图(忽略溶液体积的变化、H2S的挥发)。
①pH=13时,溶液中的c(H2S)+c(HS-)=
 。
。②某溶液含0.020
 Mn2+、0.10
Mn2+、0.10 H2S,当溶液pH=
H2S,当溶液pH= =2.8×10-13]
=2.8×10-13](3)25℃,两种酸的电离平衡常数如下表。
| Ka1 | Ka2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
 NaHSO3溶液中粒子浓度由大到小的顺序为
NaHSO3溶液中粒子浓度由大到小的顺序为②向NaHCO3溶液中通入少量二氧化硫时反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)25℃时,某Na2SO4溶液中c(SO )=1×10-4mol/L,则该溶液中c(Na+)∶c(OH-)=
)=1×10-4mol/L,则该溶液中c(Na+)∶c(OH-)=___ 。
(2)某温度(t℃)时,测得0.01mol·L-1的NaOH溶液的pH=11,在该温度下,纯水的Kw=___ 。此时,将pH=12的NaOH溶液VaL与pH=2的H2SO4溶液VbL混合,所得混合液为中性,则Va︰Vb=___ 。
(3)25℃时,已知0.1mol·L-1CH3COONa溶液pH=8,
①该溶液中离子浓度由大到小排列的顺序为:___ 。
②精确表达下列算式的数学结果:c(Na+)-c(CH3COO-)=___ ;c(OH-)-c(CH3COOH)=___ 。
(1)25℃时,某Na2SO4溶液中c(SO
 )=1×10-4mol/L,则该溶液中c(Na+)∶c(OH-)=
)=1×10-4mol/L,则该溶液中c(Na+)∶c(OH-)=(2)某温度(t℃)时,测得0.01mol·L-1的NaOH溶液的pH=11,在该温度下,纯水的Kw=
(3)25℃时,已知0.1mol·L-1CH3COONa溶液pH=8,
①该溶液中离子浓度由大到小排列的顺序为:
②精确表达下列算式的数学结果:c(Na+)-c(CH3COO-)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】研究电解质在水溶液中的平衡能了解它的存在形式。
(1)常温下,向100mL0.01mol•L-1HA的溶液中逐滴加入0.02mol•L-1MOH溶液,所得溶液的pH随MOH溶液的体积变化如图所示(溶液体积变化忽略不计)。

①常温下,0.01mol•L-1HA溶液中由水电离出的c(H+)=______ mol•L-1。
②常温下一定浓度的MA稀溶液的pH=a,则a__ 7(填“>”、“<”或“=”),用离子方程式表示其原因为_______________________________________ ;
③X点时,溶液中c(H+)、c(M+)、c(A—)由大到小的顺序是___________________ ;
④K点时,溶液中c(H+)+c(M+)—c(OH—)=____ mol•L-1。
⑵20℃时,在c(H2C2O4)+c(HC2O4—)+c(C2O42—)=0.100mol•L—1的H2C2O4、NaOH混合溶液中,H2C2O4、HC2O4-、C2O42-的物质的量分数δ随溶液pH变化的关系如图所示。

①Q点:c(H2C2O4)______ c(HC2O4—)(填“>”、“<”或“=”)
②该温度下HC2O4-的电离常数K=___________________ 。
(1)常温下,向100mL0.01mol•L-1HA的溶液中逐滴加入0.02mol•L-1MOH溶液,所得溶液的pH随MOH溶液的体积变化如图所示(溶液体积变化忽略不计)。

①常温下,0.01mol•L-1HA溶液中由水电离出的c(H+)=
②常温下一定浓度的MA稀溶液的pH=a,则a
③X点时,溶液中c(H+)、c(M+)、c(A—)由大到小的顺序是
④K点时,溶液中c(H+)+c(M+)—c(OH—)=
⑵20℃时,在c(H2C2O4)+c(HC2O4—)+c(C2O42—)=0.100mol•L—1的H2C2O4、NaOH混合溶液中,H2C2O4、HC2O4-、C2O42-的物质的量分数δ随溶液pH变化的关系如图所示。

①Q点:c(H2C2O4)
②该温度下HC2O4-的电离常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知:
(1)浓度均为0.05 mol·L-1的下列四种溶液,pH值最大的是________。
(2)将pH值和体积均相同的CH3COOH溶液和HClO溶液加水稀释,pH变化如图所示。下列说法正确的是_______。
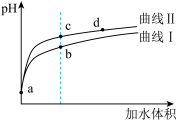
(3)从c→d过程中,下列数据变大的是_______。
(4)下列反应难以发生的是________。
(5)下列物质溶于水后溶液呈酸性的是_______(溶质不挥发)。
(6)向10mL浓度均为0.01 mol·L-1的HCl和CH3COOH的混合液中加入等体积0.02 mol·L-1的NaOH,充分反应后混合溶液呈_____ (选填编号);
A.酸性 B.碱性 C.中性
(7)上述混合液中离子浓度由大到小的顺序为________________ 。
(8)25℃时,用pH=3和pH=12的H2SO4溶液和NaOH溶液混合,使pH=11,则酸、碱溶液的体积比为___________ 。
| 25℃ | CH3COOH | H2CO3 | HClO | NH3·H2O |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4.5×10-7 Ka2=4.7×10-11 | Ka=3.0×10-8 | Kb=1.8×10-5 |
| A.CH3COONa | B.Na2CO3 | C.NaClO | D.NaHCO3 |

| A.曲线Ⅰ代表HClO溶液 | B.酸的浓度:CH3COOH>HClO |
| C.a点有[CH3COO-]>[ClO-] | D.水的电离程度:b点>c点 |
| A.[H+] | B. |
| C.[H+][OH-] | D.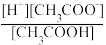 |
| A.2CH3COOH+Na2CO3=2CH3COONa+H2O+CO2↑ |
| B.HClO+Na2CO3=NaHCO3+NaClO |
| C.CH3COOH+NaClO=CH3COONa+HClO |
| D.HClO+NaHCO3=NaClO+H2O+CO2↑ |
| A.CH3COONH4 | B.(NH4)2CO3 |
| C.NH4HCO3 | D.等量CH3COOH与CH3COONa |
A.酸性 B.碱性 C.中性
(7)上述混合液中离子浓度由大到小的顺序为
(8)25℃时,用pH=3和pH=12的H2SO4溶液和NaOH溶液混合,使pH=11,则酸、碱溶液的体积比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】现有常温下浓度均为 的下列5种溶液:
的下列5种溶液: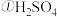 溶液
溶液  溶液
溶液  溶液
溶液 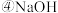 溶液
溶液  溶液
溶液
 这5种溶液pH由大到小的顺序是
这5种溶液pH由大到小的顺序是________________ ,其中由水电离的 浓度最小的是
浓度最小的是______ 。 填序号
填序号
 中各离子浓度由大到小的顺序是
中各离子浓度由大到小的顺序是________________________________________________________ , 的水解平衡常数
的水解平衡常数
_________________ 。 已知碳酸的电离常数
已知碳酸的电离常数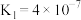 ,
,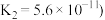
 向
向 中通入少量氨气,此时
中通入少量氨气,此时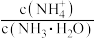 的值
的值__________  填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变” 。
。
 若将
若将 和
和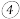 混合后溶液恰好呈中性,则混合前
混合后溶液恰好呈中性,则混合前 的体积
的体积______ 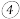 的体积
的体积 填“大于”、“小于”或“等于”
填“大于”、“小于”或“等于” 。
。
 将
将 的溶液分别蒸干并灼烧,最终可得原溶质的是
的溶液分别蒸干并灼烧,最终可得原溶质的是____________  填序号
填序号 。
。
 一定量的稀
一定量的稀 溶液与足量的Zn反应,为减缓产生的
溶液与足量的Zn反应,为减缓产生的 速率但又不影响
速率但又不影响 的总量,可采取的措施是
的总量,可采取的措施是______  填字母
填字母 。
。
A.加 固体
固体  加
加 固体
固体  加
加 溶液
溶液  加氨水
加氨水  加
加 溶液
溶液
 常温下,向
常温下,向 溶液中加入
溶液中加入 溶液,可观察到的现象是
溶液,可观察到的现象是_______________________________________ ,发生反应的离子方程式为______________________________ ,若将所得悬浊液的pH值调整为4,则溶液中 的溶液为
的溶液为_____ 
 已知常温下
已知常温下 。
。
 等体积、等浓度的氢氧化钠与醋酸混合后溶液呈
等体积、等浓度的氢氧化钠与醋酸混合后溶液呈____________ 性,溶液中
__________ 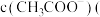 填“
填“ ”“
”“ ”或“
”或“ ”
” ;
; 的氢氧化钠与
的氢氧化钠与 的醋酸等体积混合后溶液呈
的醋酸等体积混合后溶液呈__________________ 性,溶液中
______ 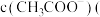 填“
填“ ”“
”“ ”或“
”或“ ”
” ;
;
 常温下,用
常温下,用 溶液滴定
溶液滴定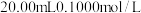 某一元酸HA溶液所得滴定曲线如图.
某一元酸HA溶液所得滴定曲线如图.

 A、B、C三点所示溶液导电能力最强的是
A、B、C三点所示溶液导电能力最强的是______ 点对应的溶液;
 点的离子浓度大小关系是
点的离子浓度大小关系是________________________________ .
 的下列5种溶液:
的下列5种溶液: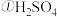 溶液
溶液  溶液
溶液  溶液
溶液 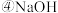 溶液
溶液  溶液
溶液 这5种溶液pH由大到小的顺序是
这5种溶液pH由大到小的顺序是 浓度最小的是
浓度最小的是 填序号
填序号
 中各离子浓度由大到小的顺序是
中各离子浓度由大到小的顺序是 的水解平衡常数
的水解平衡常数
 已知碳酸的电离常数
已知碳酸的电离常数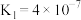 ,
,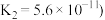
 向
向 中通入少量氨气,此时
中通入少量氨气,此时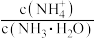 的值
的值 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变” 。
。 若将
若将 和
和 混合后溶液恰好呈中性,则混合前
混合后溶液恰好呈中性,则混合前 的体积
的体积 的体积
的体积 填“大于”、“小于”或“等于”
填“大于”、“小于”或“等于” 。
。 将
将 的溶液分别蒸干并灼烧,最终可得原溶质的是
的溶液分别蒸干并灼烧,最终可得原溶质的是 填序号
填序号 。
。 一定量的稀
一定量的稀 溶液与足量的Zn反应,为减缓产生的
溶液与足量的Zn反应,为减缓产生的 速率但又不影响
速率但又不影响 的总量,可采取的措施是
的总量,可采取的措施是 填字母
填字母 。
。A.加
 固体
固体  加
加 固体
固体  加
加 溶液
溶液  加氨水
加氨水  加
加 溶液
溶液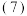 常温下,向
常温下,向 溶液中加入
溶液中加入 溶液,可观察到的现象是
溶液,可观察到的现象是 的溶液为
的溶液为
 已知常温下
已知常温下 。
。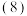 等体积、等浓度的氢氧化钠与醋酸混合后溶液呈
等体积、等浓度的氢氧化钠与醋酸混合后溶液呈
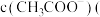 填“
填“ ”“
”“ ”或“
”或“ ”
” ;
; 的氢氧化钠与
的氢氧化钠与 的醋酸等体积混合后溶液呈
的醋酸等体积混合后溶液呈
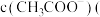 填“
填“ ”“
”“ ”或“
”或“ ”
” ;
; 常温下,用
常温下,用 溶液滴定
溶液滴定 某一元酸HA溶液所得滴定曲线如图.
某一元酸HA溶液所得滴定曲线如图.
 A、B、C三点所示溶液导电能力最强的是
A、B、C三点所示溶液导电能力最强的是 点的离子浓度大小关系是
点的离子浓度大小关系是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知25℃时,醋酸、碳酸、氢氰酸的电离平衡常数如下表:
(1)写出碳酸的第一步电离方程式_______ 。
(2)25℃时,等浓度的三种溶液①NaCN 溶液、②Na2CO3溶液、③CH3COONa 溶液,pH由大到小的顺序为_______ (填序号)。
(3)25℃时,H2SO3⇌HSO +H+的电离常数Ka=1×10-2mol/L,则该温度下pH=3、c(HSO
+H+的电离常数Ka=1×10-2mol/L,则该温度下pH=3、c(HSO )=0.1mol/L的NaHSO3溶液中c(H2SO3)=
)=0.1mol/L的NaHSO3溶液中c(H2SO3)=_______ 。
(4)下列方法中,可以使0.10mol/LCH3COOH溶液中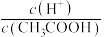 值增大的措施是
值增大的措施是_______ (填序号)。
a.加水稀释 b.加入少量CH3COONa固体 c.加入少量冰醋酸 d.通入少量HCl气体 e.加少量烧碱溶液 f.升高温度
(5)向20 mL硫酸和盐酸的混合溶液中,逐滴加入0.05 mol·L-1Ba(OH)2溶液时,生成沉淀的质量变化及由此而引起的溶液的pH的变化如图所示。计算:
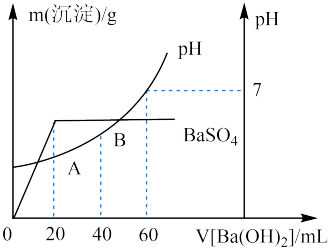
①原混合溶液中c(H+)=_______ ;c(Cl-)=_______ 。
②A点的pH=_______ 。
③将0.15mol·L-1稀硫酸V1mL与0.1mol·L-1NaOH溶液V2mL混合,所得溶液pH为1,则V1∶V2=_______ (溶液体积变化忽略不计)。
| 醋酸 | 碳酸 | 氢氰酸 |
Ka=1.7×10 | Ka1=4.2×10 Ka2=5.6×10  | Ka=6.2×10 |
(2)25℃时,等浓度的三种溶液①NaCN 溶液、②Na2CO3溶液、③CH3COONa 溶液,pH由大到小的顺序为
(3)25℃时,H2SO3⇌HSO
 +H+的电离常数Ka=1×10-2mol/L,则该温度下pH=3、c(HSO
+H+的电离常数Ka=1×10-2mol/L,则该温度下pH=3、c(HSO )=0.1mol/L的NaHSO3溶液中c(H2SO3)=
)=0.1mol/L的NaHSO3溶液中c(H2SO3)=(4)下列方法中,可以使0.10mol/LCH3COOH溶液中
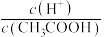 值增大的措施是
值增大的措施是a.加水稀释 b.加入少量CH3COONa固体 c.加入少量冰醋酸 d.通入少量HCl气体 e.加少量烧碱溶液 f.升高温度
(5)向20 mL硫酸和盐酸的混合溶液中,逐滴加入0.05 mol·L-1Ba(OH)2溶液时,生成沉淀的质量变化及由此而引起的溶液的pH的变化如图所示。计算:

①原混合溶液中c(H+)=
②A点的pH=
③将0.15mol·L-1稀硫酸V1mL与0.1mol·L-1NaOH溶液V2mL混合,所得溶液pH为1,则V1∶V2=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学上把外加少量酸、碱而pH基本不变的溶液称为缓冲溶液。回答下列问题:
I.25℃时,浓度均为0.1mol·L-1的CH3COOH和CH3COONa的缓冲溶液的pH=4.76。
(1)改变下列条件,能使CH3COONa稀溶液中 的值增大的是
的值增大的是___________ (填字母)。
a.加入少量CH3COONa固体 b.升温 c.稀释 d.加入NaOH固体 e.加入冰醋酸(忽略体积变化)
(2)该缓冲溶液中各离子浓度由小到大的顺序为___________ 。
(3)请用化学语言解释CH3COOH和CH3COONa组成的溶液具有一定的缓冲作用的原理________
II.人体血液里主要通过碳酸氢盐缓冲体系(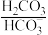 )维持pH稳定。
)维持pH稳定。
(4)已知正常人体血液在正常体温时,H2CO3的一级电离常数Ka1=10-6.1, ≈20,lg2=0.3,此时溶液的pH=
≈20,lg2=0.3,此时溶液的pH=___________ ,当过量的酸进入血液中时,血液缓冲体系中 的值将
的值将___________ (填“变大”、“变小”或“不变”)。
(5)某同学将0.1mol·L-1的NaHCO3溶液滴加到0.1mol·L-1的CaCl2溶液中,产生了白色沉淀和气体,试用离子方程式表示该过程:___________ 。
I.25℃时,浓度均为0.1mol·L-1的CH3COOH和CH3COONa的缓冲溶液的pH=4.76。
(1)改变下列条件,能使CH3COONa稀溶液中
 的值增大的是
的值增大的是a.加入少量CH3COONa固体 b.升温 c.稀释 d.加入NaOH固体 e.加入冰醋酸(忽略体积变化)
(2)该缓冲溶液中各离子浓度由小到大的顺序为
(3)请用化学语言解释CH3COOH和CH3COONa组成的溶液具有一定的缓冲作用的原理
II.人体血液里主要通过碳酸氢盐缓冲体系(
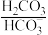 )维持pH稳定。
)维持pH稳定。(4)已知正常人体血液在正常体温时,H2CO3的一级电离常数Ka1=10-6.1,
 ≈20,lg2=0.3,此时溶液的pH=
≈20,lg2=0.3,此时溶液的pH= 的值将
的值将(5)某同学将0.1mol·L-1的NaHCO3溶液滴加到0.1mol·L-1的CaCl2溶液中,产生了白色沉淀和气体,试用离子方程式表示该过程:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】平衡思想是化学研究的一个重要观念,在水溶液中存在多种平衡体系。常温下,部分弱酸的电离平衡常数如下表:
已知 溶于水的过程及其平衡常数可表示为:
溶于水的过程及其平衡常数可表示为: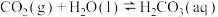
 ,
,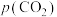 表示
表示 的平衡压强。
的平衡压强。
(1)天然雨水的 ,用电离方程式解释其原因
,用电离方程式解释其原因_______ 。
(2)将 通入
通入 水溶液中,发生的主要反应为
水溶液中,发生的主要反应为 。写出该反应的平衡常数表达式:
。写出该反应的平衡常数表达式:
_______ [用 、
、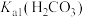 和
和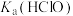 的式子表示]
的式子表示]
(3)下列方法中,可以使0.1
 溶液中
溶液中 的电离度增大的是_______。
的电离度增大的是_______。
(4)常温下,同浓度的① 、②
、② 、③
、③ 、④
、④ 这4种溶液中
这4种溶液中 由大到小的顺序是
由大到小的顺序是_______ (填编号)。
(5)若取 、体积均相等的盐酸和
、体积均相等的盐酸和 溶液,分别加水稀释m倍、n倍,稀释后
溶液,分别加水稀释m倍、n倍,稀释后 仍相等,则m
仍相等,则m_______ n(填“>”“<”或“=”)。
| 弱酸 |  |  |  |  |
| 电离平衡常数(25℃) | 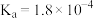 | 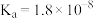 |  | 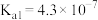  |
 溶于水的过程及其平衡常数可表示为:
溶于水的过程及其平衡常数可表示为: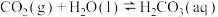
 ,
,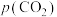 表示
表示 的平衡压强。
的平衡压强。(1)天然雨水的
 ,用电离方程式解释其原因
,用电离方程式解释其原因(2)将
 通入
通入 水溶液中,发生的主要反应为
水溶液中,发生的主要反应为 。写出该反应的平衡常数表达式:
。写出该反应的平衡常数表达式:
 、
、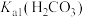 和
和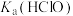 的式子表示]
的式子表示](3)下列方法中,可以使0.1

 溶液中
溶液中 的电离度增大的是_______。
的电离度增大的是_______。A.通入少量 气体 气体 | B.加入少量冰醋酸 |
| C.加入少量醋酸钠固体 | D.加入少量水 |
 、②
、② 、③
、③ 、④
、④ 这4种溶液中
这4种溶液中 由大到小的顺序是
由大到小的顺序是(5)若取
 、体积均相等的盐酸和
、体积均相等的盐酸和 溶液,分别加水稀释m倍、n倍,稀释后
溶液,分别加水稀释m倍、n倍,稀释后 仍相等,则m
仍相等,则m
您最近一年使用:0次



