某二元酸(H2A)在水中的电离方程式:H2A=H++HA-;HA- H++A2-。回答下列问题:
H++A2-。回答下列问题:
(1)Na2A溶液显碱性理由是:__ (用离子方程式表示)。
(2)在0.1mol/L的Na2A溶液中,下列微粒浓度关系式正确的是__ 。
A.c(A2-)+c(HA-)+c(H2A)=0.1mol/L B.c(OH-)=c(H+)+c(HA-)
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-) D.c(Na+)=2c(A2-)+2c(HA-)
(3)水的电离平衡曲线如图所示。下列说法正确的是___ 。
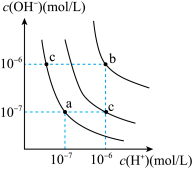
A.图中对应点的温度关系为:a>b>c
B.纯水仅升高温度,可从a点变到c点
C.水的电离常数Kw数值大小关系为:b>c>d
D.在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性
 H++A2-。回答下列问题:
H++A2-。回答下列问题:(1)Na2A溶液显碱性理由是:
(2)在0.1mol/L的Na2A溶液中,下列微粒浓度关系式正确的是
A.c(A2-)+c(HA-)+c(H2A)=0.1mol/L B.c(OH-)=c(H+)+c(HA-)
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-) D.c(Na+)=2c(A2-)+2c(HA-)
(3)水的电离平衡曲线如图所示。下列说法正确的是

A.图中对应点的温度关系为:a>b>c
B.纯水仅升高温度,可从a点变到c点
C.水的电离常数Kw数值大小关系为:b>c>d
D.在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性
2014·上海嘉定·三模 查看更多[1]
(已下线)上海市嘉定区2014届高三三模化学试题
更新时间:2020-03-23 19:32:25
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】水溶液中的离子平衡是中学学习的一个重要内容。
(1)下列溶液①0.10mol•L-1盐酸②0.10mol•L-1H2SO4溶液③0.10mol•L-1CH3COONa溶液④0.10mol•L-1NH4Cl溶液⑤0.10mol•L-1NaOH溶液,按pH由小到大顺序为____ (填序号)。
(2)在一定温度下,将一定质量冰醋酸加水稀释过程中溶液的导电能力变化如图所示。
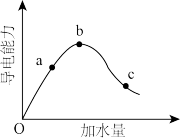
a、b、c三点对应的溶液中,CH3COOH电离程度最大的是____ ;a、b、c三点溶液用1mol•L-1NaOH溶液中和,消耗NaOH溶液体积大小关系____ 。
(3)已知25℃时,CO 水解反应的一级平衡常数Kh=2×10-4mol•L-1,写出此Kh的表达式
水解反应的一级平衡常数Kh=2×10-4mol•L-1,写出此Kh的表达式____ ;当溶液中c(HCO ):c(CO
):c(CO )=2:1时,溶液的pH=
)=2:1时,溶液的pH=___ 。
(4)SOCl2是一种液态化合物,将其滴入水中,可观察到剧烈反应,液面上有雾形成,并有带刺激性气味气体溢出,该气体可使品红溶液褪色,请根据实验现象写出SOCl2和H2O反应的化学方程式:____ 。
(5)等浓度的盐酸、氨水中,由水电离出的H+浓度c盐酸(H+)____ c氨水(H+)(填“>”“<”或“=”)。在25℃下,将amol•L-1的氨水与0.01mol•L-1的盐酸等体积混合充分反应后溶液呈中性。则反应后溶液存在的离子浓度由大到小顺序为____ ,用含a的代数式表示NH3•H2O的电离常数Kb=____ 。
(1)下列溶液①0.10mol•L-1盐酸②0.10mol•L-1H2SO4溶液③0.10mol•L-1CH3COONa溶液④0.10mol•L-1NH4Cl溶液⑤0.10mol•L-1NaOH溶液,按pH由小到大顺序为
(2)在一定温度下,将一定质量冰醋酸加水稀释过程中溶液的导电能力变化如图所示。

a、b、c三点对应的溶液中,CH3COOH电离程度最大的是
(3)已知25℃时,CO
 水解反应的一级平衡常数Kh=2×10-4mol•L-1,写出此Kh的表达式
水解反应的一级平衡常数Kh=2×10-4mol•L-1,写出此Kh的表达式 ):c(CO
):c(CO )=2:1时,溶液的pH=
)=2:1时,溶液的pH=(4)SOCl2是一种液态化合物,将其滴入水中,可观察到剧烈反应,液面上有雾形成,并有带刺激性气味气体溢出,该气体可使品红溶液褪色,请根据实验现象写出SOCl2和H2O反应的化学方程式:
(5)等浓度的盐酸、氨水中,由水电离出的H+浓度c盐酸(H+)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知常温下某二元弱酸(H2R)电离常数为Ka1=5×10-7,Ka2=5.6×10-11,HClO的Ka=3.0×10-8,回答下列问题:
(1)常温下向NaClO溶液加入少量的H2R溶液发生反应的离子方程式为___________________ 。
(2)常温下pH=3的HClO溶液浓度为c1,pH=4的HClO溶液浓度为c2,则c1____ 10c2(填“>”、“<”或“=”)。
(3)常温下2mol/L的H2R溶液的pH约为_______________ 。
(4)常温下0.1mol/L的NaHR溶液pH__________ 7(填“>”、“<”或“=”),溶液中的阴阳离子的浓度由大到小的顺序为___________________________________________ 。
(5)常温下,向10mL 0.1mol/L H2R溶液中滴加0.1mol/L的KOH溶液VmL。
①若混合后的溶液中离子浓度有如下关系:c(K+)=2c(R2-)+c(HR-),V______ 10(填“>”、“<”或“=”)。
②当混合后的溶液中离子浓度有如下关系:c(K+)=c(R2-)+c(HR-)+c(H2R),则溶液中溶质为_____________ ,V______ 10(填“>”、“<”或“=”)。
③当V=30时,混合后的溶液中c(OH-)-c(H+)-c(HR-)-2c(H2R)=________ mol/L。
(1)常温下向NaClO溶液加入少量的H2R溶液发生反应的离子方程式为
(2)常温下pH=3的HClO溶液浓度为c1,pH=4的HClO溶液浓度为c2,则c1
(3)常温下2mol/L的H2R溶液的pH约为
(4)常温下0.1mol/L的NaHR溶液pH
(5)常温下,向10mL 0.1mol/L H2R溶液中滴加0.1mol/L的KOH溶液VmL。
①若混合后的溶液中离子浓度有如下关系:c(K+)=2c(R2-)+c(HR-),V
②当混合后的溶液中离子浓度有如下关系:c(K+)=c(R2-)+c(HR-)+c(H2R),则溶液中溶质为
③当V=30时,混合后的溶液中c(OH-)-c(H+)-c(HR-)-2c(H2R)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下列物质中:①NaCl;②NaOH;③NH3·H2O;④CH3COOH溶液;⑤BaSO4;⑥H2O;⑦HCl;⑧H2SO4;⑨CO2;⑩酒精溶液(均填写编号回答)
(1)pH相等的②的溶液和③的溶液等体积加水稀释相同倍数后,pH大的是______ .
(2)有pH均为2的④、⑦、⑧三种物质的溶液,物质的量浓度大到小的顺序为______ ,若分别用这三种酸中和含等物质的量NaOH的溶液,所需酸溶液的体积分别为a、b、c,则a、b、c的大小关系是__________ .
(3)某温度时,1mol·L-1的醋酸溶液电离平衡常数为1.0×10-8,达平衡时,溶液中氢离子浓度是______________ .
(1)pH相等的②的溶液和③的溶液等体积加水稀释相同倍数后,pH大的是
(2)有pH均为2的④、⑦、⑧三种物质的溶液,物质的量浓度大到小的顺序为
(3)某温度时,1mol·L-1的醋酸溶液电离平衡常数为1.0×10-8,达平衡时,溶液中氢离子浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求回答下列问题:
(1)实验室中常用NaOH溶液来进行洗气和提纯,当用250 mL 1 mol/L的NaOH溶液吸收标准状况下3.36 L CO2时,所得溶液中各离子浓度由大到小的顺序为___________ 。
(2)知NaHSO3溶液和Na2CO3溶液混合加热煮沸能产生CO2气体。下列说法正确的是___________ (填选项字母)。
a.NaHSO3溶液因水解而呈碱性
b.两溶液混合产生CO2的原因是二者发生相互促进的水解反应
c.向NaHSO3溶液中加入三氯化铁溶液既有沉淀,又有气体生成
d.0.1mol/L的NaHSO3,溶液中:c( )+2c(
)+2c( )+c(OH-)-c(H+)=0.1 mol/L
)+c(OH-)-c(H+)=0.1 mol/L
(3)25℃下,向20 mL 0.1 mol/LNa2CO3溶液中逐滴加入0.1 mol/LHCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴),随溶液pH变化的部分情况如图所示。回答下列问题:

①在同一溶液中,H2CO3、 、
、
___________ (填“能”或“不能”)大量共存;
②当pH=7时,溶液中Na+、Cl-、 三种离子的浓度大小关系为
三种离子的浓度大小关系为___________ 。
③已知在25℃, 的第一步水解常数Kh1=2.0×10-4,当溶液中c(
的第一步水解常数Kh1=2.0×10-4,当溶液中c( ):c (
):c ( )=2:1时,溶液的pH=
)=2:1时,溶液的pH=______ 。
(1)实验室中常用NaOH溶液来进行洗气和提纯,当用250 mL 1 mol/L的NaOH溶液吸收标准状况下3.36 L CO2时,所得溶液中各离子浓度由大到小的顺序为
(2)知NaHSO3溶液和Na2CO3溶液混合加热煮沸能产生CO2气体。下列说法正确的是
a.NaHSO3溶液因水解而呈碱性
b.两溶液混合产生CO2的原因是二者发生相互促进的水解反应
c.向NaHSO3溶液中加入三氯化铁溶液既有沉淀,又有气体生成
d.0.1mol/L的NaHSO3,溶液中:c(
 )+2c(
)+2c( )+c(OH-)-c(H+)=0.1 mol/L
)+c(OH-)-c(H+)=0.1 mol/L(3)25℃下,向20 mL 0.1 mol/LNa2CO3溶液中逐滴加入0.1 mol/LHCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴),随溶液pH变化的部分情况如图所示。回答下列问题:

①在同一溶液中,H2CO3、
 、
、
②当pH=7时,溶液中Na+、Cl-、
 三种离子的浓度大小关系为
三种离子的浓度大小关系为③已知在25℃,
 的第一步水解常数Kh1=2.0×10-4,当溶液中c(
的第一步水解常数Kh1=2.0×10-4,当溶液中c( ):c (
):c ( )=2:1时,溶液的pH=
)=2:1时,溶液的pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】 、
、 在医药、电子工业中用途广泛。请回答下列问题:
在医药、电子工业中用途广泛。请回答下列问题:
(1)常温时, 溶液的
溶液的 。该溶液中,
。该溶液中,
___________ (填“>”“=”或“<”) ;
;
___________ mol/L。
(2)80℃时, 溶液的pH小于3,分析导致pH随温度变化的原因:
溶液的pH小于3,分析导致pH随温度变化的原因:___________ 。
(3)常温时,向 溶液中滴加
溶液中滴加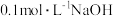 溶液,得到溶液的pH与NaOH溶液体积的关系曲线如图所示。
溶液,得到溶液的pH与NaOH溶液体积的关系曲线如图所示。

①向 溶液中滴加NaOH溶液到a点的过程中,发生反应的离子方程式为
溶液中滴加NaOH溶液到a点的过程中,发生反应的离子方程式为___________ 。
②图中a、b、c、d点中水的电离程度最小的是___________ 。
 、
、 在医药、电子工业中用途广泛。请回答下列问题:
在医药、电子工业中用途广泛。请回答下列问题:(1)常温时,
 溶液的
溶液的 。该溶液中,
。该溶液中,
 ;
;
(2)80℃时,
 溶液的pH小于3,分析导致pH随温度变化的原因:
溶液的pH小于3,分析导致pH随温度变化的原因:(3)常温时,向
 溶液中滴加
溶液中滴加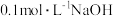 溶液,得到溶液的pH与NaOH溶液体积的关系曲线如图所示。
溶液,得到溶液的pH与NaOH溶液体积的关系曲线如图所示。
①向
 溶液中滴加NaOH溶液到a点的过程中,发生反应的离子方程式为
溶液中滴加NaOH溶液到a点的过程中,发生反应的离子方程式为②图中a、b、c、d点中水的电离程度最小的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】室温下向10mL0.1mol·L-1NaOH溶液中逐滴加入0.1mol·L-1的一元酸HA溶液,溶液pH的变化曲线如图所示。

(1)a点(横坐标为10)所示溶液中离子浓度从大到小的顺序为___ ,其中c(Na+)___ (填“>”“<”或“=”)c(A-)+c(HA)。
(2)c点所示溶液中,c(Na+)___ (填“>”“<”或“=”)c(A-)。
(3)b点所示溶液中,c(A-)___ (填“>”“<”或“=”)c(HA)。
(4)以下滴定操作会导致V(HA溶液)偏大的是___ 。
A.滴定管滴定前有气泡,滴定后气泡消失
B.锥形瓶洗涤后没有干燥
C.滴定时锥形瓶中有液体溅出
D.滴定开始前读数时平视,滴定终点读数时俯视

(1)a点(横坐标为10)所示溶液中离子浓度从大到小的顺序为
(2)c点所示溶液中,c(Na+)
(3)b点所示溶液中,c(A-)
(4)以下滴定操作会导致V(HA溶液)偏大的是
A.滴定管滴定前有气泡,滴定后气泡消失
B.锥形瓶洗涤后没有干燥
C.滴定时锥形瓶中有液体溅出
D.滴定开始前读数时平视,滴定终点读数时俯视
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表所示的是某些弱酸的电离常数(常温下),请根据要求作答。
(1)比较上述四种酸的酸性强弱____________________________________________
(2)写出1mol/L的NaHCO3溶液中的电荷守恒表达式:__________________________________ 。
(3)写出0.1mol/L NaHC2O4溶液中c(Na+)、c(HC2O4-)、c(OH-)、c(H+)的大小顺序(HC2O4- 的电离程度大于水解程度)。__________________________________________________________
| 弱酸 | 电离常数 | 弱酸 | 电离常数 |
| H2CO3 | K1=4.4 ×10-7 K2=4.7 × 10-11 | CH3COOH | K=1.75×10-5 |
| H3PO4 | K1=7.1×10-3 K2=6.3×10-8 K3=4.2×10-13 | H2C2O4 | K1=5.4×10-2 K2=5.4 ×10-5 |
(1)比较上述四种酸的酸性强弱
(2)写出1mol/L的NaHCO3溶液中的电荷守恒表达式:
(3)写出0.1mol/L NaHC2O4溶液中c(Na+)、c(HC2O4-)、c(OH-)、c(H+)的大小顺序(HC2O4- 的电离程度大于水解程度)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】甲、乙、丙、丁代表不同的一元酸,常温下,将它们分别和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合后溶液的pH如下表所示:
完成下列填空:
(1)从实验1情况分析,如何判断HA是强酸还是弱酸?___________
(2)实验2的混合溶液中c(A-)和c(Na+)的大小关系为___________ 。
(3)从实验3分析,该混合溶液中离子浓度由大到小的顺序是___________ 。
(4)分析实验4数据,写出混合溶液中下列算式的精确结果(列式即可):c(Na+)-c(A-)=___________ mol·L-1
| 实验序号 | 所用酸 | c(HA)/mol·L-1 | c(NaOH)/mol·L-1 | 混合后溶液的pH |
| 实验1 | 甲 | 0.1000 | 0.1000 | pH=a |
| 实验2 | 乙 | 0.1200 | 0.1000 | pH=7 |
| 实验3 | 丙 | 0.2000 | 0.1000 | pH>7 |
| 实验4 | 丁 | 0.1000 | 0.1000 | pH=10 |
(1)从实验1情况分析,如何判断HA是强酸还是弱酸?
(2)实验2的混合溶液中c(A-)和c(Na+)的大小关系为
(3)从实验3分析,该混合溶液中离子浓度由大到小的顺序是
(4)分析实验4数据,写出混合溶液中下列算式的精确结果(列式即可):c(Na+)-c(A-)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求回答下列问题:.
(1)室温下,用0.1mol/LNaOH溶液滴定20.00mL浓度为0.1mol/L的HA酸的溶液,滴定过程中溶液的pH随滴入的NaOH溶液体积的变化如图:
①a点对应的溶液中c(HA)____ c(A-)(选填“>”“<”或“=”);b点对应的溶液中各离子浓度由大到小的顺序为_________ 。
②K(HA)=_________ 。
(2)已知:T℃时,Kw=1×10-12。在T℃时,将pH=9的NaOH溶液aL与pH=2的H2SO4溶液bL混合(注:混合后溶液体积等于混合前两溶液体积之和)。若所得混合溶液的pH=3,则a:b=_________ 。
(1)室温下,用0.1mol/LNaOH溶液滴定20.00mL浓度为0.1mol/L的HA酸的溶液,滴定过程中溶液的pH随滴入的NaOH溶液体积的变化如图:

①a点对应的溶液中c(HA)
②K(HA)=
(2)已知:T℃时,Kw=1×10-12。在T℃时,将pH=9的NaOH溶液aL与pH=2的H2SO4溶液bL混合(注:混合后溶液体积等于混合前两溶液体积之和)。若所得混合溶液的pH=3,则a:b=
您最近一年使用:0次



