1 . 叠氮化钠(NaN3)是一种白色剧毒晶体,是常作为汽车安全气囊的药剂,其固体易溶于水,微溶于乙醇,不溶于乙醚,能与酸发生反应产生具有爆炸性的有毒气体叠氮化氢。实验室常通过以下方案制备叠氮化钠:
方案一:亚硝酸叔丁酯与N2H4、氢氧化钠溶液混合反应制备叠氮化钠;
方案二:I.2Na+NH3 2NaNH2+H2;II.NaNH2+N2O
2NaNH2+H2;II.NaNH2+N2O NaN3+H2O。
NaN3+H2O。
(1)方案一中制备亚硝酸叔丁酯的方法:取一定量NaNO2溶液与50%硫酸混合,发生反应:H2SO4+2NaNO2=2HNO2+Na2SO4;利用亚硝酸与叔丁醇(t-BuOH,以t-Bu表示叔丁基)在40℃左右制备亚硝酸叔丁酯,试写出该反应的化学方程式____ 。
(2)方案二的装置及主要步骤如图所示:

①组装仪器检查装置气性后,装入药品,a中加入____ ,c中加入____ 。
②实验过程应先点燃____ (填“A”或“D”)的酒精灯,理由是____ 。
③在反应I充分进行后,通入N2O气体,d中采用____ 加热进行反应II。
④装置D反应完全结束后,取出混合物进行以下操作,得到NaN3固体:

已知:NaNH2能与水反应生成NaOH和氨气。操作II的目的是____ ;操作IV最好选用的试剂是____ 。
(3)产率计算
①称取2.0g叠氮化钠试样,配成100mL溶液,并量取10.00mL溶液于锥形瓶中。
②用滴定管加入0.10mol•L-1六硝酸铈铵[(NH4)2Ce(NO3)6]溶液40.00mL[发生的反应为:2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑](杂质均不参与反应)。
③充分反应后将溶液稀释并酸化,滴入2滴邻菲罗啉指示液,并用0.10mol•L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]为标准液,滴定过量的Ce4+,终点时消耗标准溶液20.00mL(滴定原理:Ce4++Fe2+=Ce3++Fe3+)。
计算可知叠氮化钠的质量分数为____ (保留2位有效数字)。
方案一:亚硝酸叔丁酯与N2H4、氢氧化钠溶液混合反应制备叠氮化钠;
方案二:I.2Na+NH3
 2NaNH2+H2;II.NaNH2+N2O
2NaNH2+H2;II.NaNH2+N2O NaN3+H2O。
NaN3+H2O。(1)方案一中制备亚硝酸叔丁酯的方法:取一定量NaNO2溶液与50%硫酸混合,发生反应:H2SO4+2NaNO2=2HNO2+Na2SO4;利用亚硝酸与叔丁醇(t-BuOH,以t-Bu表示叔丁基)在40℃左右制备亚硝酸叔丁酯,试写出该反应的化学方程式
(2)方案二的装置及主要步骤如图所示:

①组装仪器检查装置气性后,装入药品,a中加入
②实验过程应先点燃
③在反应I充分进行后,通入N2O气体,d中采用
④装置D反应完全结束后,取出混合物进行以下操作,得到NaN3固体:

已知:NaNH2能与水反应生成NaOH和氨气。操作II的目的是
(3)产率计算
①称取2.0g叠氮化钠试样,配成100mL溶液,并量取10.00mL溶液于锥形瓶中。
②用滴定管加入0.10mol•L-1六硝酸铈铵[(NH4)2Ce(NO3)6]溶液40.00mL[发生的反应为:2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑](杂质均不参与反应)。
③充分反应后将溶液稀释并酸化,滴入2滴邻菲罗啉指示液,并用0.10mol•L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]为标准液,滴定过量的Ce4+,终点时消耗标准溶液20.00mL(滴定原理:Ce4++Fe2+=Ce3++Fe3+)。
计算可知叠氮化钠的质量分数为
您最近一年使用:0次
解题方法
2 . 在指定条件下,下列选项所示物质间转化能实现的是
A. | B.浓 |
C. | D. |
您最近一年使用:0次
解题方法
3 . 依据下图氮元素及其化合物的转化关系,回答问题:

(1)实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为_______ 。
(2)下列试剂不能用于干燥NH3的是_______ 。
A.浓硫酸 B.碱石灰 C.NaOH固体
(3)工业上以NH3、空气、水为原料生产硝酸分为三步:
①加热时NH3可催化氧化为NO,化学方程式为_______ 。
②NO→NO2反应的实验现象是_______ 。
③NO2+H2O→HNO3中氧化剂与还原剂物质的量之比为_______ 。
(4)若要将NH3→N2,从原理上看,下列试剂可行的是_______。

(1)实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为
(2)下列试剂不能用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.NaOH固体
(3)工业上以NH3、空气、水为原料生产硝酸分为三步:
①加热时NH3可催化氧化为NO,化学方程式为
②NO→NO2反应的实验现象是
③NO2+H2O→HNO3中氧化剂与还原剂物质的量之比为
(4)若要将NH3→N2,从原理上看,下列试剂可行的是_______。
| A.O2 | B.Na | C.NH4Cl | D.NO2 |
您最近一年使用:0次
名校
4 . 下列化合物的性质与用途具有对应关系的是
| A.NH3有还原性,可用于制硝酸 | B.N2性质活泼,可用于保护粮食 |
| C.NaHCO3受热易分解,可用作胃酸中和剂 | D.Na2O2有强还原性,可用于杀菌消毒 |
您最近一年使用:0次
解题方法
5 . 合成氨及其相关工业中,部分物质间的转化关系如下:
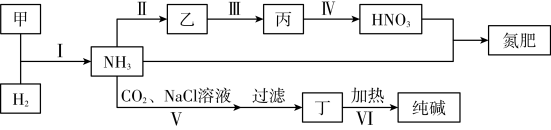
下列说法不正确的是

下列说法不正确的是
| A.甲、乙、丙三种物质中都含有氮元素 |
| B.反应IV的氧化剂是H2O |
| C.VI的产物可在上述流程中被再次利用 |
| D.V中发生反应:NH3+CO2+H2O+NaCl═NaHCO3↓+NH4Cl |
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
6 . 氨可被氯气氧化生成N2,同时还可能产生白烟现象。(_______)
您最近一年使用:0次
7 . 下图是氮元素及其化合物的转化关系,下列说法正确的是


A. 的电子式为 的电子式为 |
B. 的酸酐是 的酸酐是 |
C. 的转化反应属于氮的固定 的转化反应属于氮的固定 |
D.一定条件下, 可与NO反应实现 可与NO反应实现 的转化 的转化 |
您最近一年使用:0次
名校
解题方法
8 . 下列选项所示的物质间转化均能实现的是
A. |
B. |
C. |
D. |
您最近一年使用:0次
2022-07-01更新
|
248次组卷
|
2卷引用:浙江省舟山市舟山中学2021-2022学年高三上学期开学考试化学试题
名校
9 . 元素的价-类二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图象。结合氮及其化合物“价类”二维图,下列分析或预测正确的是


| A.N2O3、NO2、N2O5均能与水反应生成酸,三者均为酸性氧化物 |
| B.HNO3、HNO3、NaNO3、NH3的水溶液均可以导电,四者均属于电解质 |
| C.可用浓盐酸检测输送NH3的管道是否发生泄漏 |
| D.HNO3具有强氧化性,可溶解铜、银、金等不活泼金属 |
您最近一年使用:0次
名校
解题方法
10 . 天然脑砂含少量 ,《唐本草》记载脑砂入药可以散瘀消肿。某学习小组设计下列步骤制取
,《唐本草》记载脑砂入药可以散瘀消肿。某学习小组设计下列步骤制取 ,并进行天然脑砂含量的测定。请回答相关问题:
,并进行天然脑砂含量的测定。请回答相关问题:
步骤Ⅰ:用氨气与适量氯气反应制取 。
。_______ ;若用浓盐酸与 反应制取氯气,则该反应的离子方程式为
反应制取氯气,则该反应的离子方程式为_______ 。
(2)要得到干燥纯净的氯气,C的作用是_______ 。
(3)氨气与适量氯气混合反应可生成 和一种无污染的气体,利用E装置模拟该反应,氨气应从
和一种无污染的气体,利用E装置模拟该反应,氨气应从_______ (填“f”或“g”)通入,反应的化学方程式为_______ 。
步骤Ⅱ:天然脑砂中 含量的测定。
含量的测定。
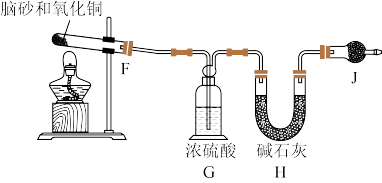
准确称取一定质量脑砂,与足量的氧化铜混合,如图所示进行实验。
已知: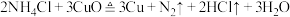 。
。 含量的测定,请完成下列实验步骤:加热前,称量H装置的总质量;当观察到G中不再有气泡冒出时,停止加热,冷却,
含量的测定,请完成下列实验步骤:加热前,称量H装置的总质量;当观察到G中不再有气泡冒出时,停止加热,冷却,_______ 。
(5)如果不用J装置,测出 的含量将
的含量将_______ (填“偏高”“偏低”或“无影响”)。
 ,《唐本草》记载脑砂入药可以散瘀消肿。某学习小组设计下列步骤制取
,《唐本草》记载脑砂入药可以散瘀消肿。某学习小组设计下列步骤制取 ,并进行天然脑砂含量的测定。请回答相关问题:
,并进行天然脑砂含量的测定。请回答相关问题:步骤Ⅰ:用氨气与适量氯气反应制取
 。
。
 反应制取氯气,则该反应的离子方程式为
反应制取氯气,则该反应的离子方程式为(2)要得到干燥纯净的氯气,C的作用是
(3)氨气与适量氯气混合反应可生成
 和一种无污染的气体,利用E装置模拟该反应,氨气应从
和一种无污染的气体,利用E装置模拟该反应,氨气应从步骤Ⅱ:天然脑砂中
 含量的测定。
含量的测定。准确称取一定质量脑砂,与足量的氧化铜混合,如图所示进行实验。
已知:
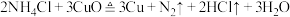 。
。
 含量的测定,请完成下列实验步骤:加热前,称量H装置的总质量;当观察到G中不再有气泡冒出时,停止加热,冷却,
含量的测定,请完成下列实验步骤:加热前,称量H装置的总质量;当观察到G中不再有气泡冒出时,停止加热,冷却,(5)如果不用J装置,测出
 的含量将
的含量将
您最近一年使用:0次
2022-06-19更新
|
357次组卷
|
3卷引用:湖南省长沙市第一中学2020-2021学年高一下学期期末考试化学试题



