1 . 氨气遇到氯气会产生白烟。氯碱工业中用氨气检验氯气管道是否泄漏。
(1)已知白烟成分是氯化铵,反应还生成一种无毒的气态单质。试写出反应的化学方程式:_________ 。
(2)在反应中,每生成1mol氯化铵,有_________ mol氯气被还原,_________ mol氨气被氧化,发生反应的氨气是_________ mol。
(1)已知白烟成分是氯化铵,反应还生成一种无毒的气态单质。试写出反应的化学方程式:
(2)在反应中,每生成1mol氯化铵,有
您最近一年使用:0次
解题方法
2 . 图是工业上制备硝酸的设备和流程示意图。主要的化学反应如下:
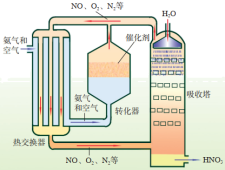
(1)氨在催化剂作用下与氧气发生反应,生成一氧化氮。
(2)一氧化氮进一步被氧气氧化,生成二氧化氮。
(3)用水吸收二氧化氮,生成硝酸。
请写出工业上制备硝酸的化学方程式_________ 。

(1)氨在催化剂作用下与氧气发生反应,生成一氧化氮。
(2)一氧化氮进一步被氧气氧化,生成二氧化氮。
(3)用水吸收二氧化氮,生成硝酸。
请写出工业上制备硝酸的化学方程式
您最近一年使用:0次
解题方法
3 . 已知氨可以与灼热的氧化铜反应生成氮气和金属铜,用下面示意图中的装置可以实现该反应。
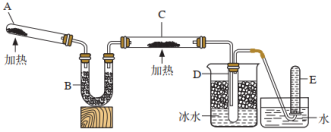
A中装有的NH4Cl和Ca(OH)2混合物在加热条件下,可以发生反应生成CaCl2、NH3和H2O。
试回答下列问题:
(1)B中加入的物质是碱石灰(CaO和NaOH的混合物),其作用是____ 。
(2)实验时在C中观察到的现象是____ ,发生反应的化学方程式是_____ 。
(3)实验时在D中观察到的现象是____ ,收集到的物质是____ 。

A中装有的NH4Cl和Ca(OH)2混合物在加热条件下,可以发生反应生成CaCl2、NH3和H2O。
试回答下列问题:
(1)B中加入的物质是碱石灰(CaO和NaOH的混合物),其作用是
(2)实验时在C中观察到的现象是
(3)实验时在D中观察到的现象是
您最近一年使用:0次
4 . 工业上硝酸的制备和自然界中硝酸的生成既有相同的地方,又有区别。线路①②③是工业生产硝酸的主要途径,线路I、II、III是雷电固氮过程中硝酸的产生途径。
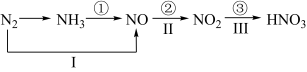
(1)写出各变化的化学方程式,如果属于氧化还原反应,指出其中的氧化剂和还原剂____ 、____ 、____ 、____ 、____ 。
(2)硝酸生产过程中排放出来的一氧化氮是大气污染物之一。目前有一种治理方法,是在400℃左右且有催化剂存在的条件下,用氨把一氧化氮还原成可直接排入大气的无色无毒气体。请写出有关反应的化学方程式____ 。

(1)写出各变化的化学方程式,如果属于氧化还原反应,指出其中的氧化剂和还原剂
(2)硝酸生产过程中排放出来的一氧化氮是大气污染物之一。目前有一种治理方法,是在400℃左右且有催化剂存在的条件下,用氨把一氧化氮还原成可直接排入大气的无色无毒气体。请写出有关反应的化学方程式
您最近一年使用:0次
名校
解题方法
5 . 甲、乙两个研究性学习小组为测定氨分子中氮、氢原子个数比,设计了如下实验流程:

实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜。反应完成后,黑色的氧化铜转化为红色的铜。反应方程式:2NH3+3CuO N2+3Cu+3H2O。下图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。
N2+3Cu+3H2O。下图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。

甲小组测得:反应前氧化铜的质量为m1 g、氧化铜反应后剩余固体的质量为m2 g、生成的氮气在标准状况下的体积为V1 L。
乙小组测得:洗气前装置D的质量为m3 g、洗气后装置D的质量为m4 g、生成的氮气在标准状况下的体积为V2 L。
请回答下列问题:
(1)写出仪器a的名称:_______ 。
(2)检查装置A气密性的操作是_______ 。
(3)甲、乙两小组选择了不同的方法制取氨气,请将实验装置的字母编号和制备原理填写在下表的空格中:
(4)甲小组用所测数据计算出氨分子中氮、氢的原子个数之比为_______ 。
(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数比明显小于理论值,其原因是_______ 。为此,乙小组在原有实验的基础上增加了一个装有某药品的实验仪器,重新实验。根据实验前后该药品的质量变化及生成氮气的体积,得出了合理的实验结果。该药品的名称是_______ 。

实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜。反应完成后,黑色的氧化铜转化为红色的铜。反应方程式:2NH3+3CuO
 N2+3Cu+3H2O。下图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。
N2+3Cu+3H2O。下图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。
甲小组测得:反应前氧化铜的质量为m1 g、氧化铜反应后剩余固体的质量为m2 g、生成的氮气在标准状况下的体积为V1 L。
乙小组测得:洗气前装置D的质量为m3 g、洗气后装置D的质量为m4 g、生成的氮气在标准状况下的体积为V2 L。
请回答下列问题:
(1)写出仪器a的名称:
(2)检查装置A气密性的操作是
(3)甲、乙两小组选择了不同的方法制取氨气,请将实验装置的字母编号和制备原理填写在下表的空格中:
| 实验装置 | 实验药品 | 制备原理 | |
| 甲小组 | A | 氢氧化钙、氯化铵 | 反应的化学方程式: |
| 乙小组 | 浓氨水、氢氧化钠 | 氢氧化钠溶于水会放热,且使溶液碱性增强,促进氨气逸出 |
(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数比明显小于理论值,其原因是
您最近一年使用:0次
2022-03-24更新
|
348次组卷
|
4卷引用:人教版2019必修第二册 第五章 本章达标检测
6 . NO是大气污染物之一、目前有一种治理方法是在400℃左右、有催化剂存在的条件下,使 与NO反应生成无污染的
与NO反应生成无污染的 和
和 。请写出该反应的化学方程式。
。请写出该反应的化学方程式。___________
 与NO反应生成无污染的
与NO反应生成无污染的 和
和 。请写出该反应的化学方程式。
。请写出该反应的化学方程式。
您最近一年使用:0次
7 . 氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。

(1)写出合成塔和氧化炉中发生反应的化学方程式____ ,并指出其中的氧化剂和还原剂__ 。
(2)请思考A是什么物质_______ ,以及向吸收塔中通入A的作用_________ 。
(3)工业生产中为了盛装大量浓硝酸,可选择_______ 作为罐体材料。
a.铜 b.铂 c.铝 d.镁
(4)为避免硝酸生产尾气中的氮氧化物污染环境,人们开发了溶液吸收、催化还原等尾气处理方法。前者使用具有碱性的 溶液等吸收尾气,后者使用
溶液等吸收尾气,后者使用 或其他物质将氮氧化物还原为
或其他物质将氮氧化物还原为 。请以尾气中的
。请以尾气中的 处理为例,写出相关反应的化学方程式
处理为例,写出相关反应的化学方程式___ ,并查阅资料,了解还有哪些尾气处理方法______ 。

(1)写出合成塔和氧化炉中发生反应的化学方程式
(2)请思考A是什么物质
(3)工业生产中为了盛装大量浓硝酸,可选择
a.铜 b.铂 c.铝 d.镁
(4)为避免硝酸生产尾气中的氮氧化物污染环境,人们开发了溶液吸收、催化还原等尾气处理方法。前者使用具有碱性的
 溶液等吸收尾气,后者使用
溶液等吸收尾气,后者使用 或其他物质将氮氧化物还原为
或其他物质将氮氧化物还原为 。请以尾气中的
。请以尾气中的 处理为例,写出相关反应的化学方程式
处理为例,写出相关反应的化学方程式
您最近一年使用:0次
2021-12-02更新
|
1370次组卷
|
2卷引用:人教2019版必修第二册第五章 化工生产中的重要非金属元素复习与提高
8 . 在下图所示的物质转化关系中,A是常见的气态氢化物,B是能使带火星的木条复燃的无色、无味气体,E的相对分子质量比D的大17,G是一种紫红色金属单质(反应条件和部分生成物未列出)。
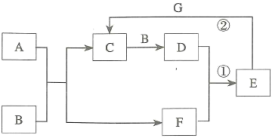
(1)A的电子式为___________ ,B的化学式为___________ 。
(2)请写出:
反应①的化学方程式_________
反应②的离子方程式____________ 。

(1)A的电子式为
(2)请写出:
反应①的化学方程式
反应②的离子方程式
您最近一年使用:0次
2021-12-02更新
|
1104次组卷
|
2卷引用:人教2019版必修第二册第五章 化工生产中的重要非金属元素复习与提高
21-22高一上·浙江绍兴·期中
名校
9 . 下列物质的转化在给定条件下能实现的是
A.Fe 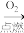 Fe2O3 Fe2O3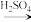 Fe2(SO4)3 Fe2(SO4)3 | B.S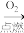 SO3 SO3 H2SO4 H2SO4 |
C.SO2 H2SO3 H2SO3 H2SO4 H2SO4 | D.NH3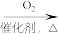 NO NO HNO3 HNO3 |
您最近一年使用:0次
2021-11-23更新
|
454次组卷
|
3卷引用:第三章 单元检测-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)
(已下线)第三章 单元检测-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)浙江省绍兴市诸暨中学2021-2022学年高一上学期期中考试(实验班)化学试题浙江省瑞安市瑞祥高级中学2022-2023学年高一上学期期末考试化学试题
21-22高三上·河南郑州·期中
名校
解题方法
10 . 在给定条件下,下列选项正确的是
①NaHCO3 Na2CO3
Na2CO3 NaOH
NaOH
②CaCO3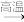 CaO
CaO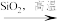 CaSiO3
CaSiO3
③NH3 NO
NO  HNO3
HNO3
④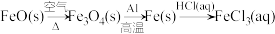
⑤S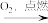 SO3
SO3 H2SO4
H2SO4
⑥
①NaHCO3
 Na2CO3
Na2CO3 NaOH
NaOH ②CaCO3
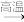 CaO
CaO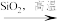 CaSiO3
CaSiO3③NH3
 NO
NO  HNO3
HNO3④
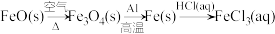
⑤S
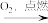 SO3
SO3 H2SO4
H2SO4 ⑥

| A.有2项能实现 | B.有3项能实现 |
| C.有4项能实现 | D.以上转化均不能实现 |
您最近一年使用:0次
2021-11-22更新
|
476次组卷
|
3卷引用:3.3 氮的循环-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)
(已下线)3.3 氮的循环-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)河南省实验中学2021-2022学年高三上学期期中考试化学试题江西省南昌市第二中学2022-2023学年高三上学期第四次考试化学试题



