解题方法
1 . 某小组同学欲探究 催化氧化反应,按如图装置进行实验。
催化氧化反应,按如图装置进行实验。
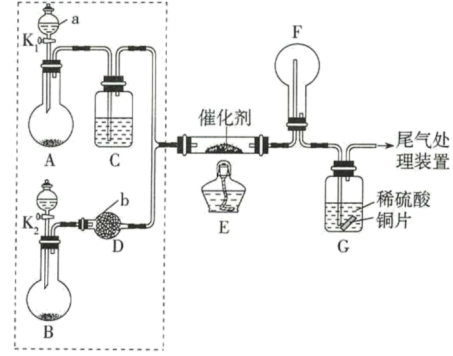
已知A、B装置可选药品:浓氨水、 、蒸馏水、生石灰、
、蒸馏水、生石灰、 。
。
(1)仪器a的名称为___________ ;仪器b的名称为___________ 。
(2)装置A烧瓶中固体的作用为___________ (填序号)。
A.催化剂 B.氧化剂 C.还原剂 D.反应物
(3)仪器b中盛放的试剂可以是___________ (填序号)。
A.浓硫酸 B.碱石灰 C.五氧化二磷 D.硫酸铜
(4)装置E中发生反应的化学方程式为___________ 。
(5)甲,乙两同学分别按上述装置进行实验,一段时间后。甲同学观察到装置F中只有白烟生成,白烟的成分是___________ (写化学式)。
(6)为帮助甲同学实现在装置F中也观察到红棕色气体,可在原实验的基础上进行改进。你的改进措施是___________ 。
 催化氧化反应,按如图装置进行实验。
催化氧化反应,按如图装置进行实验。
已知A、B装置可选药品:浓氨水、
 、蒸馏水、生石灰、
、蒸馏水、生石灰、 。
。(1)仪器a的名称为
(2)装置A烧瓶中固体的作用为
A.催化剂 B.氧化剂 C.还原剂 D.反应物
(3)仪器b中盛放的试剂可以是
A.浓硫酸 B.碱石灰 C.五氧化二磷 D.硫酸铜
(4)装置E中发生反应的化学方程式为
(5)甲,乙两同学分别按上述装置进行实验,一段时间后。甲同学观察到装置F中只有白烟生成,白烟的成分是
(6)为帮助甲同学实现在装置F中也观察到红棕色气体,可在原实验的基础上进行改进。你的改进措施是
您最近一年使用:0次
解题方法
2 . 下列反应中,不能表现氨气还原性的是
A.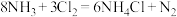 |
B. |
C. |
D. |
您最近一年使用:0次
2021-01-08更新
|
156次组卷
|
3卷引用:专题7 第二单元 第1课时 氨气-高中化学必修第二册苏教版2019
专题7 第二单元 第1课时 氨气-高中化学必修第二册苏教版2019(已下线)3.2.1 固氮和氨气-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)天津市武清区黄花店中学2023-2024学年高一下学期第一次月考化学试题(文科)
解题方法
3 .  、NO和
、NO和 等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(1) 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为_____________________________________ 。
(2)NO和 的处理。已除去
的处理。已除去 的硝酸尾气可用NaOH溶液吸收,主要反应为
的硝酸尾气可用NaOH溶液吸收,主要反应为
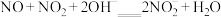
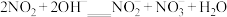
①下列措施能提高尾气中NO和NO2去除率的有___________ (填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是___________ (填化学式);吸收后排放的尾气中含量较高的氮氧化物是__________________ (填化学式)。
 、NO和
、NO和 等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。(1)
 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为(2)NO和
 的处理。已除去
的处理。已除去 的硝酸尾气可用NaOH溶液吸收,主要反应为
的硝酸尾气可用NaOH溶液吸收,主要反应为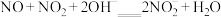
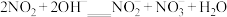
①下列措施能提高尾气中NO和NO2去除率的有
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到
 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是
您最近一年使用:0次
2020-10-03更新
|
1070次组卷
|
3卷引用:(苏教版2019)必修第二册专题7 氮与社会可持续发展 C 高考挑战区
4 . 已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使湿润红色石蕊试纸变蓝的气体,它们之间能发生如下反应:
①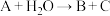 ;②
;② ;③
;③
(1)写出下列物质的化学式:C______ ,D______ ,E______ 。
(2)写出下列反应的离子方程式:①________ ;③________ 。
(3)工业生产C的过程中涉及一步反应,即F经催化氧化生成B和 。写出该步反应的化学方程式:
。写出该步反应的化学方程式:_____ 。
①
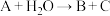 ;②
;② ;③
;③
(1)写出下列物质的化学式:C
(2)写出下列反应的离子方程式:①
(3)工业生产C的过程中涉及一步反应,即F经催化氧化生成B和
 。写出该步反应的化学方程式:
。写出该步反应的化学方程式:
您最近一年使用:0次
2020-10-03更新
|
424次组卷
|
5卷引用:5.2.2 氨与铵盐(练好题)(基础过关)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)
(已下线)5.2.2 氨与铵盐(练好题)(基础过关)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)必修第二册RJ第5章第二节 氮及其化合物 课时2 氨和铵盐安徽省滁州市定远县育才学校2020-2021学年高一下学期第一次月考化学试题7.3.1铵盐的性质(课后)-2019苏教版必修2课前课中课后山西省长治市第一中学校2021-2022学年高一下学期第一次阶段测试化学试题
5 .  、NO和
、NO和 等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(1) 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为_______________________________________ 。
(2)NO和 的处理。已除去
的处理。已除去 的硝酸尾气可用NaOH溶液吸收,主要反应为
的硝酸尾气可用NaOH溶液吸收,主要反应为
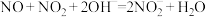
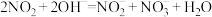
①下列措施能提高尾气中NO和 去除率的有
去除率的有____________ (填字母)。
A.加快通入尾气的速率B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是________________ (填化学式);吸收后排放的尾气中含量较高的氮氧化物是____________________ (填化学式)。
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。
在酸性NaClO溶液中,HClO氧化NO生成 和
和 ,其离子方程式为
,其离子方程式为____________________ 。
 、NO和
、NO和 等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。(1)
 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为(2)NO和
 的处理。已除去
的处理。已除去 的硝酸尾气可用NaOH溶液吸收,主要反应为
的硝酸尾气可用NaOH溶液吸收,主要反应为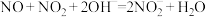
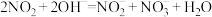
①下列措施能提高尾气中NO和
 去除率的有
去除率的有A.加快通入尾气的速率B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到
 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。
在酸性NaClO溶液中,HClO氧化NO生成
 和
和 ,其离子方程式为
,其离子方程式为
您最近一年使用:0次
2020-09-23更新
|
437次组卷
|
4卷引用:(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第二节 氮及其化合物
名校
解题方法
6 . SCR和NSR技术可有效降低柴油发动机在空气过量条件下的 排放。
排放。
(1)SCR(选择性催化还原)工作原理如图所示: 水溶液热分解为
水溶液热分解为 和
和 ,该反应的化学方程式;
,该反应的化学方程式;_____________________ 。
②反应器中 还原
还原 的化学方程式:
的化学方程式:_________________________________ 。
③当燃油中含硫量较高时,尾气中 在
在 作用下会形成
作用下会形成 ,使催化剂中毒。用化学方程式表示
,使催化剂中毒。用化学方程式表示 的形成:
的形成:___________________________________________________ 。
④尿素溶液浓度影响 的转化,测定溶液中尿素(
的转化,测定溶液中尿素(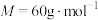 )含量的方法如下:取
)含量的方法如下:取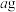 尿素溶液,将所含氮完全转化为
尿素溶液,将所含氮完全转化为 ,所得
,所得 用过量的
用过量的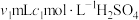 溶液吸收完全,剩余
溶液吸收完全,剩余 用
用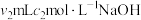 溶液恰好中和,则尿素溶液中溶质的质量分数是
溶液恰好中和,则尿素溶液中溶质的质量分数是_____________ 。
(2)NSR( 储存还原)工作原理:
储存还原)工作原理:
 的储存和还原在不同时段交替进行,如图所示。
的储存和还原在不同时段交替进行,如图所示。 的相互转化实现
的相互转化实现 的储存和还原。储存
的储存和还原。储存 的物质是
的物质是__________ 。
②用 模拟尾气中还原性气体研究了
模拟尾气中还原性气体研究了 的催化还原过程,该过程分两步进行,图表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的
的催化还原过程,该过程分两步进行,图表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的 与
与 的物质的量之比是
的物质的量之比是___________________ 。
 排放。
排放。(1)SCR(选择性催化还原)工作原理如图所示:
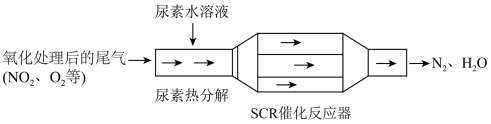
 水溶液热分解为
水溶液热分解为 和
和 ,该反应的化学方程式;
,该反应的化学方程式;②反应器中
 还原
还原 的化学方程式:
的化学方程式:③当燃油中含硫量较高时,尾气中
 在
在 作用下会形成
作用下会形成 ,使催化剂中毒。用化学方程式表示
,使催化剂中毒。用化学方程式表示 的形成:
的形成:④尿素溶液浓度影响
 的转化,测定溶液中尿素(
的转化,测定溶液中尿素(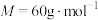 )含量的方法如下:取
)含量的方法如下:取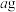 尿素溶液,将所含氮完全转化为
尿素溶液,将所含氮完全转化为 ,所得
,所得 用过量的
用过量的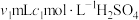 溶液吸收完全,剩余
溶液吸收完全,剩余 用
用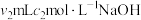 溶液恰好中和,则尿素溶液中溶质的质量分数是
溶液恰好中和,则尿素溶液中溶质的质量分数是(2)NSR(
 储存还原)工作原理:
储存还原)工作原理: 的储存和还原在不同时段交替进行,如图所示。
的储存和还原在不同时段交替进行,如图所示。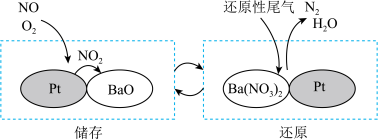
 的相互转化实现
的相互转化实现 的储存和还原。储存
的储存和还原。储存 的物质是
的物质是②用
 模拟尾气中还原性气体研究了
模拟尾气中还原性气体研究了 的催化还原过程,该过程分两步进行,图表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的
的催化还原过程,该过程分两步进行,图表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的 与
与 的物质的量之比是
的物质的量之比是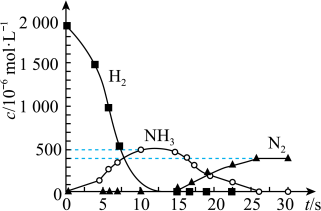
您最近一年使用:0次
2020-09-23更新
|
381次组卷
|
3卷引用:(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第二节 氮及其化合物
名校
解题方法
7 . 如图是某元素形成物质的“价—类”图,图中显示各物质之间的转化关系。其中A为正盐,X是一种强碱,通常条件下Z是无色液体,E的相对分子质量比D的大16。下列说法正确的是


| A.A是适合与草木灰混合施用的肥料 | B.C可用排空气法收集 |
| C.B和F能发生复分解反应生成盐 | D.B在一定条件下可直接与Y反应生成D |
您最近一年使用:0次
2020-09-23更新
|
511次组卷
|
4卷引用:(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第二节 氮及其化合物
(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第二节 氮及其化合物高一必修第一册(鲁科2019)第3章 第3节 氮的循环辽宁省沈阳市第一二〇中学2021-2022学年高三上学期第四次质量监测化学试题(已下线)小题必刷20 氮及其化合物——2021年高考化学一轮复习小题必刷(通用版)
解题方法
8 . 膨松剂是一种食品添加剂。它在面包制作过程中发生反应产生气体,使面包变得松软,膨松剂产生气体的量是检验膨松剂品质的一项重要指标。已知某膨松剂含碳酸氢钠、碳酸氢铵中的一种或两种,某化学兴趣小组对该膨松剂进行了探究。
探究Ⅰ:检验膨松剂的成分:在硬质玻璃管中加入该膨松剂,按如图所示连接好装置(装置气密性良好,且装置内空气已排尽)。
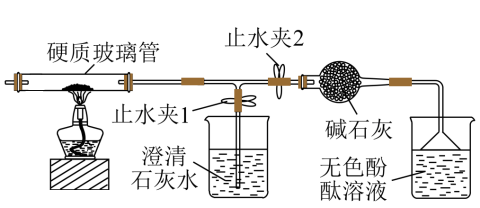
【观察与分析Ⅰ】点燃酒精灯。
(1)关闭止水夹2,打开止水夹1,澄清石灰水变浑浊,说明产物中有二氧化碳,该反应的化学方程式为_______ 。
(2)打开止水夹2,关闭止水夹1,观察到的现象是____ ,说明产物中有氨气。
(3)充分加热后,硬质玻璃管中_____ (填“有”或“无”)固体剩余。
【实验结论】该膨松剂是碳酸氢钠和碳酸氢铵的混合物。
探究Ⅱ:测定该膨松剂受热产生气体的质量:用如图所示装置测定该膨松剂样品产生的二氧化碳和氨气的质量(装置气密性良好,各装置中气体吸收剂足量)。
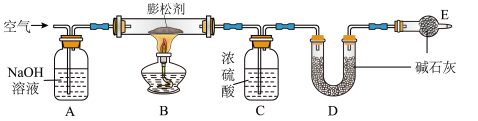
【观察与分析Ⅱ】(4)通过测定实验前后装置D的质量,其质量差即为样品产生二氧化碳的质量,装置C的作用是___ ,装置D的作用是______ ,若没有装置E,会造成测定结果______ (填“偏大”“不变”或“偏小”)。
(5)实验过程中必须向装置内通入空气,装置A的作用是除去空气中的______ (填名称)。停止加热后,继续通入空气一段时间,目的是______ 。
(6)若对装置C、D、E连接顺序进行调整,即可用于测定另一份同质量的相同样品受热分解产生的氨气的质量。则装置C、D、E连接顺序为________ ,通过测定实验前后装置C的质量,其质量差即为样品产生氨气的质量。
【拓展研究】(7)若将产生的氨气通过灼热的氧化铜会生成红色固体、无色液体和气体单质三种物质,则该反应的化学方程式为_____ 。
探究Ⅰ:检验膨松剂的成分:在硬质玻璃管中加入该膨松剂,按如图所示连接好装置(装置气密性良好,且装置内空气已排尽)。

【观察与分析Ⅰ】点燃酒精灯。
(1)关闭止水夹2,打开止水夹1,澄清石灰水变浑浊,说明产物中有二氧化碳,该反应的化学方程式为
(2)打开止水夹2,关闭止水夹1,观察到的现象是
(3)充分加热后,硬质玻璃管中
【实验结论】该膨松剂是碳酸氢钠和碳酸氢铵的混合物。
探究Ⅱ:测定该膨松剂受热产生气体的质量:用如图所示装置测定该膨松剂样品产生的二氧化碳和氨气的质量(装置气密性良好,各装置中气体吸收剂足量)。

【观察与分析Ⅱ】(4)通过测定实验前后装置D的质量,其质量差即为样品产生二氧化碳的质量,装置C的作用是
(5)实验过程中必须向装置内通入空气,装置A的作用是除去空气中的
(6)若对装置C、D、E连接顺序进行调整,即可用于测定另一份同质量的相同样品受热分解产生的氨气的质量。则装置C、D、E连接顺序为
【拓展研究】(7)若将产生的氨气通过灼热的氧化铜会生成红色固体、无色液体和气体单质三种物质,则该反应的化学方程式为
您最近一年使用:0次
解题方法
9 . 某化学课外活动小组设计实验探究氨的催化氧化。检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯。部分实验现象如下:C处铂丝继续保持红热,F处铜片逐渐溶解。

(1)装置A中使用的药品是NH4HCO3固体,则A需要的仪器有试管、导管橡胶塞和__ (填选项序号)。
a.锥形瓶 b.酒精灯 c.烧瓶 d.蒸发皿
(2)装置B的作用是___ 。
(3)装置C中发生反应的化学方程式为__ 。
(4)该装置存在的主要缺陷是__ 。
(5)如图所示的E装置可防止F中溶液倒吸进入D中,请在图中画出装置E中的导气管。___
(6)若进入F装置的物质成分和质量一定,可向F中加入下列物质中的__ (填字母)使铜片溶解的质量增多。
A.Na2CO3 B.NaCl C.CuSO4 D.H2SO4
(7)乙小组认为可将甲小组的装置中A、B部分换成如图2所示装置(其余部分相同)进行实验。烧瓶中加入的是过氧化钠固体,则分液漏斗中加入的最佳试剂是__ ,U形管中加入的试剂是__ 。

(1)装置A中使用的药品是NH4HCO3固体,则A需要的仪器有试管、导管橡胶塞和
a.锥形瓶 b.酒精灯 c.烧瓶 d.蒸发皿
(2)装置B的作用是
(3)装置C中发生反应的化学方程式为
(4)该装置存在的主要缺陷是
(5)如图所示的E装置可防止F中溶液倒吸进入D中,请在图中画出装置E中的导气管。
(6)若进入F装置的物质成分和质量一定,可向F中加入下列物质中的
A.Na2CO3 B.NaCl C.CuSO4 D.H2SO4
(7)乙小组认为可将甲小组的装置中A、B部分换成如图2所示装置(其余部分相同)进行实验。烧瓶中加入的是过氧化钠固体,则分液漏斗中加入的最佳试剂是
您最近一年使用:0次
2020-08-21更新
|
486次组卷
|
4卷引用:(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第二节 氮及其化合物
名校
解题方法
10 . 关于氮的变化关系图如下:
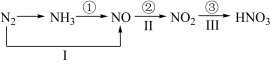
则下列说法不正确的是( )

则下列说法不正确的是( )
| A.路线①②③是工业生产硝酸的主要途径 |
| B.路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径 |
| C.氮气可在足量的氧气中通过一步反应生成NO2 |
| D.上述所有反应都是氧化还原反应 |
您最近一年使用:0次
2020-06-11更新
|
873次组卷
|
13卷引用:5.2.3 硝酸(练好题)(基础过关)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)
(已下线)5.2.3 硝酸(练好题)(基础过关)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)湖南省常德市芷兰实验中学2020-2021学年高一下学期第一次月考化学试题山东省淄博市高青县第一中学2020-2021学年高二下学期第一次月考化学试题江苏省沭阳县2020-2021学年高一下学期中调研测试化学试题江苏省盐城市滨海县五汛中学2021-2022学年高一上学期期中考试化学试题陕西省宝鸡市渭滨区2019—2020学年高一上学期期末考试化学试题安徽省滁州市明光中学2019-2020学年高一下学期开学考试化学试题陕西省延安市第一中学2019-2020学年高一下学期线上摸底考试化学试题内蒙古自治区呼和浩特市土默特左旗第一中学2019-2020学年高一下学期期末考试化学试题西藏自治区拉萨市那曲第二高级中学2019-2020学年高一下学期期末考试化学试题专题7 本专题达标检测-高中化学必修第二册苏教版2019北京市平谷区第五中学2019-2020学年高一下学期3月月考化学试题广西三新2021-2022学年高一下学期教学质量测评4月段考化学试题



