1 . 氨气遇到氯气会产生白烟。氯碱工业中用氨气检验氯气管道是否泄漏。
(1)已知白烟成分是氯化铵,反应还生成一种无毒的气态单质。试写出反应的化学方程式:_________ 。
(2)在反应中,每生成1mol氯化铵,有_________ mol氯气被还原,_________ mol氨气被氧化,发生反应的氨气是_________ mol。
(1)已知白烟成分是氯化铵,反应还生成一种无毒的气态单质。试写出反应的化学方程式:
(2)在反应中,每生成1mol氯化铵,有
您最近一年使用:0次
2 . 工业上硝酸的制备和自然界中硝酸的生成既有相同的地方,又有区别。线路①②③是工业生产硝酸的主要途径,线路I、II、III是雷电固氮过程中硝酸的产生途径。
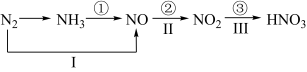
(1)写出各变化的化学方程式,如果属于氧化还原反应,指出其中的氧化剂和还原剂____ 、____ 、____ 、____ 、____ 。
(2)硝酸生产过程中排放出来的一氧化氮是大气污染物之一。目前有一种治理方法,是在400℃左右且有催化剂存在的条件下,用氨把一氧化氮还原成可直接排入大气的无色无毒气体。请写出有关反应的化学方程式____ 。

(1)写出各变化的化学方程式,如果属于氧化还原反应,指出其中的氧化剂和还原剂
(2)硝酸生产过程中排放出来的一氧化氮是大气污染物之一。目前有一种治理方法,是在400℃左右且有催化剂存在的条件下,用氨把一氧化氮还原成可直接排入大气的无色无毒气体。请写出有关反应的化学方程式
您最近一年使用:0次
名校
解题方法
3 . 甲、乙两个研究性学习小组为测定氨分子中氮、氢原子个数比,设计了如下实验流程:

实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜。反应完成后,黑色的氧化铜转化为红色的铜。反应方程式:2NH3+3CuO N2+3Cu+3H2O。下图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。
N2+3Cu+3H2O。下图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。

甲小组测得:反应前氧化铜的质量为m1 g、氧化铜反应后剩余固体的质量为m2 g、生成的氮气在标准状况下的体积为V1 L。
乙小组测得:洗气前装置D的质量为m3 g、洗气后装置D的质量为m4 g、生成的氮气在标准状况下的体积为V2 L。
请回答下列问题:
(1)写出仪器a的名称:_______ 。
(2)检查装置A气密性的操作是_______ 。
(3)甲、乙两小组选择了不同的方法制取氨气,请将实验装置的字母编号和制备原理填写在下表的空格中:
(4)甲小组用所测数据计算出氨分子中氮、氢的原子个数之比为_______ 。
(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数比明显小于理论值,其原因是_______ 。为此,乙小组在原有实验的基础上增加了一个装有某药品的实验仪器,重新实验。根据实验前后该药品的质量变化及生成氮气的体积,得出了合理的实验结果。该药品的名称是_______ 。

实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜。反应完成后,黑色的氧化铜转化为红色的铜。反应方程式:2NH3+3CuO
 N2+3Cu+3H2O。下图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。
N2+3Cu+3H2O。下图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。
甲小组测得:反应前氧化铜的质量为m1 g、氧化铜反应后剩余固体的质量为m2 g、生成的氮气在标准状况下的体积为V1 L。
乙小组测得:洗气前装置D的质量为m3 g、洗气后装置D的质量为m4 g、生成的氮气在标准状况下的体积为V2 L。
请回答下列问题:
(1)写出仪器a的名称:
(2)检查装置A气密性的操作是
(3)甲、乙两小组选择了不同的方法制取氨气,请将实验装置的字母编号和制备原理填写在下表的空格中:
| 实验装置 | 实验药品 | 制备原理 | |
| 甲小组 | A | 氢氧化钙、氯化铵 | 反应的化学方程式: |
| 乙小组 | 浓氨水、氢氧化钠 | 氢氧化钠溶于水会放热,且使溶液碱性增强,促进氨气逸出 |
(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数比明显小于理论值,其原因是
您最近一年使用:0次
2022-03-24更新
|
351次组卷
|
4卷引用:人教版2019必修第二册 第五章 本章达标检测
4 . 在下图所示的物质转化关系中,A是常见的气态氢化物,B是能使带火星的木条复燃的无色、无味气体,E的相对分子质量比D的大17,G是一种紫红色金属单质(反应条件和部分生成物未列出)。
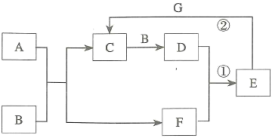
(1)A的电子式为___________ ,B的化学式为___________ 。
(2)请写出:
反应①的化学方程式_________
反应②的离子方程式____________ 。

(1)A的电子式为
(2)请写出:
反应①的化学方程式
反应②的离子方程式
您最近一年使用:0次
2021-12-02更新
|
1112次组卷
|
2卷引用:人教2019版必修第二册第五章 化工生产中的重要非金属元素复习与提高
21-22高一上·浙江绍兴·期中
名校
5 . 下列物质的转化在给定条件下能实现的是
A.Fe 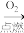 Fe2O3 Fe2O3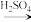 Fe2(SO4)3 Fe2(SO4)3 | B.S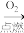 SO3 SO3 H2SO4 H2SO4 |
C.SO2 H2SO3 H2SO3 H2SO4 H2SO4 | D.NH3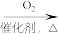 NO NO HNO3 HNO3 |
您最近一年使用:0次
2021-11-23更新
|
456次组卷
|
3卷引用:第三章 单元检测-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)
(已下线)第三章 单元检测-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)浙江省绍兴市诸暨中学2021-2022学年高一上学期期中考试(实验班)化学试题浙江省瑞安市瑞祥高级中学2022-2023学年高一上学期期末考试化学试题
21-22高三上·河南郑州·期中
名校
解题方法
6 . 在给定条件下,下列选项正确的是
①NaHCO3 Na2CO3
Na2CO3 NaOH
NaOH
②CaCO3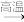 CaO
CaO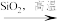 CaSiO3
CaSiO3
③NH3 NO
NO  HNO3
HNO3
④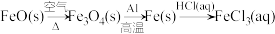
⑤S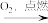 SO3
SO3 H2SO4
H2SO4
⑥
①NaHCO3
 Na2CO3
Na2CO3 NaOH
NaOH ②CaCO3
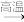 CaO
CaO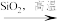 CaSiO3
CaSiO3③NH3
 NO
NO  HNO3
HNO3④
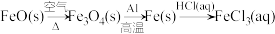
⑤S
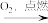 SO3
SO3 H2SO4
H2SO4 ⑥

| A.有2项能实现 | B.有3项能实现 |
| C.有4项能实现 | D.以上转化均不能实现 |
您最近一年使用:0次
2021-11-22更新
|
476次组卷
|
3卷引用:3.3 氮的循环-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)
(已下线)3.3 氮的循环-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)河南省实验中学2021-2022学年高三上学期期中考试化学试题江西省南昌市第二中学2022-2023学年高三上学期第四次考试化学试题
21-22高三上·辽宁·期中
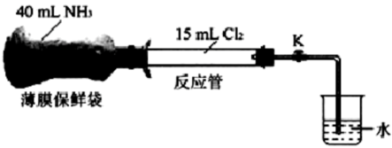
7 . 某实验小组探究氨气与氯气的反应,装置如图所示,在常温常压下将氨气收集在薄膜保鲜袋(无弹性)中,氯气收集在反应管中,关闭K。如图连接好装置,将氨气压入反应管,充分反应后打开K,下列说法不正确的是

| A.该反应原理可应用于检验输送氯气的管道是否泄漏 |
| B.反应开始后,薄膜保鲜袋逐渐被吸入反应管中 |
| C.打开K后,烧杯内的水会倒吸入反应管 |
| D.反应过程中,反应管内气体颜色逐渐变浅,有白烟生成 |
您最近一年使用:0次
解题方法
8 . 下列关于氨气的说法正确的是

| A.氨气不能用浓硫酸干燥 |
B.氨的催化氧化是工业制硝酸的基础,化学方程式为4NH3+7O2 4NO2+6H2O 4NO2+6H2O |
| C.NH3是电解质,所以氨水能导电 |
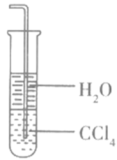
| D.可用如图所示的装置吸收NH3,且可以防止倒吸(NH3不溶于CCl4) |
您最近一年使用:0次
解题方法
9 . 农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用图1所示装置制备氨气并探究其相关性质。


(1)装置A中,盛有浓氨水的仪器名称为_______ 。烧瓶内药品可选用_______ 。装置B的作用是_______ 。
(2)连接好装置并检验装置的气密性后,装入药品,然后应先_______ (填“a”或“b”)。
a.逐滴向圆底烧瓶中加入氨水
b.加热装置C
(3)实验中观察到C中 粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应的化学方程式为
粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应的化学方程式为_______ ,该反应证明氨气具有_______ 性。
(4)该实验缺少尾气吸收装置,图2中能用来吸收尾气的装置是_______ (填序号)。


(1)装置A中,盛有浓氨水的仪器名称为
(2)连接好装置并检验装置的气密性后,装入药品,然后应先
a.逐滴向圆底烧瓶中加入氨水
b.加热装置C
(3)实验中观察到C中
 粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应的化学方程式为
粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应的化学方程式为(4)该实验缺少尾气吸收装置,图2中能用来吸收尾气的装置是
您最近一年使用:0次
20-21高一下·全国·课时练习
解题方法
10 . 某课外活动小组在实验室用下图所示装置快速制取氨并验证氨的某些性质,同时收集少量纯净的氮气,请回答。

(1)写出用生石灰和浓氨水反应制氨的化学方程式_______ ,解释放出NH3的原因_______ 。
(2)实验进行一段时间,观察到硬质玻璃管内黑色氧化铜粉末变为红色,盛无水硫酸铜的干燥管内出现蓝色,并且在最后的出气导管口处收集到纯净、干燥的氮气。根据这些现象,写出在硬质玻璃管内发生反应的化学方程式:_______ ,这个反应说明氨具有_______ 。
A.碱性 B.还原性 C.氧化性 D.不稳定性
(3)洗气瓶中浓硫酸的主要作用是_______ 。
(4)在最后的出气导管口处收集干燥、纯净的氮气,收集方法是_______ 。
A.排空气法 B.排水法 C.用气囊收集
(5)装置E的作用是_______ ,装置F的作用_______ 。E中的碱石灰_______ (填“能”或“不能”)换成CaCl2。

(1)写出用生石灰和浓氨水反应制氨的化学方程式
(2)实验进行一段时间,观察到硬质玻璃管内黑色氧化铜粉末变为红色,盛无水硫酸铜的干燥管内出现蓝色,并且在最后的出气导管口处收集到纯净、干燥的氮气。根据这些现象,写出在硬质玻璃管内发生反应的化学方程式:
A.碱性 B.还原性 C.氧化性 D.不稳定性
(3)洗气瓶中浓硫酸的主要作用是
(4)在最后的出气导管口处收集干燥、纯净的氮气,收集方法是
A.排空气法 B.排水法 C.用气囊收集
(5)装置E的作用是
您最近一年使用:0次



