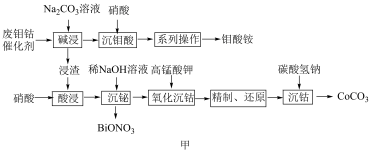
1 . 一种从废钼钴催化剂中回收有价金属的工艺流程如图甲所示:
已知:I.废钼钴催化剂的主要成分如表。
II.“酸浸”所得溶液中主要含有H+、Bi3+、Co2+等阳离子。
回答下列问题:
(1)钼酸铵 中Mo元素的化合价为
中Mo元素的化合价为_______ ,其所含非金属元素的电负性由大到小排序为_______ 。
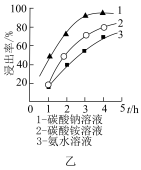
(2)“碱浸”时需在75℃条件下进行反应,且选择不同碱性试剂钼元素的浸出率随时间变化如图乙所示。则“碱浸”时的最佳条件为_______ 。
(3)“沉钼酸”时,一般控制反应温度为60℃,温度不宜太高的原因为_______ 。
(4)“沉铋”时,反应的离子方程式为_______ 。
(5)“氧化沉钴”时调节溶液 ,反应生成
,反应生成 和
和 ,其离子方程式为
,其离子方程式为_______ 。
(6)若通过该流程处理1kg废钼钴催化剂,得到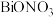 的质量为0.1435kg,则Bi元素的回收率最接近
的质量为0.1435kg,则Bi元素的回收率最接近_____ (填标号)(Bi元素的回收率 )。
)。
A.70% B.80% C.90%

已知:I.废钼钴催化剂的主要成分如表。
| 主要成分 |  |  |  |
| 质量分数 | 44.61% | 6.67% | 13.98% |
回答下列问题:
(1)钼酸铵
 中Mo元素的化合价为
中Mo元素的化合价为(2)“碱浸”时需在75℃条件下进行反应,且选择不同碱性试剂钼元素的浸出率随时间变化如图乙所示。则“碱浸”时的最佳条件为

(3)“沉钼酸”时,一般控制反应温度为60℃,温度不宜太高的原因为
(4)“沉铋”时,反应的离子方程式为
(5)“氧化沉钴”时调节溶液
 ,反应生成
,反应生成 和
和 ,其离子方程式为
,其离子方程式为(6)若通过该流程处理1kg废钼钴催化剂,得到
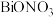 的质量为0.1435kg,则Bi元素的回收率最接近
的质量为0.1435kg,则Bi元素的回收率最接近 )。
)。A.70% B.80% C.90%
您最近一年使用:0次
2 . NA为阿伏伽德罗常数的值,下列说法错误的是
| A.1LpH=1的H2SO4溶液中H+的数目为0.1NA |
B.常温常压下,1个CO2分子的体积大于 |
C.浓硝酸热分解生成NO2、N2O4共23g时,转移电子数为 |
D.0.1molNH3溶于水得到的溶液中,NH3·H2O和 的总数小于 的总数小于 |
您最近一年使用:0次
名校
解题方法
3 . 某学习小组想通过研究NO2性质,提出减少汽车尾气NO2含量的同时,降低汽车排气管中积碳的实验方案。回答下列问题:
(1)通过浓硝酸分解分析NO2能否支持燃烧:如图所示,向试管中加入浓硝酸,加热至沸腾,向试管中伸入燃烧的木条,木条熄灭。

①写出浓硝酸受热分解的化学方程式:_____ 。
②甲同学根据实验现象得出NO2不支持燃烧,不能与红热的碳反应的结论,乙同学不同意该结论,理由可能是_____ 。
③除了原理上的不合理,从环保角度考虑,该实验还有一个明显不足之处是_____ 。
(2)查阅资料发现Cu(NO3)2受热时发生反应:2Cu(NO3)2 2CuO+4NO2↑+O2↑。收集硝酸铜分解后的气体,发现该气体能使带火星的木条复燃,但空气(空气中O2的体积分数约为
2CuO+4NO2↑+O2↑。收集硝酸铜分解后的气体,发现该气体能使带火星的木条复燃,但空气(空气中O2的体积分数约为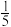 )不能使带火星的木条复燃。
)不能使带火星的木条复燃。
①结论:NO2能与碳反应,支持燃烧,理由是_____ 。
②经检验,加热时碳与NO2反应的两种产物均为空气成分,写出该反应的化学方程式:______ 。
(3)设计NO2与碳反应的条件控制实验:初始温度为280℃(汽车尾气的大致温度),其它初始条件也完全相同,分别在体积相同的绝热恒容密闭容器A和恒温恒容密闭容器B中加入等量的焦炭和NO2气体。
①反应达到平衡时,平衡转化率较高的是容器_____ (填“A”或“B”)。
②请写出工农业生产中NO2的一种用途:_____ 。
(1)通过浓硝酸分解分析NO2能否支持燃烧:如图所示,向试管中加入浓硝酸,加热至沸腾,向试管中伸入燃烧的木条,木条熄灭。

①写出浓硝酸受热分解的化学方程式:
②甲同学根据实验现象得出NO2不支持燃烧,不能与红热的碳反应的结论,乙同学不同意该结论,理由可能是
③除了原理上的不合理,从环保角度考虑,该实验还有一个明显不足之处是
(2)查阅资料发现Cu(NO3)2受热时发生反应:2Cu(NO3)2
 2CuO+4NO2↑+O2↑。收集硝酸铜分解后的气体,发现该气体能使带火星的木条复燃,但空气(空气中O2的体积分数约为
2CuO+4NO2↑+O2↑。收集硝酸铜分解后的气体,发现该气体能使带火星的木条复燃,但空气(空气中O2的体积分数约为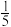 )不能使带火星的木条复燃。
)不能使带火星的木条复燃。①结论:NO2能与碳反应,支持燃烧,理由是
②经检验,加热时碳与NO2反应的两种产物均为空气成分,写出该反应的化学方程式:
(3)设计NO2与碳反应的条件控制实验:初始温度为280℃(汽车尾气的大致温度),其它初始条件也完全相同,分别在体积相同的绝热恒容密闭容器A和恒温恒容密闭容器B中加入等量的焦炭和NO2气体。
①反应达到平衡时,平衡转化率较高的是容器
②请写出工农业生产中NO2的一种用途:
您最近一年使用:0次
2022-12-17更新
|
109次组卷
|
2卷引用:四川省泸县第五中学2022-2023学年高二上学期期末考试化学试题
名校
解题方法
4 . 某化学小组为探究浓HNO3和NaCl固体的反应产物,进行实验:
实验I
资料:
①向AgNO3的95%的乙醇溶液中通入HCl产生白色沉淀,通入Cl2无此现象。
②王水中因含有NOCl呈橙色。NOCl(N元素为+3价)有刺鼻恶臭味,受热易分解为NO和Cl2。
(1)浓HNO3需保存在棕色试剂瓶中,用化学方程式表示原因:_______ 。
(2)探究注射器1中浅棕色气体的成分。甲同学用注射器2抽取注射器1中的浅棕色气体,然后吸取适量蒸馏水并振荡,气体颜色褪去,吸入氧气后又变为浅棕色。经检验,浅棕色气体中几乎不含NOCl。
①甲同学根据实验现象推断浅棕色气体中含有NO2,结合氧化还原反应规律分析一定还含有Cl2,用离子方程式表示甲同学的依据:_______ 。
②乙同学认为需设计实验证明存在Cl2.请结合资料,设计证实存在Cl2的实验方案:_______ 。
(3)探究注射器1内橙色溶液的成分。
实验II:取2mL橙色溶液于试管中,加热一段时间,观察到试管内有红棕色气体生成,溶液变为无色。接着向溶液中滴加AgNO3溶液,无明显现象。
①丙同学认为实验II中“接着向溶液中滴加AgNO3溶液,无明显现象”,是因为加热使溶液中的Cl-全部变为HCl气体放出。请设计实验证明丙同学的观点不成立:_______ 。
②丁同学通过与王水类比,并查阅资料,确认产生实验II中的现象的原因是:浓HNO3与NaCl固体反应生成了NOCl,继而溶液中的NOCl受热发生分解反应,使溶液中的Cl-反应完全,所以向溶液中滴加AgNO3溶液时无明显现象。浓HNO3与NaCl固体反应生成了NOCl,化学方程式是_______ 。
(4)综合上述实验,可以得出结论:_______ 。
实验I
| 实验装置 | 实验步骤及现象 |
| 室温下,按图连接实验装置并检查气密性。向注射器1中先加入1.17gNaCl固体,然后吸入5mL浓HNO3,关闭止水夹。一段时间后,注射器内溶液变为橙色,液面上方有浅棕色刺激性气味气体,溶液温度无明显变化。 |
①向AgNO3的95%的乙醇溶液中通入HCl产生白色沉淀,通入Cl2无此现象。
②王水中因含有NOCl呈橙色。NOCl(N元素为+3价)有刺鼻恶臭味,受热易分解为NO和Cl2。
(1)浓HNO3需保存在棕色试剂瓶中,用化学方程式表示原因:
(2)探究注射器1中浅棕色气体的成分。甲同学用注射器2抽取注射器1中的浅棕色气体,然后吸取适量蒸馏水并振荡,气体颜色褪去,吸入氧气后又变为浅棕色。经检验,浅棕色气体中几乎不含NOCl。
①甲同学根据实验现象推断浅棕色气体中含有NO2,结合氧化还原反应规律分析一定还含有Cl2,用离子方程式表示甲同学的依据:
②乙同学认为需设计实验证明存在Cl2.请结合资料,设计证实存在Cl2的实验方案:
(3)探究注射器1内橙色溶液的成分。
实验II:取2mL橙色溶液于试管中,加热一段时间,观察到试管内有红棕色气体生成,溶液变为无色。接着向溶液中滴加AgNO3溶液,无明显现象。
①丙同学认为实验II中“接着向溶液中滴加AgNO3溶液,无明显现象”,是因为加热使溶液中的Cl-全部变为HCl气体放出。请设计实验证明丙同学的观点不成立:
②丁同学通过与王水类比,并查阅资料,确认产生实验II中的现象的原因是:浓HNO3与NaCl固体反应生成了NOCl,继而溶液中的NOCl受热发生分解反应,使溶液中的Cl-反应完全,所以向溶液中滴加AgNO3溶液时无明显现象。浓HNO3与NaCl固体反应生成了NOCl,化学方程式是
(4)综合上述实验,可以得出结论:
您最近一年使用:0次
2022-07-10更新
|
431次组卷
|
4卷引用:北京市西城区2021-2022学年高一下学期期末化学试题
北京市西城区2021-2022学年高一下学期期末化学试题(已下线)重难点04 硫和氮综合题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)北京市西城外国语学校2022-2023学年高一下学期期中考试化学试题北京市育才学校2023-2024学年高一下学期期中考试化学(选考)试题
5 . 下列说法正确的是( )
| A.向新制氯水中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
| B.浓硝酸在光照下颜色变黄,说明浓硝酸不稳定 |
| C.铁与水蒸气在高温下的反应产物为Fe2O3和H2 |
| D.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有吸水性 |
您最近一年使用:0次
2020-01-11更新
|
851次组卷
|
4卷引用:宁夏回族自治区石嘴山市第三中学2019-2020学年高一上学期期末考试化学试题
6 . 下列关于浓硝酸的说法不正确的是
| A.光照易分解 |
| B.露置于空气中溶液浓度降低 |
| C.能与碳反应说明其具有强氧化性 |
| D.常温下铜在浓硝酸中发生钝化 |
您最近一年使用:0次
2018-05-07更新
|
328次组卷
|
5卷引用:云南省中央民大附中芒市国际学校2017-2018学年高一下学期期末考试化学试题
云南省中央民大附中芒市国际学校2017-2018学年高一下学期期末考试化学试题【全国百强校】江苏省清江中学2017-2018学年高一下学期期中考试化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高一下学期4月月考化学试题江苏省淮阴市师范学院附属中学2018-2019学年高一下学期期中考试化学试题(已下线)3.3.3 硝酸的性质 人类活动对氮循环和环境的影响练习(2)——《高中新教材同步备课》(鲁科版 必修第一册)
7 . 下列对有关实验描述和解释正确的是
| A.SO2气体通入酸性高锰酸钾溶液中,使高锰酸钾褪色说明SO2有漂白性 |
| B.浓硝酸在光照条件下变黄,说明浓硝酸易分解生成有色产物且溶于浓硝酸 |
| C.常温下,将铝、铁片放入浓硫酸、浓硝酸中,无明显现象,说明铝、铁不与冷的浓硫酸、浓硝酸反应 |
| D.向CuSO4溶液中加入一小块金属钠,则钠与Cu2+反应可置换出铜 |
您最近一年使用:0次
2017-03-01更新
|
748次组卷
|
3卷引用:2016-2017学年安徽省安庆市高一上学期期末考试化学试卷




