名校
1 . 下列反应在指定条件下能实现的是
A.HClO HCl HCl | B.Fe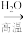 Fe2O3 Fe2O3 |
C.S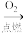 SO3 SO3 | D.S Fe2S3 Fe2S3 |
您最近一年使用:0次
名校
2 . 设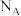 为阿伏加德罗常数的值,下列说法中
为阿伏加德罗常数的值,下列说法中不正确 的是
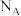 为阿伏加德罗常数的值,下列说法中
为阿伏加德罗常数的值,下列说法中A.25℃,101kPa时,22.4L 中含有的原子数小于 中含有的原子数小于 |
B.1molCu与足量的硫黄反应,转移电子数为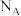 |
C.4.6g分子式为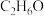 的有机物中含有 的有机物中含有 键数一定为 键数一定为 |
D.在标准状况下,20mL 和60mL 和60mL 所含分子个数比为1∶3 所含分子个数比为1∶3 |
您最近一年使用:0次
解题方法
3 . 不能通过两种单质直接化合得到的化合物是
A. | B. | C. | D. |
您最近一年使用:0次
名校
4 . 下列关于硫及其化合物的叙述,正确的是
| A.SO2能使酸性KMnO4溶液褪色,说明SO2有漂白性 |
| B.浓硫酸能与木炭在加热时反应,说明浓硫酸有强氧化性 |
| C.硫与铜在加热时反应生成硫化铜,说明硫有还原性 |
| D.葡萄酒中添加二氧化硫,说明二氧化硫可以在食品中大量使用 |
您最近一年使用:0次
名校
解题方法
5 . 下列事实可以用同一原理解释的是
| A.SO2、Cl2均能使品红溶液褪色 | B.S与铁、铜反应均生成低价态硫化物 |
| C.NH4HCO3晶体、碘固体受热均能变成气体 | D.ClO-与S2-、H+在溶液中均不能大量共存 |
您最近一年使用:0次
名校
6 . 元素周期表是化学史上重要的里程碑之一,下表是现行长式周期表的一部分。结合下表用化学用语回答问题:
(1)上表元素①~⑦中,非金属性最强的是___________ 。
(2)元素⑦为铁元素,其在周期表中的位置为___________ ,写出其单质与⑤的单质反应的化学方程式___________ 。
(3)可以用元素③的氢化物的水溶液溶蚀玻璃生产磨砂玻璃,写出反应的化学方程式___________ 。
(4)元素②④⑥简单离子半径由大到小为___________ 。
(5)元素④与元素①形成化合物X,写出X的电子式___________ ,其化学键类型为___________ ,X在野外能做生氢剂,其与水反应生氢的反应中,氧化剂为___________ 。
| ① | |||||||||||||||||
| ② | ③ | ||||||||||||||||
| ④ | ⑤ | ||||||||||||||||
| ⑥ | ⑦ | ||||||||||||||||
(2)元素⑦为铁元素,其在周期表中的位置为
(3)可以用元素③的氢化物的水溶液溶蚀玻璃生产磨砂玻璃,写出反应的化学方程式
(4)元素②④⑥简单离子半径由大到小为
(5)元素④与元素①形成化合物X,写出X的电子式
您最近一年使用:0次
名校
7 .  为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是| A.在100g98%的浓硫酸中含氧原子个数等于4NA |
| B.标准状况下,2.24L正庚烷完全燃烧,生成0.7molCO2和0.8mol水 |
| C.50mL、18mol/L浓硫酸与足量铜粉共热充分反应,生成SO2分子的数目为0.45NA |
D. 和 和 充分反应转移电子数为0.2NA 充分反应转移电子数为0.2NA |
您最近一年使用:0次
2024-05-03更新
|
406次组卷
|
2卷引用:海南省海口市海南中学2023-2024学年高一下学期4月期中考试化学试题
8 . 下列有关硫及其化合物的说法错误的是
| A.浓硫酸用作干燥剂利用了其脱水性 | B.常温下,浓硫酸可以用铁制容器盛放 |
| C.硫黄可以用于处理破碎的水银温度计 | D.浓硫酸和铜的反应体现酸性和氧化性 |
您最近一年使用:0次
名校
9 . NA代表阿伏加德罗常数的值,下列说法中正确的是
| A.100g34%的过氧化氢溶液中含有的极性键为2NA |
| B.标准状况下,44.8LNO和22.4LO2反应后的分子数为2NA |
C.18g 中含有的电子数目为9NA 中含有的电子数目为9NA |
| D.64g铜与足量的硫单质反应转移的电子数为2NA |
您最近一年使用:0次
10 . 设 为阿伏伽德罗常数的值,则下列说法正确的是
为阿伏伽德罗常数的值,则下列说法正确的是
 为阿伏伽德罗常数的值,则下列说法正确的是
为阿伏伽德罗常数的值,则下列说法正确的是A.常温常压下, 的体积为 的体积为 |
B.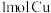 与足量的S充分反应,转移的电子数为 与足量的S充分反应,转移的电子数为 |
C. 与含 与含 的浓硫酸在加热的条件下反应时,生成的 的浓硫酸在加热的条件下反应时,生成的 在标准状况下的体积为 在标准状况下的体积为 |
D.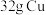 与足量浓 与足量浓 反应时,转移的电子数为 反应时,转移的电子数为 |
您最近一年使用:0次



