1 . 二氧化硫具有漂白性,工业上常用二氧化硫来漂白纸浆、毛、丝、草帽等。此外二氧化硫还能够抑制霉菌和细菌的滋生,可用作防腐剂。
Ⅰ.甲组同学拟利用 粉与浓硫酸反应制取
粉与浓硫酸反应制取 (标准状况下)
(标准状况下) 。实验方案设计如下:取
。实验方案设计如下:取 粉与
粉与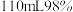 的浓硫酸(含
的浓硫酸(含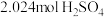 )混合,加热充分反应,待
)混合,加热充分反应,待 粉全部溶解后,干燥并收集气体。
粉全部溶解后,干燥并收集气体。
(1)写出 粉与浓硫酸反应制备
粉与浓硫酸反应制备 的化学方程式:
的化学方程式:__________________ 。
(2)乙组同学认为:按甲组同学实验方案无法达到实验目的,并且制得气体应该含有杂质,该杂质为_________ (填化学式)。
(3)为了检验甲组同学所制气体的成分,乙组同学按甲组同学的实验方案制备气体,并设计了如图所示的实验装置进行检验。(已知酸性高锰酸钾溶液及B中试剂均过量)
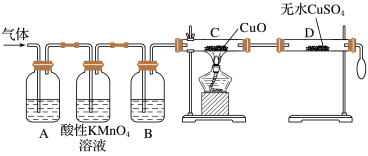
①A中试剂是品红溶液,作用是____________ 。
②B中所装试剂为____________ 。
③证明气体中混有杂质气体的实验现象是:________ 。
Ⅱ. 是常见的大气污染物,燃煤是产生
是常见的大气污染物,燃煤是产生 的主要原因。
的主要原因。
(4)工业上有多种方法可以减少 的排放。往煤中添加一些石灰石,可使燃煤过程中产生的
的排放。往煤中添加一些石灰石,可使燃煤过程中产生的 转化成硫酸钙,该反应的化学方程式是
转化成硫酸钙,该反应的化学方程式是___________ 。
(5)丙组同学认为 溶液可以做
溶液可以做 的吸收液,从而减少实验室
的吸收液,从而减少实验室 的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
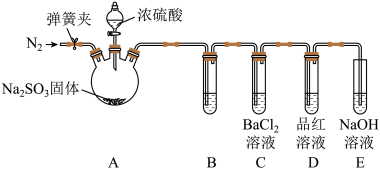
已知: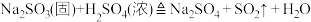
反应开始后,B、C试管中除了有气泡外,未见其他现象;D中红色褪去。通过乙组同学的实验,得出的结论是___________ 。
Ⅰ.甲组同学拟利用
 粉与浓硫酸反应制取
粉与浓硫酸反应制取 (标准状况下)
(标准状况下) 。实验方案设计如下:取
。实验方案设计如下:取 粉与
粉与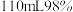 的浓硫酸(含
的浓硫酸(含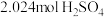 )混合,加热充分反应,待
)混合,加热充分反应,待 粉全部溶解后,干燥并收集气体。
粉全部溶解后,干燥并收集气体。(1)写出
 粉与浓硫酸反应制备
粉与浓硫酸反应制备 的化学方程式:
的化学方程式:(2)乙组同学认为:按甲组同学实验方案无法达到实验目的,并且制得气体应该含有杂质,该杂质为
(3)为了检验甲组同学所制气体的成分,乙组同学按甲组同学的实验方案制备气体,并设计了如图所示的实验装置进行检验。(已知酸性高锰酸钾溶液及B中试剂均过量)

①A中试剂是品红溶液,作用是
②B中所装试剂为
③证明气体中混有杂质气体的实验现象是:
Ⅱ.
 是常见的大气污染物,燃煤是产生
是常见的大气污染物,燃煤是产生 的主要原因。
的主要原因。(4)工业上有多种方法可以减少
 的排放。往煤中添加一些石灰石,可使燃煤过程中产生的
的排放。往煤中添加一些石灰石,可使燃煤过程中产生的 转化成硫酸钙,该反应的化学方程式是
转化成硫酸钙,该反应的化学方程式是(5)丙组同学认为
 溶液可以做
溶液可以做 的吸收液,从而减少实验室
的吸收液,从而减少实验室 的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
已知:
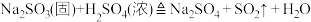
反应开始后,B、C试管中除了有气泡外,未见其他现象;D中红色褪去。通过乙组同学的实验,得出的结论是
您最近一年使用:0次
名校
解题方法
2 . 有关下列实验装置能达到实验目的的是




A.甲装置:0.1000mol/L的标准 溶液滴定未知浓度 溶液滴定未知浓度 溶液 溶液 |
B.乙装置:启停自如地制备 |
| C.丙装置:观察钾元素的焰色 |
D.丁装置:检验 中是否混有 中是否混有 |
您最近一年使用:0次
解题方法
3 . 某化学兴趣小组用以下装置制备 并探究其部分性质。
并探究其部分性质。
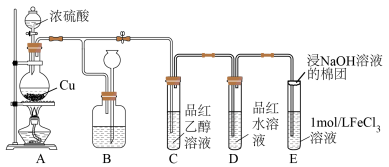
(1)装置A中制备 的化学反应方程式为
的化学反应方程式为___________ ,装置B可贮存多余的 ,B中试剂瓶内应盛放的液体是
,B中试剂瓶内应盛放的液体是___________ (填字母)。
a. 溶液 b.饱和
溶液 b.饱和 溶液 c.水 d.溴水
溶液 c.水 d.溴水
(2)若装置C中溶液无明显现象,装置D中溶液红色褪去,说明使品红水溶液褪色的含硫微粒一定不是___________ (填化学式)。
(3)通入 后,E中溶液立即由棕黄色变成红棕色,将混合液静置12小时后,溶液变成浅绿色。查阅资料,发现溶液出现红棕色是因为
后,E中溶液立即由棕黄色变成红棕色,将混合液静置12小时后,溶液变成浅绿色。查阅资料,发现溶液出现红棕色是因为 (红棕色)。
(红棕色)。
①溶液中产生 的离子方程式为
的离子方程式为___________ 。与该过程发生的其他化学反应相比, 与
与 反应生成
反应生成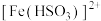 的反应速率
的反应速率___________ (填“快”或“慢”)。
②红棕色的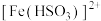 与
与 反应,溶液变成浅绿色,反应的离子方程式为
反应,溶液变成浅绿色,反应的离子方程式为___________ ,与该过程发生的其他化学反应相比,该反应的反应速率___________ (填“快”或“慢”)。
③为了缩短红棕色变为浅绿色的时间,该小组进行如下实验:
实验Ⅰ:往5mL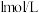
 溶液中通入
溶液中通入 ,微热3分钟,溶液变为浅绿色。
,微热3分钟,溶液变为浅绿色。
实验Ⅱ:用浓盐酸酸化 溶液后再通入
溶液后再通入 ,几分钟后,溶液变为浅绿色。
,几分钟后,溶液变为浅绿色。
结论:通过___________ 可缩短浅绿色出现的时间。
 并探究其部分性质。
并探究其部分性质。
(1)装置A中制备
 的化学反应方程式为
的化学反应方程式为 ,B中试剂瓶内应盛放的液体是
,B中试剂瓶内应盛放的液体是a.
 溶液 b.饱和
溶液 b.饱和 溶液 c.水 d.溴水
溶液 c.水 d.溴水(2)若装置C中溶液无明显现象,装置D中溶液红色褪去,说明使品红水溶液褪色的含硫微粒一定不是
(3)通入
 后,E中溶液立即由棕黄色变成红棕色,将混合液静置12小时后,溶液变成浅绿色。查阅资料,发现溶液出现红棕色是因为
后,E中溶液立即由棕黄色变成红棕色,将混合液静置12小时后,溶液变成浅绿色。查阅资料,发现溶液出现红棕色是因为 (红棕色)。
(红棕色)。①溶液中产生
 的离子方程式为
的离子方程式为 与
与 反应生成
反应生成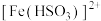 的反应速率
的反应速率②红棕色的
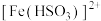 与
与 反应,溶液变成浅绿色,反应的离子方程式为
反应,溶液变成浅绿色,反应的离子方程式为③为了缩短红棕色变为浅绿色的时间,该小组进行如下实验:
实验Ⅰ:往5mL
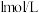
 溶液中通入
溶液中通入 ,微热3分钟,溶液变为浅绿色。
,微热3分钟,溶液变为浅绿色。实验Ⅱ:用浓盐酸酸化
 溶液后再通入
溶液后再通入 ,几分钟后,溶液变为浅绿色。
,几分钟后,溶液变为浅绿色。结论:通过
您最近一年使用:0次
4 .  是中学化学重要的氧化物之一,在生产、生活中应用也十分广泛。某化学兴趣小组为制备、收集并探究
是中学化学重要的氧化物之一,在生产、生活中应用也十分广泛。某化学兴趣小组为制备、收集并探究 的性质。利用下图装置进行实验。
的性质。利用下图装置进行实验。

(1)装置A中,盛装浓硫酸的仪器名称是___________ 。
(2)装置B中盛装的也是浓硫酸,装置B的作用是___________ 。
(3)装置D中的现象为___________ ;体现了 的
的___________ 性。
(4)装置D中,浸有 溶液的碱性棉球的作用是
溶液的碱性棉球的作用是___________ 。若将碱性棉球改为浸 溶液,会在棉球上出现黄色固体,该反应的化学方程式为
溶液,会在棉球上出现黄色固体,该反应的化学方程式为___________ 。
(5)若将 通入
通入 溶液中,发生反应的离子方程式为
溶液中,发生反应的离子方程式为___________ 。检验生成的阴离子的实验操作及现象是___________ 。
 是中学化学重要的氧化物之一,在生产、生活中应用也十分广泛。某化学兴趣小组为制备、收集并探究
是中学化学重要的氧化物之一,在生产、生活中应用也十分广泛。某化学兴趣小组为制备、收集并探究 的性质。利用下图装置进行实验。
的性质。利用下图装置进行实验。
(1)装置A中,盛装浓硫酸的仪器名称是
(2)装置B中盛装的也是浓硫酸,装置B的作用是
(3)装置D中的现象为
 的
的(4)装置D中,浸有
 溶液的碱性棉球的作用是
溶液的碱性棉球的作用是 溶液,会在棉球上出现黄色固体,该反应的化学方程式为
溶液,会在棉球上出现黄色固体,该反应的化学方程式为(5)若将
 通入
通入 溶液中,发生反应的离子方程式为
溶液中,发生反应的离子方程式为
您最近一年使用:0次
名校
解题方法
5 . 下列实验操作、现象和结论都正确的是
| 选项 | 实验操作 | 实验目的 |
| A | 向FeCl3(含少量CuCl2杂质)溶液中加入足量铁粉,待充分反应后过滤 | 提纯FeCl3 |
| B | 向 溶液中通入过量的CO2气体,有白色沉淀生成 溶液中通入过量的CO2气体,有白色沉淀生成 | 验证元素非金属性:C>Si |
| C | SO2通入含有酚酞的NaOH溶液中,红色消失 | 验证SO2具有漂白性 |
| D | 充分加热过量铁粉和硫粉的混合物,冷却后取少量固体于试管中,加入足量稀硫酸,再滴 溶液,产生蓝色沉淀 溶液,产生蓝色沉淀 | 说明铁被硫氧化至Fe(Ⅱ) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 某兴趣小组利用如图装置探究黑面包实验(蔗糖均为10 g),实验记录如下,下列说法错误的是
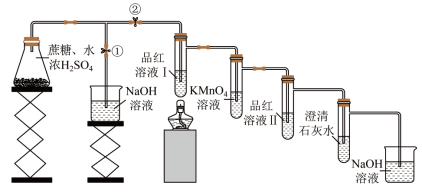

| 实验编号 | 实验条件 | 黑面包的高度/cm | 品红溶液Ⅰ | 品红溶液Ⅰ加热后 |  溶液 溶液 | 品红溶液Ⅱ | 澄清石灰水 | |
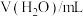 | V(浓 )/mL )/mL | |||||||
| 1 | 1 | 8 | 3.5 | 褪色 | 变红 | 颜色变浅 | 不变 | 变浑浊 |
| 2 | 1.5 | 4.7 | 褪色 | 变红 | 颜色变浅 | 不变 | 变浑浊 | |
| 3 | 2 | 3.8 | 褪色 | 变红 | 褪色 | 不变 | 变浑浊 | |
A.该装置可以防止过量的 污染空气 污染空气 |
B.品红溶液Ⅱ是为了检验 是否除尽 是否除尽 |
C.根据实验3的实验现象不能推出生成物中含有 |
D.根据实验3的现象分析,C与浓 反应产生的 反应产生的 气体较多 气体较多 |
您最近一年使用:0次
2023-04-19更新
|
122次组卷
|
2卷引用:重庆市乌江新高考协作体2022-2023学年高一下学期7月期末考试化学试题
名校
解题方法
7 . 某研究小组用如图装置制取 并对其性质进行相关实验(夹持装置已略去)。
并对其性质进行相关实验(夹持装置已略去)。
(1)装置A中发生反应的化学方程式为_______ 。
(2)D中观察到的现象是_______ ;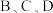 三支试管中的现象分别体现了
三支试管中的现象分别体现了 的漂白性、
的漂白性、_______ 性和_______ 性。
(3)写出C中反应的离子方程式:_______ 。
(4)仪器X的名称是_______ ;E装置的作用是_______ ,E装置中发生反应的化学方程式为_______ 。
(5)实验结束发现装置A中Y型试管产生白色固体,倾斜使左侧的物质全部转移到右侧水中,这时看到溶液的颜色为_______ 色。
 并对其性质进行相关实验(夹持装置已略去)。
并对其性质进行相关实验(夹持装置已略去)。
(1)装置A中发生反应的化学方程式为
(2)D中观察到的现象是
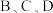 三支试管中的现象分别体现了
三支试管中的现象分别体现了 的漂白性、
的漂白性、(3)写出C中反应的离子方程式:
(4)仪器X的名称是
(5)实验结束发现装置A中Y型试管产生白色固体,倾斜使左侧的物质全部转移到右侧水中,这时看到溶液的颜色为
您最近一年使用:0次
2022-10-08更新
|
220次组卷
|
2卷引用:重庆市巫山县官渡中学2021-2022学年高一下学期期末考试化学试题
8 . SO2和Cl2是中学化学中常见的气体,探究二者的制法和性质是十分重要的内容。
(1)实验室可通过铜与浓硫酸加热制SO2。请写出该反应的化学方程式_______ ,该反应中氧化剂与还原剂的物质的量之比为:_______ 。
(2)某同学用如图装置探究SO2、Cl2的化学性质。通过控制弹簧夹a、b,向X中分别通入不同气体:
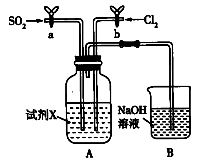
①若关闭b,打开a,X溶液为品红溶液,则X中的现象为_______ ,说明二氧化硫具有_______ 性。
②若关闭a,打开b,X溶液为紫色石蕊试液,则X中的现象为_______ 。
③若同时打开a、b,X溶液为紫色石蕊试液,同时通入体积比(同温同压)为1:1的气体,则X中的现象为_______ ,与②中现象不同的原因是_______ (用化学方程式表示)。
(1)实验室可通过铜与浓硫酸加热制SO2。请写出该反应的化学方程式
(2)某同学用如图装置探究SO2、Cl2的化学性质。通过控制弹簧夹a、b,向X中分别通入不同气体:

①若关闭b,打开a,X溶液为品红溶液,则X中的现象为
②若关闭a,打开b,X溶液为紫色石蕊试液,则X中的现象为
③若同时打开a、b,X溶液为紫色石蕊试液,同时通入体积比(同温同压)为1:1的气体,则X中的现象为
您最近一年使用:0次
2021-05-20更新
|
315次组卷
|
4卷引用:重庆市巫山大昌中学校2021-2022学年高一下学期期末考试化学试题
重庆市巫山大昌中学校2021-2022学年高一下学期期末考试化学试题武汉市江夏实验高中2020-2021学年高一下学期3月月考化学试题(已下线)4.1.1 二氧化硫的性质与应用-2021-2022学年高一化学课后培优练(苏教版2019必修第一册)云南省弥勒市第一中学2021-2022学年高一下学期第四次月考化学试题
9 . 某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验时,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气。为了验证甲、乙两位同学的判断是否正确,丙同学设计了如图所示实验装置(锌与浓硫酸共热时产生的气体为X,且该装置略去),试回答下列问题:
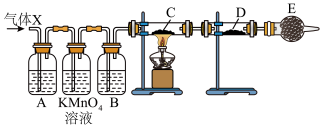
(1)上述反应中生成二氧化硫的化学方程式为__ 。
(2)乙同学认为还可能产生氢气的理由是__ 。
(3)丙同学在安装好装置后,必须首先进行的一步操作是__ 。
(4)A中加入的试剂可能是__ ,作用是__ ;B中加入的试剂可能是__ ,作用是__ ;E中加入的试剂可能是__ ,作用是__ 。
(5)可以证明气体X中含有氢气的实验现象是:
C中:__ ,
D中:__ 。
如果去掉装置B,还能否根据D中的现象判断气体X中有氢气?__ (填“能”或“不能”),原因是_ 。

(1)上述反应中生成二氧化硫的化学方程式为
(2)乙同学认为还可能产生氢气的理由是
(3)丙同学在安装好装置后,必须首先进行的一步操作是
(4)A中加入的试剂可能是
(5)可以证明气体X中含有氢气的实验现象是:
C中:
D中:
如果去掉装置B,还能否根据D中的现象判断气体X中有氢气?
您最近一年使用:0次
2020-04-26更新
|
1548次组卷
|
21卷引用:09-10年万州二中高一下学期期末考试化学卷
(已下线)09-10年万州二中高一下学期期末考试化学卷上海市上海中学2016—2017学年高一上学期期末考试化学试题吉林省长春汽车经济开发区第六中学2017-2018学年高一下学期4月月考化学试题【全国百强校】四川省南充高级中学2017-2018学年高一下学期期中考试化学试题(已下线)2018年12月16日 《每日一题》人教必修1- 每周一测【校级联考】黑龙江省哈尔滨市呼兰一中、阿城二中、宾县三中、尚志五中四校2018-2019学年高一下学期期中考试(呼兰用卷)化学试题(已下线)2019年12月15日 《每日一题》化学人教版(必修1)——每周一测鲁科版高中化学必修1第三章《自然界中的元素》测试卷苏教版高中化学必修1专题四《硫、氮和可持续发展》测试卷5.1.2 硫酸不同价态含硫物质的转化——2020年春高一新人教版第二册化学一课一练2020年春高一化学新人教版第二册课后同步:5.1.2 硫酸不同价态含硫物质的转化云南省昆明市东川区明月中学2018-2019学年高一下学期期中考试化学试题苏教版(2020)高一必修第一册专题4第一单元课时2 硫酸鲁科版(2019)高一必修第一册第3章 物质的性质与转化 第2节 硫的转化 课时2 硫酸鲁科版(2019)高一必修第一册第三章第2节 硫的转化 课时4 不同价态硫元素之间的转化酸雨及其防治高一必修第二册(人教2019版)第五章 第一节 硫及其化合物 课时2 硫酸及硫酸根离子的检验高一必修第一册(苏教2019版)专题4 B 素养拓展区 过素养 学科素养拓展训练辽宁省海城市高中教育集团2019-2020学年高一下学期6月联考化学试题(已下线)4.1.2 硫酸的工业制备 浓硫酸的性质(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)(已下线)第02讲 三氧化硫和硫酸(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)(已下线)3.1.2 浓硫酸和硫酸盐-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)
10 . 根据下图所示实验回答下列问题:

(1)装置A中试管内发生反应的化学方程式是_________________________________ 。
(2)根据装置B中的现象可以证明SO2具有__________ 性,反应一段时间后,将装置B中试管加热,可以观察到_______________________ 。
(3)装置C中试管口的棉花团上发生反应的离子方程式为________________________ 。
(4)如果将装置B换成装置D,并从直立导管中向氯化钡溶液中通入另一种气体,产生白色沉淀,则这种气体可能是_________________ (填一种即可)。

(1)装置A中试管内发生反应的化学方程式是
(2)根据装置B中的现象可以证明SO2具有
(3)装置C中试管口的棉花团上发生反应的离子方程式为
(4)如果将装置B换成装置D,并从直立导管中向氯化钡溶液中通入另一种气体,产生白色沉淀,则这种气体可能是
您最近一年使用:0次
2019-12-06更新
|
285次组卷
|
2卷引用:重庆市大足区2018-2019学年高一下学期期末考试化学试题



