名校
解题方法
1 . 某小组根据 既有还原性又有氧化性,探究其能否实现
既有还原性又有氧化性,探究其能否实现 或
或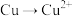 的转化。
的转化。
已知:ⅰ.水合 既易被氧化也易被还原,因此水溶液中无法生成水合
既易被氧化也易被还原,因此水溶液中无法生成水合 。
。
ⅱ. 为白色固体,难溶于水,可溶于
为白色固体,难溶于水,可溶于 较大的溶液生成
较大的溶液生成 ,也可溶于氨水生成
,也可溶于氨水生成 (无色)。
(无色)。
Ⅰ. 与
与 的反应
的反应
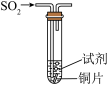
向试管中通入足量 (尾气处理装置已略),记录如下。
(尾气处理装置已略),记录如下。
(1)基态 的价层电子排布式为
的价层电子排布式为_______ 。
(2)将b所得沉淀过滤,充分洗涤,进行下列实验,证实该沉淀为 。
。 ,推理过程是
,推理过程是_______ 。
②ⅲ排除了干扰 检验的因素。写出ⅲ中反应的离子方程式:
检验的因素。写出ⅲ中反应的离子方程式:_______ ;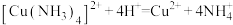 。
。
(3)进一步证实b中 作还原剂,补全实验方案和预期现象:取b中反应后的上层清液于试管中,
作还原剂,补全实验方案和预期现象:取b中反应后的上层清液于试管中,_______ 。
(4)由实验Ⅰ可推知,该条件下:①a中 不能将
不能将 还原为
还原为 或
或 ;
;
② 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为_______ 。
综上所述,改变还原产物的价态或形态可以影响氧化还原反应能否发生。
Ⅱ. 与
与 的反应
的反应
向试管中通入足量 (尾气处理装置已略),记录如下
(尾气处理装置已略),记录如下
(5)证明d所得棕色溶液含有 :用滴管吸取少量棕色溶液,滴入蒸馏水中,出现白色沉淀。用平衡移动原理解释产生该现象的原因:
:用滴管吸取少量棕色溶液,滴入蒸馏水中,出现白色沉淀。用平衡移动原理解释产生该现象的原因:_______ 。
(6)经进一步检验,铜表面黑色物质为 。补全d中反应的离子方程式:
。补全d中反应的离子方程式:________ _______ 。
 既有还原性又有氧化性,探究其能否实现
既有还原性又有氧化性,探究其能否实现 或
或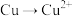 的转化。
的转化。已知:ⅰ.水合
 既易被氧化也易被还原,因此水溶液中无法生成水合
既易被氧化也易被还原,因此水溶液中无法生成水合 。
。ⅱ.
 为白色固体,难溶于水,可溶于
为白色固体,难溶于水,可溶于 较大的溶液生成
较大的溶液生成 ,也可溶于氨水生成
,也可溶于氨水生成 (无色)。
(无色)。Ⅰ.
 与
与 的反应
的反应向试管中通入足量
 (尾气处理装置已略),记录如下。
(尾气处理装置已略),记录如下。| 装置 | 编号 | 试剂 | 实验现象 |
| a | 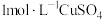 溶液 溶液 | 始终无明显变化 |
| b | 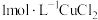 溶液 溶液 | 溶液变绿,进而变棕黄色,一段时间后出现白色沉淀 |
 的价层电子排布式为
的价层电子排布式为(2)将b所得沉淀过滤,充分洗涤,进行下列实验,证实该沉淀为
 。
。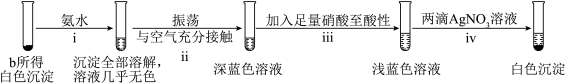
 ,推理过程是
,推理过程是②ⅲ排除了干扰
 检验的因素。写出ⅲ中反应的离子方程式:
检验的因素。写出ⅲ中反应的离子方程式: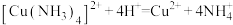 。
。(3)进一步证实b中
 作还原剂,补全实验方案和预期现象:取b中反应后的上层清液于试管中,
作还原剂,补全实验方案和预期现象:取b中反应后的上层清液于试管中,(4)由实验Ⅰ可推知,该条件下:①a中
 不能将
不能将 还原为
还原为 或
或 ;
;②
 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为综上所述,改变还原产物的价态或形态可以影响氧化还原反应能否发生。
Ⅱ.
 与
与 的反应
的反应向试管中通入足量
 (尾气处理装置已略),记录如下
(尾气处理装置已略),记录如下| 装置 | 编号 | 试剂 | 实验现象 |
| c |  稀硫酸 稀硫酸 | 始终无明显变化 |
| d |  稀盐酸 稀盐酸 | 铜片表面变黑,溶液变为棕色 |
 :用滴管吸取少量棕色溶液,滴入蒸馏水中,出现白色沉淀。用平衡移动原理解释产生该现象的原因:
:用滴管吸取少量棕色溶液,滴入蒸馏水中,出现白色沉淀。用平衡移动原理解释产生该现象的原因:(6)经进一步检验,铜表面黑色物质为
 。补全d中反应的离子方程式:
。补全d中反应的离子方程式:
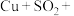


 _______
_______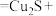

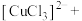
 _______。
_______。
您最近一年使用:0次
2023-01-06更新
|
984次组卷
|
5卷引用:北京市第四中学2023-2024学年高三上学期期中考试化学试题
(已下线)北京市第四中学2023-2024学年高三上学期期中考试化学试题(已下线)北京市第四中学2023-2024学年高三上学期 期中化学试卷北京市东城区2022-2023学年高三上学期1月期末统一检测化学试卷江西省贵溪市实验中学2023-2024学年高三上学期9月第一次月考化学试题北京市第八中学2023-2024学年高三上学期12月月考化学试题
20-21高三上·浙江绍兴·期中
解题方法
2 . I.由三种元素组成的化合物A,其相对分子质量小于200,按如下流程进行实验。气体B为红棕色混合物,气体D能使带火星的木条复燃,溶液E为蓝色,固体C为混合物,固体F为紫红色。
(1)组成A的三种元素是_______ 。(填元素符号),A的化学式是________ 。
(2)固体A加热分解的化学方程式是________ 。
(3)若固体G的组成与A类似,且隔绝空气加热后红棕色气体与带火星木条复燃气体的物质的量为8:1,该反应的化学方程式是。___________ 。
II.某兴趣小组为制取并验证二氧化硫的性质进行相关实验,实验装置如图所示。请回答:___________ 。
(2)写出烧杯中过量的NaClO溶液吸收SO2的离子反应方程式___________ 。

(1)组成A的三种元素是
(2)固体A加热分解的化学方程式是
(3)若固体G的组成与A类似,且隔绝空气加热后红棕色气体与带火星木条复燃气体的物质的量为8:1,该反应的化学方程式是。
II.某兴趣小组为制取并验证二氧化硫的性质进行相关实验,实验装置如图所示。请回答:
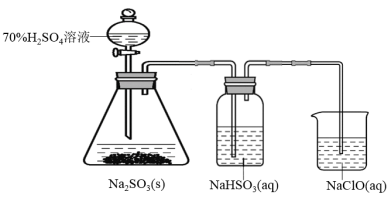
(2)写出烧杯中过量的NaClO溶液吸收SO2的离子反应方程式
您最近一年使用:0次
3 . 某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示:

(1)SO2气体还原Fe3+反应的产物是_____________ 、_____________ (填离子符号)。
(2)下列实验方案可以用于在实验室制取所需SO2的是____ 。
(3)装置C的作用是_____________ 。
(4)如果有280 mL SO2气体(已折算为标态)进入C装置中,则C中50 mL NaOH溶液的浓度至少为_____________ mol/L才能达到目的。
(5)在上述装置中通入过量的SO2为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去。
方案②:往第一份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是____ ,原因是_______________________________________ 。
(6)能表明I-的还原性弱于SO2的现象是_________________________________________ ,写出有关离子方程式:_______________________________________ 。

(1)SO2气体还原Fe3+反应的产物是
(2)下列实验方案可以用于在实验室制取所需SO2的是
| A.Na2SO3溶液与HNO3 | B.Na2SO3固体与浓硫酸 |
| C.固体硫在纯氧中燃烧 | D.铜与热浓H2SO4 |
(3)装置C的作用是
(4)如果有280 mL SO2气体(已折算为标态)进入C装置中,则C中50 mL NaOH溶液的浓度至少为
(5)在上述装置中通入过量的SO2为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去。
方案②:往第一份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是
(6)能表明I-的还原性弱于SO2的现象是
您最近一年使用:0次