名校
解题方法
1 . 探究硫及其化合物的性质,下列方案设计、现象和结论中有不正确的是
实验方案 | 现象 | 结论 | |
A | 在过硫化钠(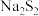 )中加入稀盐酸 )中加入稀盐酸 | 产生淡黄色沉淀和臭鸡蛋气味的气体。 | 发生歧化反应: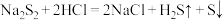 |
B | 已知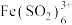 呈红棕色,将 呈红棕色,将 气体通入 气体通入 溶液中 溶液中 | 溶液先变为红棕色,过一段时间又变成浅绿色。 |  与 与 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大。 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大。 |
C | 燃着的镁条插入盛有 的集气瓶中。冷却后,往集气瓶中加入适量稀盐酸,静置,取少量上层清液于试管中,滴加少量 的集气瓶中。冷却后,往集气瓶中加入适量稀盐酸,静置,取少量上层清液于试管中,滴加少量 溶液。 溶液。 | 剧烈燃烧,集气瓶口有淡黄色固体附着,集气瓶底有白色固体生成。试管中没有产生黑色沉淀 | 镁能在 中燃烧: 中燃烧: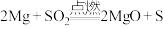 |
D | 探究电石与水的反应 | 将电石与饱和食盐水反应产生的气体通入酸性高锰酸钾溶液,观察现象 | 若酸性高锰酸钾溶液褪色,说明电石与水反应生成了乙炔 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-22更新
|
1772次组卷
|
6卷引用:江西省抚州市乐安县第二中学2023-2024学年高三上学期11月期中化学试题
江西省抚州市乐安县第二中学2023-2024学年高三上学期11月期中化学试题浙江省天域全国名校协作体2022-2023学年高三下学期4月阶段性联考化学试题重庆市万州第二高级中学2023-2024学年高三上学期7月月考化学试题(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)湖南省长沙市第一中学2023-2024学年高三上学期月考卷(三)化学试题2024年山东省潍坊市高三下学期高考模拟训练调研试题(二)
22-23高三上·北京东城·期末
名校
解题方法
2 . 某小组根据 既有还原性又有氧化性,探究其能否实现
既有还原性又有氧化性,探究其能否实现 或
或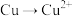 的转化。
的转化。
已知:ⅰ.水合 既易被氧化也易被还原,因此水溶液中无法生成水合
既易被氧化也易被还原,因此水溶液中无法生成水合 。
。
ⅱ. 为白色固体,难溶于水,可溶于
为白色固体,难溶于水,可溶于 较大的溶液生成
较大的溶液生成 ,也可溶于氨水生成
,也可溶于氨水生成 (无色)。
(无色)。
Ⅰ. 与
与 的反应
的反应
向试管中通入足量 (尾气处理装置已略),记录如下。
(尾气处理装置已略),记录如下。
(1)基态 的价层电子排布式为
的价层电子排布式为_______ 。
(2)将b所得沉淀过滤,充分洗涤,进行下列实验,证实该沉淀为 。
。
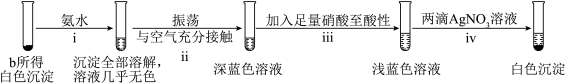
①证明白色沉淀中有 ,推理过程是
,推理过程是_______ 。
②ⅲ排除了干扰 检验的因素。写出ⅲ中反应的离子方程式:
检验的因素。写出ⅲ中反应的离子方程式:_______ ;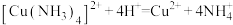 。
。
(3)进一步证实b中 作还原剂,补全实验方案和预期现象:取b中反应后的上层清液于试管中,
作还原剂,补全实验方案和预期现象:取b中反应后的上层清液于试管中,_______ 。
(4)由实验Ⅰ可推知,该条件下:①a中 不能将
不能将 还原为
还原为 或
或 ;
;
② 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为_______ 。
综上所述,改变还原产物的价态或形态可以影响氧化还原反应能否发生。
Ⅱ. 与
与 的反应
的反应
向试管中通入足量 (尾气处理装置已略),记录如下
(尾气处理装置已略),记录如下
(5)证明d所得棕色溶液含有 :用滴管吸取少量棕色溶液,滴入蒸馏水中,出现白色沉淀。用平衡移动原理解释产生该现象的原因:
:用滴管吸取少量棕色溶液,滴入蒸馏水中,出现白色沉淀。用平衡移动原理解释产生该现象的原因:_______ 。
(6)经进一步检验,铜表面黑色物质为 。补全d中反应的离子方程式:
。补全d中反应的离子方程式:________

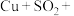


 _______
_______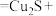

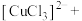
 _______。
_______。
(7)与c对比,d能发生反应的原因是_______ 。
 既有还原性又有氧化性,探究其能否实现
既有还原性又有氧化性,探究其能否实现 或
或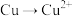 的转化。
的转化。已知:ⅰ.水合
 既易被氧化也易被还原,因此水溶液中无法生成水合
既易被氧化也易被还原,因此水溶液中无法生成水合 。
。ⅱ.
 为白色固体,难溶于水,可溶于
为白色固体,难溶于水,可溶于 较大的溶液生成
较大的溶液生成 ,也可溶于氨水生成
,也可溶于氨水生成 (无色)。
(无色)。Ⅰ.
 与
与 的反应
的反应向试管中通入足量
 (尾气处理装置已略),记录如下。
(尾气处理装置已略),记录如下。| 装置 | 编号 | 试剂 | 实验现象 |
 | a | 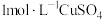 溶液 溶液 | 始终无明显变化 |
| b | 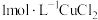 溶液 溶液 | 溶液变绿,进而变棕黄色,一段时间后出现白色沉淀 |
 的价层电子排布式为
的价层电子排布式为(2)将b所得沉淀过滤,充分洗涤,进行下列实验,证实该沉淀为
 。
。
①证明白色沉淀中有
 ,推理过程是
,推理过程是②ⅲ排除了干扰
 检验的因素。写出ⅲ中反应的离子方程式:
检验的因素。写出ⅲ中反应的离子方程式: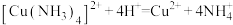 。
。(3)进一步证实b中
 作还原剂,补全实验方案和预期现象:取b中反应后的上层清液于试管中,
作还原剂,补全实验方案和预期现象:取b中反应后的上层清液于试管中,(4)由实验Ⅰ可推知,该条件下:①a中
 不能将
不能将 还原为
还原为 或
或 ;
;②
 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为综上所述,改变还原产物的价态或形态可以影响氧化还原反应能否发生。
Ⅱ.
 与
与 的反应
的反应向试管中通入足量
 (尾气处理装置已略),记录如下
(尾气处理装置已略),记录如下| 装置 | 编号 | 试剂 | 实验现象 |
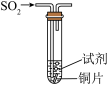 | c |  稀硫酸 稀硫酸 | 始终无明显变化 |
| d |  稀盐酸 稀盐酸 | 铜片表面变黑,溶液变为棕色 |
 :用滴管吸取少量棕色溶液,滴入蒸馏水中,出现白色沉淀。用平衡移动原理解释产生该现象的原因:
:用滴管吸取少量棕色溶液,滴入蒸馏水中,出现白色沉淀。用平衡移动原理解释产生该现象的原因:(6)经进一步检验,铜表面黑色物质为
 。补全d中反应的离子方程式:
。补全d中反应的离子方程式:
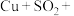


 _______
_______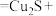

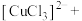
 _______。
_______。(7)与c对比,d能发生反应的原因是
您最近一年使用:0次
2023-01-06更新
|
966次组卷
|
5卷引用:北京市第四中学2023-2024学年高三上学期期中考试化学试题
(已下线)北京市第四中学2023-2024学年高三上学期期中考试化学试题(已下线)北京市第四中学2023-2024学年高三上学期 期中化学试卷北京市东城区2022-2023学年高三上学期1月期末统一检测化学试卷江西省贵溪市实验中学2023-2024学年高三上学期9月第一次月考化学试题北京市第八中学2023-2024学年高三上学期12月月考化学试题
20-21高三上·浙江绍兴·期中
解题方法
3 . I.由三种元素组成的化合物A,其相对分子质量小于200,按如下流程进行实验。气体B为红棕色混合物,气体D能使带火星的木条复燃,溶液E为蓝色,固体C为混合物,固体F为紫红色。

请回答:
(1)组成A的三种元素是_______ 。(填元素符号),A的化学式是________ 。
(2)固体A加热分解的化学方程式是________ 。
(3)若固体G的组成与A类似,且隔绝空气加热后红棕色气体与带火星木条复燃气体的物质的量为8:1,该反应的化学方程式是。___________ 。
II.某兴趣小组为制取并验证二氧化硫的性质进行相关实验,实验装置如图所示。请回答:
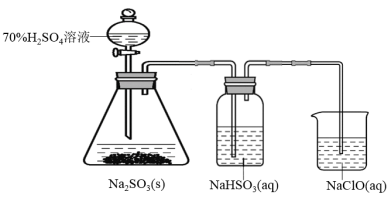
(1)饱和NaHSO3溶液的作用是___________ 。
(2)写出烧杯中过量的NaClO溶液吸收SO2的离子反应方程式___________ 。

请回答:
(1)组成A的三种元素是
(2)固体A加热分解的化学方程式是
(3)若固体G的组成与A类似,且隔绝空气加热后红棕色气体与带火星木条复燃气体的物质的量为8:1,该反应的化学方程式是。
II.某兴趣小组为制取并验证二氧化硫的性质进行相关实验,实验装置如图所示。请回答:

(1)饱和NaHSO3溶液的作用是
(2)写出烧杯中过量的NaClO溶液吸收SO2的离子反应方程式
您最近一年使用:0次
名校
4 . 向含a mol NaClO的溶液通入b mol SO2充分反应(不考虑二氧化硫与水之间的反应以及次氯酸的分解)。下列说法不正确的是
A.当0<b<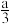 时:SO2+H2O+3ClO-= 时:SO2+H2O+3ClO-= +2HClO+Cl- +2HClO+Cl- |
B.当b=a时:SO2+H2O+ClO-= +2H++Cl- +2H++Cl- |
C.当 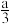 <b<a时;反应后溶液中H+的物质的量:0<n(H+)<2bmol <b<a时;反应后溶液中H+的物质的量:0<n(H+)<2bmol |
D.当0<b<a时;反应后溶液中Cl-、ClO-和 物质的量之比为:(a-b):b:b 物质的量之比为:(a-b):b:b |
您最近一年使用:0次
2017-05-27更新
|
675次组卷
|
4卷引用:安徽省亳州市蒙城县五校联考2023-2024学年高三上学期11月期中考试化学试题
5 . 某无色混合气体,可能含有CO、H2、SO2、Cl2、HCl中的一种或几种,把此混合气体通过少量澄清石灰水,无沉淀生成;再通过少量品红溶液,完全褪色;随后将该气体通过足量的氢氧化钠溶液后,再通过足量红热的CuO粉末,粉末变成红色;最后通入CaCl2溶液中,无沉淀生成,则下列关于此混合气体的叙述正确的是
| A.澄清石灰水中无沉淀,说明一定不含有SO2 |
| B.品红褪色,可能是Cl2导致的 |
| C.氧化铜粉末变红,说明CO和H2中至少有一种 |
| D.CaCl2溶液中无沉淀,说明通过CuO后得到的气体中一定不含有CO2 |
您最近一年使用:0次
2017-05-05更新
|
5342次组卷
|
12卷引用:上海市复旦大学附中浦东分校2016-2017学年高一下学期期中考试化学试题
上海市复旦大学附中浦东分校2016-2017学年高一下学期期中考试化学试题【全国百强校】云南省曲靖市第一中学2018-2019学年高一下学期期中考试化学试题山东省济宁市嘉祥县第一中学2021-2022学年高三上学期期中考试化学试题广东省大联考2021-2022学年高一下学期期中检测化学试题黑龙江省哈尔滨市德强学校2021-2022学年高一下学期期中考试化学试题安徽省合肥市第六中学2019-2020学年高一下学期开学考试化学试题山西省实验中学2021届高三9月月考化学试题高一必修第一册(苏教2019) 模块综合测评安徽省灵璧县第一中学2020-2021学年高一上学期12月月考试题山西省实验中学2020-2021学年高三上学期第一次月考化学试题上海市复旦大学附属中学2022-2023学年高一下学期阶段测试化学试题辽宁省沈阳市第一二〇中学2023-2024学年高三上学期第一次质量检测化学试题
6 . 某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示:

(1)SO2气体还原Fe3+反应的产物是_____________ 、_____________ (填离子符号)。
(2)下列实验方案可以用于在实验室制取所需SO2的是____ 。
(3)装置C的作用是_____________ 。
(4)如果有280 mL SO2气体(已折算为标态)进入C装置中,则C中50 mL NaOH溶液的浓度至少为_____________ mol/L才能达到目的。
(5)在上述装置中通入过量的SO2为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去。
方案②:往第一份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是____ ,原因是_______________________________________ 。
(6)能表明I-的还原性弱于SO2的现象是_________________________________________ ,写出有关离子方程式:_______________________________________ 。

(1)SO2气体还原Fe3+反应的产物是
(2)下列实验方案可以用于在实验室制取所需SO2的是
| A.Na2SO3溶液与HNO3 | B.Na2SO3固体与浓硫酸 |
| C.固体硫在纯氧中燃烧 | D.铜与热浓H2SO4 |
(3)装置C的作用是
(4)如果有280 mL SO2气体(已折算为标态)进入C装置中,则C中50 mL NaOH溶液的浓度至少为
(5)在上述装置中通入过量的SO2为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去。
方案②:往第一份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是
(6)能表明I-的还原性弱于SO2的现象是
您最近一年使用:0次



