名校
1 . 某学习小组设计了如图装置用于制取 并验证其性质。
并验证其性质。 的仪器名称为
的仪器名称为__________ ,装置F中的溶液为_________ 。
(2)装置B中长颈漏斗的作用是_________________ 。
(3)装置C中酸性高锰酸钾溶液褪色,试写出该反应的离子方程式:________ 。该现象能验证 具有
具有__________ (填“漂白性”“氧化性”或“还原性”)。
(4)装置D中开始没有白色沉淀产生,但随着反应的进行,发现装置D中产生了少量白色沉淀。为进一步探究产生沉淀的原因,某实验小组进行如下实验:分别用煮沸和未煮沸过的蒸馏水配制的 和
和 溶液,操作装置如图所示。
溶液,操作装置如图所示。
①据G中现象推测D中产生的白色沉淀的化学式是___________ 。
②据I中出现白色沉淀的速率比H中快很多的现象,推测其根本原因可能是______________ 。
(5)该实验小组用200mL 0.01 碘溶液(含两滴淀粉溶液)测定空气中
碘溶液(含两滴淀粉溶液)测定空气中 含量,若气体流速为
含量,若气体流速为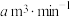 ,当观察装置内
,当观察装置内_________ 时,结束计时,时间为t min,则空气中 的含量为
的含量为_______ 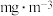 。
。
 并验证其性质。
并验证其性质。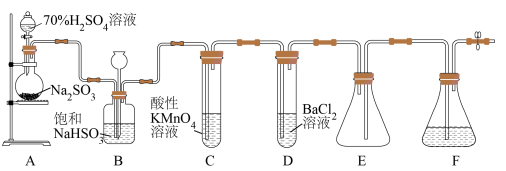
 的仪器名称为
的仪器名称为(2)装置B中长颈漏斗的作用是
(3)装置C中酸性高锰酸钾溶液褪色,试写出该反应的离子方程式:
 具有
具有(4)装置D中开始没有白色沉淀产生,但随着反应的进行,发现装置D中产生了少量白色沉淀。为进一步探究产生沉淀的原因,某实验小组进行如下实验:分别用煮沸和未煮沸过的蒸馏水配制的
 和
和 溶液,操作装置如图所示。
溶液,操作装置如图所示。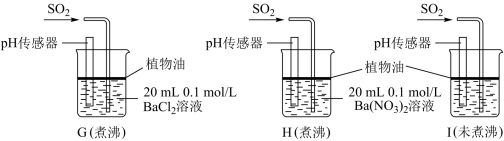
烧杯 | 实验现象 |
G | 无白色沉淀产生,pH传感器测得溶液pH=5.3 |
H | 有白色沉淀产生 |
I | 有白色沉淀产生,I中出现白色沉淀比H中快很多 |
②据I中出现白色沉淀的速率比H中快很多的现象,推测其根本原因可能是
(5)该实验小组用200mL 0.01
 碘溶液(含两滴淀粉溶液)测定空气中
碘溶液(含两滴淀粉溶液)测定空气中 含量,若气体流速为
含量,若气体流速为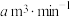 ,当观察装置内
,当观察装置内 的含量为
的含量为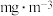 。
。
您最近一年使用:0次
名校
解题方法
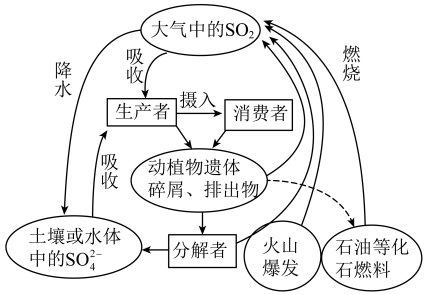
2 . 硫是生物必需的大量营养元素之一,下图是自然界中硫的循环图,在循环过程中S的价态变化在-2价至+6价之间,请分析此图并回答有关问题:______ 。
A.硫化氢分子很稳定,受热难分解
B.硫化氢分子中所有原子的最外层都达到8电子结构
C.将硫化氢通入硫酸亚铁溶液,产生沉淀
D.硫化氢中硫元素为-2价,因此只有还原性,没有氧化性
E.硫化氢可在空气中燃烧生成二氧化硫
(2)大中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。收集某次酸雨样品,发现8小时内,样品pH一直在减小,其原因可能是___________ (用化学方程式表示)。
(3)研究发现,空气中少量的NO2也能参与硫酸型酸雨的形成,反应过程如下:
①SO+NO2→SO3+NO ②SO3+H2O→H2SO4 ③2NO+O2→2NO2
NO2在上述过程中的作用,与H2SO4在下列变化中的作用不符的是___________。
(4)在制葡萄酒时可以人工添加SO2,有两个目的:抗氧化和抗菌,实验室模拟二氧化硫抗氧化过程,向溴水中通入SO2,请用离子方程式表示该反应原理___________ 。发酵酒卫生标准中对葡萄酒中的二氧化硫含量有要求:总SO2小于250mg/L,若在室温下。每升溶液中最多通入___________ mL SO2.(室温下Vm=24.5L/mol,结果保留3位有效数字,体积变化忽略不计)
(5)明代《徐光启手迹》记载了用硫酸盐制备硝酸的方法,其主要流程(部分产物已省略)如下:___________ 。
②关于整个制备过程,下列说法正确的是___________ 。
A.本流程涉及复分解反应
B.由H2SO4制HNO3利用了强酸制弱酸原理
C.制备使用的铁锅易损坏
(6)工业上为了防止制硫酸过程中产生污染,可以利用氧化亚铁硫杆菌(T·f)对硫铁矿进行催化脱硫,该过程如图所示:___________ 。
②脱硫过程中产生的 在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式
在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式___________ 。
③从氧化还原角度分析,若要制备Na2S2O3应选择___________ (填字母)。
A.SO2+Na2SO4 B.Na2S+S C.Na2SO3+Na2SO4 D.Na2SO3+S
A.硫化氢分子很稳定,受热难分解
B.硫化氢分子中所有原子的最外层都达到8电子结构
C.将硫化氢通入硫酸亚铁溶液,产生沉淀
D.硫化氢中硫元素为-2价,因此只有还原性,没有氧化性
E.硫化氢可在空气中燃烧生成二氧化硫
(2)大中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。收集某次酸雨样品,发现8小时内,样品pH一直在减小,其原因可能是
(3)研究发现,空气中少量的NO2也能参与硫酸型酸雨的形成,反应过程如下:
①SO+NO2→SO3+NO ②SO3+H2O→H2SO4 ③2NO+O2→2NO2
NO2在上述过程中的作用,与H2SO4在下列变化中的作用不符的是___________。
| A.潮湿的氯气通过盛有浓H2SO4的洗气瓶 |
| B.硫化氢通入浓H2SO4中 |
| C.浓H2SO4滴入萤石中,加热 |
| D.向盐酸中加入浓硫酸产生白雾 |
(4)在制葡萄酒时可以人工添加SO2,有两个目的:抗氧化和抗菌,实验室模拟二氧化硫抗氧化过程,向溴水中通入SO2,请用离子方程式表示该反应原理
(5)明代《徐光启手迹》记载了用硫酸盐制备硝酸的方法,其主要流程(部分产物已省略)如下:

②关于整个制备过程,下列说法正确的是
A.本流程涉及复分解反应
B.由H2SO4制HNO3利用了强酸制弱酸原理
C.制备使用的铁锅易损坏
(6)工业上为了防止制硫酸过程中产生污染,可以利用氧化亚铁硫杆菌(T·f)对硫铁矿进行催化脱硫,该过程如图所示:
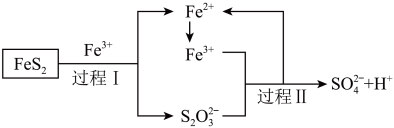
②脱硫过程中产生的
 在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式
在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式③从氧化还原角度分析,若要制备Na2S2O3应选择
A.SO2+Na2SO4 B.Na2S+S C.Na2SO3+Na2SO4 D.Na2SO3+S
您最近一年使用:0次
3 . 某同学用下列装置完成了浓硫酸和SO2性质实验(夹持装置已省略),下列说法中错误的是
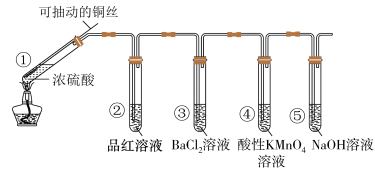
| A.为确认生成CuSO4,向试管①中加水,观察溶液颜色 |
| B.试管②与试管④溶液褪色的原理不同 |
| C.取下试管③并不断振荡,出现浑浊,是因为生成了BaSO4 |
| D.试管⑤可以改为装有碱石灰的干燥管 |
您最近一年使用:0次
名校
解题方法
4 . 宏观辨识与微观探析是化学学科核心素养之一,下列物质性质实验对应的离子方程式书写正确的是
A.明矾溶液中滴入Ba(OH)2溶液使 恰好完全沉淀:2Ba2++3OH-+Al3++2 恰好完全沉淀:2Ba2++3OH-+Al3++2 =2BaSO4↓+Al(OH)3↓ =2BaSO4↓+Al(OH)3↓ |
B.NO2通入水中制硝酸:2NO2+H2O=2H++ +NO +NO |
C.H2SO3溶液中滴入氯化钙溶液: +Ca2+=CaSO3↓ +Ca2+=CaSO3↓ |
D.SO2通入酸性KMnO4溶液中:5SO2+2H2O+2 =5 =5 +4H++2Mn2+ +4H++2Mn2+ |
您最近一年使用:0次
名校
5 . 认识物质的性质,我们一般可以从物质类别与核心元素的价态来认识。如图是某元素的“价—类”二维图,其中单质b是黄色固体,f、h均为正盐,且焰色都是黄色。下列说法不正确的是

| A.a与c能反应生成b |
B.不能用 溶液鉴别f和h的溶液 溶液鉴别f和h的溶液 |
| C.e的浓溶液可使蔗糖变黑,产生刺激性气味的气体 |
| D.能使品红溶液褪色的物质一定为c |
您最近一年使用:0次
名校
解题方法
6 . 生活中,化学无处不在。下列说法不正确的是
| A.二氧化硫可用于杀菌消毒,还是一种食品添加剂 |
| B.碳酸钡可用于胃肠X射线造影检查 |
| C.可用氢氟酸溶蚀玻璃生产磨砂玻璃 |
| D.锂离子电池因高效、安全、环保,在手机、笔记本电脑、照相机中有广泛应用 |
您最近一年使用:0次
名校
解题方法
7 . 将SO2分别通入无氧、有氧的浓度均为0.1mol∙L-1的BaCl2溶液和Ba(NO3)2溶液中,除BaCl2溶液(无氧)外,都产生白色沉淀。实验测得各溶液pH变化曲线如图。下列说法不正确的是

A.曲线a所示溶液pH降低的原因: |
B.依据曲线b可推知 溶液(无氧)能氧化 溶液(无氧)能氧化 |
C.曲线c所示溶液中发生反应的离子方程式为: |
D.曲线d所表示的过程中 是氧化SO2的主要微粒 是氧化SO2的主要微粒 |
您最近一年使用:0次
名校
解题方法
8 . 在给定条件下,下列选项中所示的物质间转化均能实现的是
A.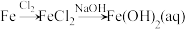 |
B. |
C. |
D.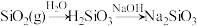 |
您最近一年使用:0次
名校
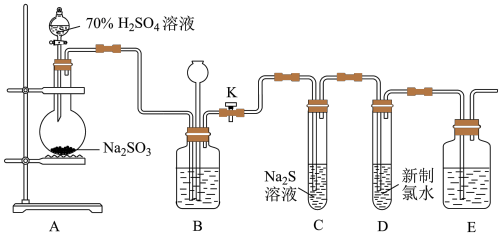
9 . 实验室可用下列装置(部分夹持仪器略去)制取SO2并验证其性质。_______ ,则气密性良好。
(2)装置A中反应的化学方程式为_______ 。
(3)实验时,通气一段时间后,C中试管中出现大量淡黄色浑浊现象,证明二氧化硫具有_______ (填“还原性”、“氧化性”或“漂白性”);经测定,产物中含有一种摩尔质量为104g/mol的盐,该盐的化学式为_______ 。
(4)试管D中反应的离子方程式为_______ 。
(5)实验结束时,关闭止水夹K,装置B的作用是_______ 。
(6)用图所示装置验证H2SO3酸性比H2CO3强。_______ ,Y为_______ ,Z为_______ 。
(2)装置A中反应的化学方程式为
(3)实验时,通气一段时间后,C中试管中出现大量淡黄色浑浊现象,证明二氧化硫具有
(4)试管D中反应的离子方程式为
(5)实验结束时,关闭止水夹K,装置B的作用是
(6)用图所示装置验证H2SO3酸性比H2CO3强。
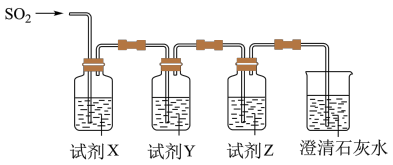
您最近一年使用:0次
名校
解题方法
10 . 下列离子方程式不正确的是
A.铜与浓硝酸反应: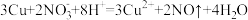 |
B.向CuCl2溶液中加入Na2S溶液: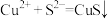 |
C.二氧化硅与氢氧化钠反应:SiO2+2OH-= +H2O +H2O |
D.SO2通入酸性KMnO4溶液中: |
您最近一年使用:0次



