1 . 化学中常用类比的方法可预测许多物质的性质。如根据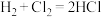 推测:
推测: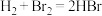 。但类比是相对的,如根据
。但类比是相对的,如根据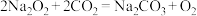 ,推测:
,推测: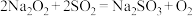 是错误的,应该是
是错误的,应该是 。下列左边正确,类推法应用于右边也正确的是
。下列左边正确,类推法应用于右边也正确的是
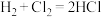 推测:
推测: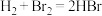 。但类比是相对的,如根据
。但类比是相对的,如根据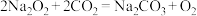 ,推测:
,推测: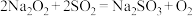 是错误的,应该是
是错误的,应该是 。下列左边正确,类推法应用于右边也正确的是
。下列左边正确,类推法应用于右边也正确的是| A | 钠与水反应生成NaOH和 | 所有金属与水反应都生成碱和 |
| B |  通入漂白粉溶液中 通入漂白粉溶液中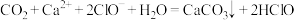 |  通入漂白粉溶液中 通入漂白粉溶液中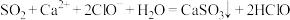 |
| C |  是碱性氧化物 是碱性氧化物 |  也是碱性氧化物 也是碱性氧化物 |
| D | 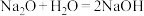 | 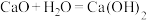 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 下列反应过程对应的离子方程式书写正确的是
A.向 溶液中通入过量 溶液中通入过量 |
B.向氯化铝溶液中加入小苏打溶液: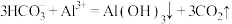 |
C.向 溶液中加入 溶液中加入 溶液: 溶液: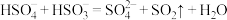 |
D.向稀硝酸中加入 溶液: 溶液: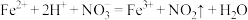 |
您最近一年使用:0次
2023-12-13更新
|
195次组卷
|
3卷引用:陕西省西安市2023-2024学年高三上学期12月联考化学试卷
3 . 某小组设计实验探究 的性质,装置如图所示。
的性质,装置如图所示。
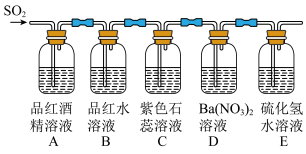
观察到的实验现象如下:
已知:NO能被酸性 氧化成
氧化成 ,与碱石灰不反应。
,与碱石灰不反应。
回答下列问题:
(1)实验室制 宜选择下列试剂中的__________(填标号)。
宜选择下列试剂中的__________(填标号)。
(2)依据实验现象判断 在
在___________ (填化学式)存在下表现漂白性,预测C中现象是___________ 。
(3)D中产生的白色沉淀是_______ (填化学式),D中发生反应的离子方程式为________ 。
(4)E中现象表明 具有的性质是
具有的性质是___________ (填标号)。
a.漂白性 b.酸性 c.氧化性 d.还原性
(5)为了证明 的漂白性是暂时性的,请设计一个补充实验:
的漂白性是暂时性的,请设计一个补充实验:___________ 。
(6)为处理上述实验尾气,下列装置中可供选择的是___________ (填标号)。

 的性质,装置如图所示。
的性质,装置如图所示。
观察到的实验现象如下:
| 装置标号 | A | B | C | D | E |
| 现象 | 溶液不褪色 | 溶液变无色 | ? | 产生白色沉淀 | 产生黄色浑浊 |
 氧化成
氧化成 ,与碱石灰不反应。
,与碱石灰不反应。回答下列问题:
(1)实验室制
 宜选择下列试剂中的__________(填标号)。
宜选择下列试剂中的__________(填标号)。A. 粉末和浓硝酸 粉末和浓硝酸 | B. 粉末和70%浓硫酸 粉末和70%浓硫酸 |
C. 粉末和30%稀硝酸 粉末和30%稀硝酸 | D. 粉末和10%盐酸 粉末和10%盐酸 |
(2)依据实验现象判断
 在
在(3)D中产生的白色沉淀是
(4)E中现象表明
 具有的性质是
具有的性质是a.漂白性 b.酸性 c.氧化性 d.还原性
(5)为了证明
 的漂白性是暂时性的,请设计一个补充实验:
的漂白性是暂时性的,请设计一个补充实验:(6)为处理上述实验尾气,下列装置中可供选择的是

您最近一年使用:0次
2023-11-10更新
|
208次组卷
|
2卷引用:陕西省渭南市尚德中学2023-2024学年高三上学期期中考试化学试卷
4 . 某学习小组探究铜跟浓硫酸的反应时,利用如图实验装置进行相关实验。
按要求填写下列空白:
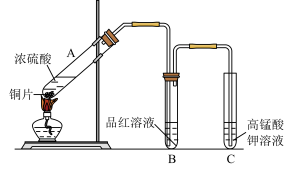
(1)装置A中发生的化学反应方程式为___________ 。
(2)实验过程中装置C中溶液褪色说明装置A中产生的气体具有___________ 性。
(3)有学生提出装置C的试管口还应放置一团浸有NaOH溶液的棉花,其目的是___________ 。
(4)实验结束拆开装置后,加热装置B的试管,观察到的现象是___________ 。
(5)根据氮及其化合物 转化关系回答下列问题:
转化关系回答下列问题:
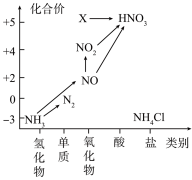
①X的化学式为___________ ,从化合价上看,X具有___________ 性(填“氧化”或“还原”)。
②写出实验制取氨气的化学方程式___________ ;
③下列试剂不能用于干燥NH3的是___________ (填字母)。
A.浓硫酸 B.碱石灰 C.NaOH固体
④NH3→NO的化学方程式为___________ 。
按要求填写下列空白:

(1)装置A中发生的化学反应方程式为
(2)实验过程中装置C中溶液褪色说明装置A中产生的气体具有
(3)有学生提出装置C的试管口还应放置一团浸有NaOH溶液的棉花,其目的是
(4)实验结束拆开装置后,加热装置B的试管,观察到的现象是
(5)根据氮及其化合物
 转化关系回答下列问题:
转化关系回答下列问题:
①X的化学式为
②写出实验制取氨气的化学方程式
③下列试剂不能用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.NaOH固体
④NH3→NO的化学方程式为
您最近一年使用:0次
5 . 研究硫及其化合物的应用价值对于社会发展意义重大。请回答以下问题:
(1)欲制备Na2S2O3,从氧化还原角度分析,下列方法合理的是___________(选填字母序号)。
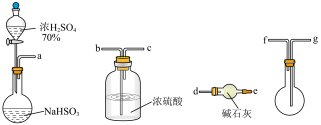
(2)用下图所示装置制备纯净的SO2(同时生成一种正盐),请写出发生装置中反应的化学方程式为___________ ,碱石灰的主要作用为___________ 。
(3)工业上回收利用SO2的一种途径是: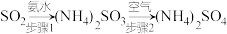 。
。
①写出少量SO2通入氨水发生的离子方程式___________ 。
②某实验小组为测定步骤2溶液中(NH4)2SO3的氧化率α,设计了以下实验方案。[提示:氧化率 ]
]
【方案一】一定条件下向100mL1mol∙L-的(NH4)2SO3溶液中通入空气后,先加入足量的稀盐酸,充分反应后,再加入足量BaCl2溶液,过滤、洗涤、烘干,得到沉淀18.64g。
I.计算(NH4)2SO3的氧化率α=___________ (用百分数表示)。
【方案二】一定条件下向100mLc0 mol∙L-1的(NH4)2SO3溶液中通入空气后,取20.00mL反应后的溶液于锥形瓶中,用浓度为c mol∙L-1的KMnO4标准溶液(经H2SO4酸化)滴定,滴定过程中锰元素被还原成Mn2+。重复操作三次,恰好完全反应时平均消耗KMnO4溶液的体积是Vml。
Ⅱ.写出滴定反应的离子方程式___________ 。
(1)欲制备Na2S2O3,从氧化还原角度分析,下列方法合理的是___________(选填字母序号)。
| A.Na2S+S | B.Na2SO3+S | C.Na2SO3+H2SO4 | D.SO2+Na2SO3 |

(3)工业上回收利用SO2的一种途径是:
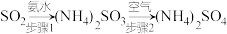 。
。①写出少量SO2通入氨水发生的离子方程式
②某实验小组为测定步骤2溶液中(NH4)2SO3的氧化率α,设计了以下实验方案。[提示:氧化率
 ]
]【方案一】一定条件下向100mL1mol∙L-的(NH4)2SO3溶液中通入空气后,先加入足量的稀盐酸,充分反应后,再加入足量BaCl2溶液,过滤、洗涤、烘干,得到沉淀18.64g。
I.计算(NH4)2SO3的氧化率α=
【方案二】一定条件下向100mLc0 mol∙L-1的(NH4)2SO3溶液中通入空气后,取20.00mL反应后的溶液于锥形瓶中,用浓度为c mol∙L-1的KMnO4标准溶液(经H2SO4酸化)滴定,滴定过程中锰元素被还原成Mn2+。重复操作三次,恰好完全反应时平均消耗KMnO4溶液的体积是Vml。
Ⅱ.写出滴定反应的离子方程式
您最近一年使用:0次
6 . 在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验图以确认上述混合气体中有C2H4和SO2。回答下列问题:

(1)I、II、III、IV装置可盛放的试剂是:I___________ ;II___________ ;III___________ ;IV___________ (将下列有关试剂的序号填入空格内)。
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(2)能说明SO2气体存在的现象是___________ 。
(3)使用装置II的目的是___________ 。
(4)使用装置III的目的是___________ 。
(5)确定含有乙烯的现象是___________ 。

(1)I、II、III、IV装置可盛放的试剂是:I
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(2)能说明SO2气体存在的现象是
(3)使用装置II的目的是
(4)使用装置III的目的是
(5)确定含有乙烯的现象是
您最近一年使用:0次
2023-06-29更新
|
61次组卷
|
18卷引用:陕西省西安市蓝田县大学区联考2022-2023学年高二下学期4月期中考试化学试题
陕西省西安市蓝田县大学区联考2022-2023学年高二下学期4月期中考试化学试题山东省德州市齐河县实验中学2019-2020学年高一下学期期中考试化学试题陕西省西安市蓝田县大学区联考2022-2023学年高二下学期6月期末考试化学试题(已下线)2012年人教版高中化学选修5 2.1脂肪烃练习卷(已下线)2014年高一化学人教版必修2 3.2.1乙烯练习卷内蒙古北京八中乌兰察布分校2016-2017学年高一下学期第二次调考化学试题高二人教版选修5 第三章 烃的含氧衍生物 第一节 醇酚云南省绥江县一中2018-2019学年高一下学期期末考试化学试题吉林省公主岭市范家屯镇第一中学2019-2020学年高二上学期第二次月考化学试题黑龙江省大兴安岭地区漠河县第一中学2018-2019学年高二上学期第一次月考化学试题课时1 石油的炼制 乙烯——A学习区 夯实基础(鲁科版必修2)课时1 甲烷 石油的炼制与乙烯——A学习区 夯实基础(鲁科版(2019)第二册)福建省莆田第七中学2020-2021学年高二上学期第一次月考化学试题上海市奉城高级中学2018-2019学年高二上学期期末考试化学试题安徽省安庆桐城市第八中学2020-2021学年高二上学期第一次段考化学试题黑龙江省双鸭山市第一中学2020-2021学年高二下学期4月月考化学试题云南省元阳县一中2020-2021学年高一下学期6月份考试化学试题2.1.1有机化学反应的主要类型(课前)-鲁科版选择性必修3
名校
7 . 关于下列物质的性质描述正确的是
| A.SO2能使酸性高锰酸钾溶液褪色,说明SO2具有漂白性 |
| B.H2S不能和CuSO4溶液反应,因为弱酸不能制强酸 |
| C.常温下,浓硫酸可以用铁罐储存和运输,说明铁在常温下与浓硫酸不反应 |
| D.蔗糖与浓硫酸反应有黑色物质和刺激性气体生成,体现了浓硫酸的脱水性和强氧化性 |
您最近一年使用:0次
名校
8 . NA代表阿伏加德罗常数的值。下列说法正确的是
| A.常温常压下,124 g P4中所含P-P键数目为4NA |
| B.58.5gNaCl中含有NA个NaCl分子 |
| C.标准状况下,11.2 L NO和O2混合气体中含原子数目为NA |
| D.密闭容器中,2 mol SO2和1 mol O2充分反应后分子总数为2NA |
您最近一年使用:0次
9 . 某小组为验证 的性质设计如图所示的实验装置,下列说法错误的是
的性质设计如图所示的实验装置,下列说法错误的是
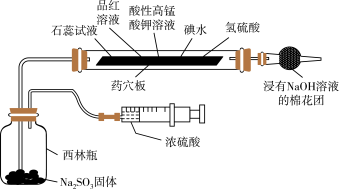
 的性质设计如图所示的实验装置,下列说法错误的是
的性质设计如图所示的实验装置,下列说法错误的是
| A.该装置能体现实验的微型化和绿色化 |
B.一段时间后氢硫酸溶液中有淡黄色沉淀生成,说明 有氧化性 有氧化性 |
C.一段时间后石蕊试液和品红溶液均褪色,说明 有漂白性 有漂白性 |
D.一段时间后酸性高锰酸钾溶液、碘水褪色,说明 有还原性 有还原性 |
您最近一年使用:0次
10 . 化学兴趣小组制备 并探究
并探究 的部分性质,实验装置如图所示。
的部分性质,实验装置如图所示。
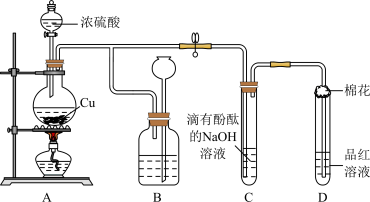
(1)装置A烧瓶中发生反应的化学方程式为_______ 。
(2)装置A制取 的反应中,体现了浓硫酸的
的反应中,体现了浓硫酸的_______ 性和_______ 性,_______ (填“能”或“不能”)用浓盐酸代替浓硫酸来制取 。
。
(3)装置B的作用是贮存多余的气体,B广口瓶内应盛放的液体是_______ (填序号)。
①水 ②饱和 溶液 ③NaOH溶液 ④酸性
溶液 ③NaOH溶液 ④酸性
(4)装置C和D中产生的现象相同,但原因却不同。C中是由于 与溶液中的NaOH反应使碱性减弱,而D中则是由于
与溶液中的NaOH反应使碱性减弱,而D中则是由于 具有
具有_______ 性。
(5)装置D中试管口塞一团棉花,棉花中应浸有一种液体,其作用是_______ 。
(6) 为无色、有强烈刺激性气味的气体,是大气主要污染物之一,具有一定的还原性。探究
为无色、有强烈刺激性气味的气体,是大气主要污染物之一,具有一定的还原性。探究 气体还原
气体还原 、
、 的装置如图所示:
的装置如图所示:
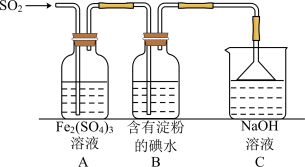
①在上述装置中通入过量的 ,为了验证A中
,为了验证A中 与
与 发生了氧化还原反应,取A中的溶液,分成两份,并设计了如下实验:
发生了氧化还原反应,取A中的溶液,分成两份,并设计了如下实验:
方案a:往第一份溶液中加入少量酸性 溶液,紫红色褪去。
溶液,紫红色褪去。
方案b:往第二份溶液中加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
上述方案不合理的是_______ (填“a”或“b”),理由是_______ 。
②在上述装置中能表明 的还原性强于
的还原性强于 的现象是
的现象是_______ 。
 并探究
并探究 的部分性质,实验装置如图所示。
的部分性质,实验装置如图所示。
(1)装置A烧瓶中发生反应的化学方程式为
(2)装置A制取
 的反应中,体现了浓硫酸的
的反应中,体现了浓硫酸的 。
。(3)装置B的作用是贮存多余的气体,B广口瓶内应盛放的液体是
①水 ②饱和
 溶液 ③NaOH溶液 ④酸性
溶液 ③NaOH溶液 ④酸性
(4)装置C和D中产生的现象相同,但原因却不同。C中是由于
 与溶液中的NaOH反应使碱性减弱,而D中则是由于
与溶液中的NaOH反应使碱性减弱,而D中则是由于 具有
具有(5)装置D中试管口塞一团棉花,棉花中应浸有一种液体,其作用是
(6)
 为无色、有强烈刺激性气味的气体,是大气主要污染物之一,具有一定的还原性。探究
为无色、有强烈刺激性气味的气体,是大气主要污染物之一,具有一定的还原性。探究 气体还原
气体还原 、
、 的装置如图所示:
的装置如图所示:
①在上述装置中通入过量的
 ,为了验证A中
,为了验证A中 与
与 发生了氧化还原反应,取A中的溶液,分成两份,并设计了如下实验:
发生了氧化还原反应,取A中的溶液,分成两份,并设计了如下实验:方案a:往第一份溶液中加入少量酸性
 溶液,紫红色褪去。
溶液,紫红色褪去。方案b:往第二份溶液中加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
上述方案不合理的是
②在上述装置中能表明
 的还原性强于
的还原性强于 的现象是
的现象是
您最近一年使用:0次
2023-04-27更新
|
117次组卷
|
2卷引用:陕西省咸阳市武功县2022-2023学年高一下学期4月期中化学试题



