名校
1 . 研究表明,我国酸雨区域占国土面积的40%以上,我国农业每年因遭受酸雨而造成经济损失高达15亿多元,酸雨的防治迫在眉睫。
(1) 是形成酸雨的主要物质之一,模仿示例图“
是形成酸雨的主要物质之一,模仿示例图“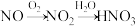 ”,画出由
”,画出由 形成硫酸型酸雨的可能的过程
形成硫酸型酸雨的可能的过程___________ 。
(2)某地降雨经检验,除 和
和 外,还含有
外,还含有 、
、 、
、 、
、 它们的浓度如下:
它们的浓度如下:
则该降雨的pH为___________ ,该降雨___________ (选填“是”或“不是”)酸雨。
(3)常温下,下列三种溶液:
①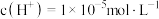 ②
②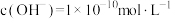 ③
③
按溶液酸性由强到弱的顺序排列为___________ 。
(4)为了减少酸雨产生的途径,你认为可采取的措施为___________。
(1)
 是形成酸雨的主要物质之一,模仿示例图“
是形成酸雨的主要物质之一,模仿示例图“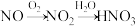 ”,画出由
”,画出由 形成硫酸型酸雨的可能的过程
形成硫酸型酸雨的可能的过程(2)某地降雨经检验,除
 和
和 外,还含有
外,还含有 、
、 、
、 、
、 它们的浓度如下:
它们的浓度如下:| 微粒 |  |  |  |  |  |  |
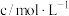 | ? |  |  |  | 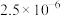 | 很小,可忽略 |
(3)常温下,下列三种溶液:
①
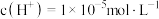 ②
②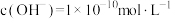 ③
③
按溶液酸性由强到弱的顺序排列为
(4)为了减少酸雨产生的途径,你认为可采取的措施为___________。
| A.把工厂烟囱造高 | B.在汽车排气管上安装汽车尾气催化转化器 |
| C.化石燃料脱硫 | D.在已酸化的土壤中加石灰 |
您最近一年使用:0次
解题方法
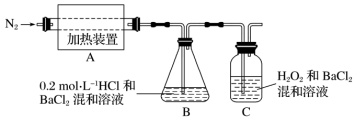
2 . 莫尔盐在500℃时隔绝空气加热完全分解,固体产物可能有FeO和Fe2O3,气体产物可能有NH3、SO3、H2O、N2和SO2,为检验分解产物的成分,设计如下实验装置进行实验。___________ 。
(2)为验证A中残留的铁的氧化物中是否含有FeO,需要选用的试剂有___________。
(3)装置B是为了检验分解产物是否有___________ 气体;装置C是为了检验分解产物是否有___________ 气体。
(4)若A中分解产物有N2,固体残留物只有Fe2O3,Fe2O3的物质的量为bmol,C中沉淀物质的量为amol,则b___________ a。
A.大于 B.小于 C.等于
(2)为验证A中残留的铁的氧化物中是否含有FeO,需要选用的试剂有___________。
| A.KSCN溶液 | B.稀硫酸 | C.浓盐酸 | D.KMnO4溶液 |
(4)若A中分解产物有N2,固体残留物只有Fe2O3,Fe2O3的物质的量为bmol,C中沉淀物质的量为amol,则b
A.大于 B.小于 C.等于
您最近一年使用:0次
名校
3 . 下列关于 和
和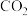 的比较正确的是
的比较正确的是
 和
和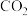 的比较正确的是
的比较正确的是| A.排放到空气中,都能加剧温室效应 | B.排放到空气中,都能形成酸雨 |
C.都不能和 溶液反应生成白色沉淀 溶液反应生成白色沉淀 | D.都能使澄清石灰水变浑浊 |
您最近一年使用:0次
名校
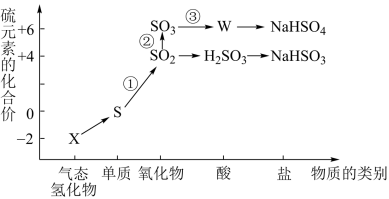
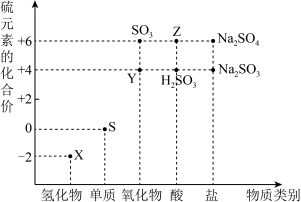
4 . 物质的类别和核心元素的化合价是研究物质性质的两个重要角度。下图所示是硫及其部分化合物的“价类二维图”。
1.X的化学式为___________ ,将X与 混合,可生成淡黄色固体,该反应的氧化产物与还原产物的质量之比为
混合,可生成淡黄色固体,该反应的氧化产物与还原产物的质量之比为___________ 。
2.过量的Zn粉与一定量W浓溶液混合加热反应,生成___________ (填化学式)气体。转化①可由S粉与热的W浓溶液反应实现,反应的化学方程式为___________ 。
3.欲制备 ,从氧化还原角度分析,下列合理的是___________(选填字母)
,从氧化还原角度分析,下列合理的是___________(选填字母)
1.X的化学式为
 混合,可生成淡黄色固体,该反应的氧化产物与还原产物的质量之比为
混合,可生成淡黄色固体,该反应的氧化产物与还原产物的质量之比为2.过量的Zn粉与一定量W浓溶液混合加热反应,生成
3.欲制备
 ,从氧化还原角度分析,下列合理的是___________(选填字母)
,从氧化还原角度分析,下列合理的是___________(选填字母)A. | B. | C. | D.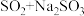 |
您最近一年使用:0次
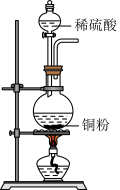
5 . 某化学兴趣小组在实验室用除去表面氧化物的铁钉(含碳元素)与浓硫酸共热制取SO2并完成相关性质探究(不考虑水蒸气)。
(1)有同学认为制得的SO2中可能混有杂质,其化学式为_____ 和______ ,原因是________ (用化学方程式表示)。
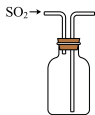
(2)为验证气体成分,兴趣小组同学设计了下图所示装置进行了实验探究:_______ ,装置C中品红溶液的作用是________ 。
②装置D中加入的试剂为________ 。
③装置G中可能出现的现象为__________ 。
④装置H的作用为______________ 。
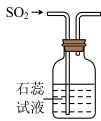
(3)兴趣小组设计如图装置验证二氧化硫的化学性质。_________ 。
②为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀;
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成;
上述方案中合理的是____ (填 “Ⅰ”“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为_______ 。
(1)有同学认为制得的SO2中可能混有杂质,其化学式为
(2)为验证气体成分,兴趣小组同学设计了下图所示装置进行了实验探究:
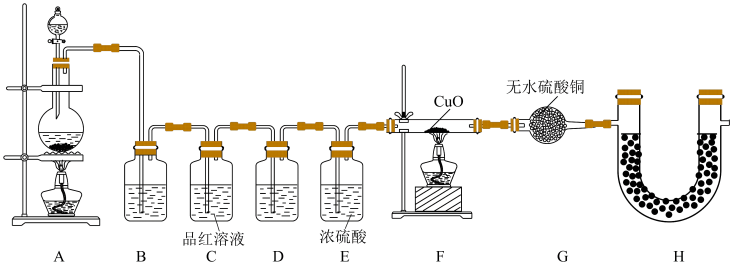
②装置D中加入的试剂为
③装置G中可能出现的现象为
④装置H的作用为
(3)兴趣小组设计如图装置验证二氧化硫的化学性质。
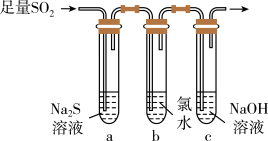
②为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀;
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成;
上述方案中合理的是
您最近一年使用:0次
名校
解题方法
6 .  俗称大苏打,是重要的化工原料。实验室用如下图所示的装置,模拟工业用含硫废水生产
俗称大苏打,是重要的化工原料。实验室用如下图所示的装置,模拟工业用含硫废水生产 。已知装置C中发生如下反应:
。已知装置C中发生如下反应:
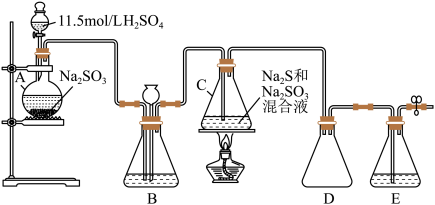
①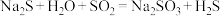 ②
② ③
③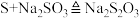
_______ 。
(2)仪器组装完成后,关闭所有活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若装置中出现_______ 现象,则整个装置气密性良好。
(3)装置E中的溶液为_______ ,此处发生反应的离子方程式为(任写一个)_______ 。
(4)装置B可用于观察 的生成速率,其中的液体最好选择_______。
的生成速率,其中的液体最好选择_______。
(5) 固体长时间暴露在空气中会变质,若要检验某
固体长时间暴露在空气中会变质,若要检验某 样品是否变质,结合必要的离子方程式说明实验操作、现象和结论
样品是否变质,结合必要的离子方程式说明实验操作、现象和结论_______ 。
(6)实验前装置C溶液中含有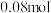
 和
和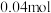
 ,反应结束后经一系列操作,得到纯净的
,反应结束后经一系列操作,得到纯净的 晶体19.11g,则
晶体19.11g,则 的产率为
的产率为_______ (保留2位有效数字)。(已知 的式量为248,
的式量为248,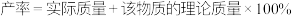 )
)
 俗称大苏打,是重要的化工原料。实验室用如下图所示的装置,模拟工业用含硫废水生产
俗称大苏打,是重要的化工原料。实验室用如下图所示的装置,模拟工业用含硫废水生产 。已知装置C中发生如下反应:
。已知装置C中发生如下反应:①
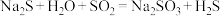 ②
② ③
③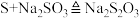
(2)仪器组装完成后,关闭所有活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若装置中出现
(3)装置E中的溶液为
(4)装置B可用于观察
 的生成速率,其中的液体最好选择_______。
的生成速率,其中的液体最好选择_______。| A.水 | B.饱和食盐水 | C.饱和 溶液 溶液 | D.饱和 溶液 溶液 |
(5)
 固体长时间暴露在空气中会变质,若要检验某
固体长时间暴露在空气中会变质,若要检验某 样品是否变质,结合必要的离子方程式说明实验操作、现象和结论
样品是否变质,结合必要的离子方程式说明实验操作、现象和结论(6)实验前装置C溶液中含有
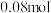
 和
和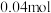
 ,反应结束后经一系列操作,得到纯净的
,反应结束后经一系列操作,得到纯净的 晶体19.11g,则
晶体19.11g,则 的产率为
的产率为 的式量为248,
的式量为248,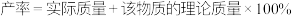 )
)
您最近一年使用:0次
名校
解题方法
7 . 某工厂每天燃烧含硫质量分数为0.64%的煤100吨,如果煤中的硫元素全部转化为 气体,且产生的
气体,且产生的 全部用来生产硫酸,理论上每年(按365天计)可得到质量分数为98%的浓硫酸的质量为
全部用来生产硫酸,理论上每年(按365天计)可得到质量分数为98%的浓硫酸的质量为_______ 吨。
 气体,且产生的
气体,且产生的 全部用来生产硫酸,理论上每年(按365天计)可得到质量分数为98%的浓硫酸的质量为
全部用来生产硫酸,理论上每年(按365天计)可得到质量分数为98%的浓硫酸的质量为
您最近一年使用:0次
名校
解题方法
8 . 如图是硫元素的“价—类”二维图:___________ 。
(2) 的浓溶液与铝单质在加热条件下可以发生化学反应生成
的浓溶液与铝单质在加热条件下可以发生化学反应生成 ,该反应的化学方程式为
,该反应的化学方程式为___________ ,可用___________ 法收集 。
。
A.向上排空气 B.向下排空气 C.排饱和食盐水 D.排饱和 溶液
溶液
(3) 和
和 均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。用离子方程式解释原因
均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。用离子方程式解释原因___________ 。
(2)
 的浓溶液与铝单质在加热条件下可以发生化学反应生成
的浓溶液与铝单质在加热条件下可以发生化学反应生成 ,该反应的化学方程式为
,该反应的化学方程式为 。
。A.向上排空气 B.向下排空气 C.排饱和食盐水 D.排饱和
 溶液
溶液(3)
 和
和 均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。用离子方程式解释原因
均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。用离子方程式解释原因
您最近一年使用:0次
名校
解题方法
9 . 钠碱法的启动吸收剂为 溶液,捕捉
溶液,捕捉 后生成
后生成 和
和 的混合液。
的混合液。
(1)工业上先用 溶液吸收
溶液吸收 ,再用
,再用 使
使 再生:NaOH溶液
再生:NaOH溶液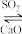 Na2SO3。使
Na2SO3。使 再生的原理是
再生的原理是___________ 。(用化学方程式表示)
(2)常温下进行“钠碱法”的模拟实验。用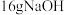 固体配成一定浓度的溶液,这些
固体配成一定浓度的溶液,这些 理论上最多可吸收
理论上最多可吸收 的体积约为
的体积约为___________  (折算成标准状况)。若实验时只吸收了
(折算成标准状况)。若实验时只吸收了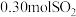 ,则反应后的吸收液中,溶质的组成为:
,则反应后的吸收液中,溶质的组成为:___________ 。(写出溶质组成和每种溶质的物质的量)
(3)若用碱液吸收工业尾气中的 后,得到等物质的量浓度的
后,得到等物质的量浓度的 和
和 溶液。继续向溶液中滴入几滴
溶液。继续向溶液中滴入几滴 溶液变浑浊,请写出发生反应的离子方程式
溶液变浑浊,请写出发生反应的离子方程式___________ 。
 溶液,捕捉
溶液,捕捉 后生成
后生成 和
和 的混合液。
的混合液。(1)工业上先用
 溶液吸收
溶液吸收 ,再用
,再用 使
使 再生:NaOH溶液
再生:NaOH溶液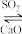 Na2SO3。使
Na2SO3。使 再生的原理是
再生的原理是(2)常温下进行“钠碱法”的模拟实验。用
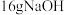 固体配成一定浓度的溶液,这些
固体配成一定浓度的溶液,这些 理论上最多可吸收
理论上最多可吸收 的体积约为
的体积约为 (折算成标准状况)。若实验时只吸收了
(折算成标准状况)。若实验时只吸收了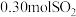 ,则反应后的吸收液中,溶质的组成为:
,则反应后的吸收液中,溶质的组成为:(3)若用碱液吸收工业尾气中的
 后,得到等物质的量浓度的
后,得到等物质的量浓度的 和
和 溶液。继续向溶液中滴入几滴
溶液。继续向溶液中滴入几滴 溶液变浑浊,请写出发生反应的离子方程式
溶液变浑浊,请写出发生反应的离子方程式
您最近一年使用:0次
名校
解题方法
10 . 研究 的性质有利于探索其资源化利用。下列实验方案设计正确的是
的性质有利于探索其资源化利用。下列实验方案设计正确的是
 的性质有利于探索其资源化利用。下列实验方案设计正确的是
的性质有利于探索其资源化利用。下列实验方案设计正确的是
|
|
 制取 制取 | B.收集 |
|
|
 验证 验证 水溶液的酸性 水溶液的酸性 |  验证 验证 的还原性 的还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次